2015-2016学年北京市东城区重点中学高三上学期期中化学试卷
2015-2016学年北京市东城区重点中学高三上学期期中化学试卷
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
对于某酸性溶液(可能含有Br﹣、SO4 2﹣、HSO3﹣、NH4+ ),分别进行如下实验:①加热时放出的气体可使品红溶液褪色;②加入碱溶液使溶液呈碱性,再加热时放出的气体可使湿润的红色石蕊试纸变蓝;③加入氯水时,溶液略呈橙红色;④加入BaCl2液和稀硝酸,产生不溶于稀硝酸的白色沉淀.对于下列微粒不能确定其在原溶液中是否存在的是( )
A . Br﹣
B . SO42﹣
C . HSO3﹣
D . NH4+
|
|
| 2. 单选题 | 详细信息 |
|
向0.1mol/L CH3COOH溶液中加入CH3COONa晶体或加水稀释时,都会引起( )
A . 溶液的pH增大
B . CH3COOH的电离程度增大
C . 溶液的导电能力减小
D . 溶液的c(OH﹣)减小
|
|
| 3. 单选题 | 详细信息 |
|
下列关于臭氧性质的叙述中,不正确的是( )
A . 臭氧比氧气的氧化性更强,常温下能将银、汞等较不活泼的金属氧化
B . 臭氧是比氯水更好的消毒剂,因为它在消灭细菌后变成O2 , 无污染
C . 臭氧和活性炭一样,能够吸附有机色素,是种很好的漂白剂
D . 臭氧和氧气在一定条件下可以相互转化
|
|
| 4. 单选题 | 详细信息 |
|
汽车的启动电源常用铅蓄电池,放电时的电池反应如下:PbO2+Pb+2H2SO4═2PbSO4+2H2O,根据此反应判断下列叙述中正确的是( )
A . PbO2是电池的负极
B . 负极的电极反应式为:Pb+SO42﹣﹣2e﹣═PbSO4
C . PbO2得电子,被氧化
D . 电池放电时,溶液酸性增强
|
|
| 5. 单选题 | 详细信息 |
|
一定条件下,可逆反应X(g)+3Y(g)⇌2Z(g),若X,Y,Z起始浓度分别为c1、c2、c3(均不为0,单位mol/L),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是( )
A . c1:c2=1:3
B . 平衡时,Y和Z的生成速率之比为3:2
C . X,Y的转化率不相等
D . c1的取值范围为0<c1<0.14mol/L
|
|
| 6. 单选题 | 详细信息 |
|
下列化合物中,既有离子键,又有共价键的是( )
A . CaO
B . SiO2
C . H2O
D . Na2O2
|
|
| 7. 单选题 | 详细信息 |
|
在2CH4(g)+2NH3(g)+3O2(g)=2HCN(g)+6H2O(g)反应中,已知v (HCN)=n mol/(L•min),且v(O2)=m mol/(L•min),则m与n的关系正确的是( )
A . m=
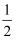 n
B . m= n
B . m= 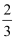 n
C . m= n
C . m=  n
D . m=2n n
D . m=2n
|
|
| 8. 单选题 | 详细信息 |
|
2003年10月15日我国成功发射了第一艘载人航天飞船﹣“神州五号”.从此我国进入了航天大国和航天强国行列.发射“神五”用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气.
已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7kJ/mol. N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=﹣534kJ/mol. 下列关于肼和NO2反应的热化学方程式中,正确的是( )
A . 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=﹣1135.7 kJ/mol
B . 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=﹣1000.3 kJ/mol
C . N2H4(g)+NO2(g)=3/2N2(g)+2H2O(l);△H=﹣1135.7 kJ/mol
D . 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=﹣1135.7 kJ/mol
|
|
| 9. 单选题 | 详细信息 |
|
从柑橘中可提炼得到结构为
A . 分子式为C10H16
B . 其一氯代物有8种
C . 能与溴水发生加成反应
D . 难溶于水,且密度比水大
|
|
| 10. 单选题 | 详细信息 |
|
一定温度下,某在物质水中的溶解度为S,计算该温度下这种饱和溶液中溶质的物质的量浓度,必不可少的物理量是 ( )
①溶液中溶质的摩尔质量②溶液中溶质和溶剂的质量比③溶液的密度④溶液的体积.
A . ①②
B . ②③
C . ①③
D . ②④
|
|
高中化学 试卷推荐
- 2015-2016学年北京市临川学校高二上学期期末化学试卷
- 高中化学鲁科版(2019)必修第二册 第2章测试卷
- 高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第一节 化学反应速率 化学反应速率
- 云南省大理市漾濞一中2019-2020学年高二上学期化学开学考试试卷
- 2015年东北三省四市教研联合体高考化学模拟试卷(三)
- 2015-2016学年山东省临沂市某重点中学高二下学期期末化学试卷
- 山东省临沂市蒙阴一中2016-2017学年高二上学期化学期中考试试卷
- 2015-2016学年山东省枣庄市滕州市实验高中高三上学期开学化学试卷
- 备考2018年高考化学二轮专题复习 总结复习:化学计算
- 广东省茂名市信宜中学2019-2020学年高一下学期化学期中考试试卷
- 2015-2016学年福建省莆田二十四中高二下学期期末化学试卷
- 广东省深圳市翠园、华侨城、三高、七高等校2019-2020学年高一上学期化学期中考试试卷
最近更新
- 电源电压为12V,将R1和R2串联到电源两端,已知R1的电阻值约为R2的2~4倍,用电压表测出R1两端的电压,用电流表测
- 下列向量组中能作为表示它们所在平面内的所有向量的基底的是( ) A.=(0,0), =(1,-2)
- 甲()可以通过下列路线合成(分离方法和其他产物已经略去): ①步骤Ⅰ的反应类型是____________________
- 12月27日至28日,湖南省人大常委会召开全体会议,对在衡阳市十四届人大一次会议期间,以贿赂手段当选的56名省人大代表,
- 在一密闭容器中,反应 aA(气) bB(气)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是
- 如图(1),等边△ABC中,D是AB边上的动点,以CD为一边,向上作等边△EDC,连接AE. (1)求证:AE∥BC;
- 宋代,儒家学者的继承人理学家开始从一个新的角度来思考社会的伦理纲常。这个新的角度是 A.从矛盾对立转换出发 B.从
- Our teacher ______ all of us to sit in a circle for a discus
- 使用电热水壶烧水,具有便捷、环保等优点。如图是某电热水壶的铭牌,假设电热水壶的电阻保持不变,已知水的比热容为c水=4.2
- 下列关于内环境的叙述正确的是 A.内环境指的是细胞内液 B.细胞与外界环境之间的物质交换,必须通过内环境才能进行 C.神
- △ABC的三个内角A,B,C所对的边分别为a,b,c,asin Asin B+bcos2A=a,则=() A.2
- 1689年英国议会颁布的《权利法案》沿袭了罗马法的精神,又开启了近代民主代议制的先河,其在世界民主化进程中最为深远的影响
- www. Chester City Library offers arange of Library Special N
- 面临金融危机带来的经济寒流,东亚一些学者提出抱团取暖的设想,即建立像欧盟一样的“东亚联盟”。如果这个设想变成现实,那么该
- 下列叙述正确的是( ) A.化学反应除了生成新的物质外,还伴随着能量的变化 B.物质燃烧一定是放热反应 C.放热的
- 下列成语出自城濮之战的是( ) A、卧薪尝胆 B、围魏救赵 C、退避三舍
- 下列关于地球内部结构的叙述正确的是( ) A.地球内部圈层的划分依据是通过打深井而获得的信息 B.地幔是指莫霍
- “基因型身份证”主要是利用现在国内外最先进的DNA指纹技术,选取若干个固定的遗传基因位点进行鉴定。2002年9月郑州市民
- 设直线与圆C1:交于A,B两点,若圆C2的圆心在线段AB上,且圆C2与圆C1相切,切点在圆C1的劣弧上,则圆C2的半径的
- It was in the garden of her old house _______ she grew up



