高考二轮复习知识点:吸热反应和放热反应1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
通过以下反应均可获取H2 . 下列有关说法正确的是( )
①太阳光催化分解水制氢:2H2O(l)═2H2(g)+O2(g)△H1=571.6kJ•mol﹣1 ②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=131.3kJ•mol﹣1 ③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=206.1kJ•mol﹣1 .
A . 反应①中电能转化为化学能
B . 反应②为放热反应
C . 反应③使用催化剂,△H3减小
D . 反应CH4(g)═C(s)+2 H2(g)的△H=74.8kJ•mol﹣1
|
|
| 2. 多选题 | 详细信息 |
|
下列说法错误的是( )
A . 物质发生化学反应的反应热仅指反应放出的热量
B . 热化学方程式中各物质的化学计量数不只表示物质的量,还表示分子的个数
C . 所有的燃烧反应都是放热的
D . 热化学方程式中,化学式前面的化学计量数可以是分数
|
|
| 3. 计算题 | 详细信息 |
 溶液与 溶液与  锌粉在量热计中充分反应。测得反应前温度为 锌粉在量热计中充分反应。测得反应前温度为  ,反应后最高温度为 ,反应后最高温度为  。 。 已知:反应前后,溶液的比热容均近似为
|
|
| 4. 多选题 | 详细信息 | |||||||||||||||
|
根据下列实验操作和现象所得结论正确的是( )
A . A
B . B
C . C
D . D
|
||||||||||||||||
| 5. 多选题 | 详细信息 |
|
俗语说“雷雨发庄稼”与N2和O2反应生成NO有关。反应过程中不使用催化剂(曲线I)和使用催化剂(曲线II)的能量变化如图所示(图中E1表示破坏旧化学键吸收的能量,E2表示形成新化学键释放的能量)。下列叙述错误的是( )
A . 上述反应属于吸热反应
B . 途径I的反应焓变比途径II大
C . 过程I的反应速率比过程II慢
D . N2与O2反应的热化学方程式为:N2(g)+O2(g)=2NO(g) ΔH=(E1-E2)kJ•mol‑1
|
|
| 6. 综合题 | 详细信息 |
|
甲烷水汽重整反应(SMR)是我国主要的制氢技术,可以转变我国能源结构,助力我国实现“碳达峰”的目标。SMR反应常伴随水煤气变换反应(WGS):
SMR:CH4(g)+H2O(g) WGS:CO(g)+H2O(g) 回答下列问题:
|
|
| 7. 综合题 | 详细信息 | |||||||||||||||||
|
工业上由N2、H2合成NH3。制备H2需经多步完成,其中“水煤气(CO、H2)变换”是纯化H2的关键一步。
|
||||||||||||||||||
| 8. 综合题 | 详细信息 |
|
科学家利用Li4SiO4吸附CO2 , 对于实现废气资源的再利用及碳循环经济技术的发展都具有重要意义。回答下列问题:
|
|
| 9. 多选题 | 详细信息 | ||||||||
|
下列图示与对应的叙述相符的是( )
A . A
B . B
C . C
D . D
|
|||||||||
| 10. 综合题 | 详细信息 |
|
随着我国碳达峰、碳中和目标的确定,含碳化合物的综合利用备受关注。回答下列问题:
|
|
- 安徽省黄山市2020-2021学年高一上学期期末考试化学试题
- 安徽省江淮名校宣城2020-2021学年高一上学期期末考试化学试题
- 广西百色市2020-2021学年高二上学期期末教学质量调研测试化学试题
- 广西贵港市2020-2021学年高二上学期期末教学质量监测化学试题
- 广西桂林市2020-2021学年高二上学期期末质量检测化学试题
- 广西河池市2020-2021学年高二上学期期末教学质量检测化学试题
- 广西来宾市2020-2021学年高二上学期期末教学质量检测化学试题
- 广西南宁市2020-2021学年高二上学期期末考试化学试题
- 广西钦州市2020-2021学年高二上学期期末教学质量监测化学试题
- 陕西省宝鸡市渭滨区2020-2021学年高二上学期期末考试化学试题
- 陕西省汉中市2020-2021学年高二上学期期末考试化学试题
- 广西北海市2020-2021学年高一上学期期末教学质量检测化学试题
- 我国海尔电冰箱生产厂,经过十几年的发展,从产品单一的电冰箱增加了空调、洗衣机、热水器、电视机等,成为一个企业集团。该企业
- 已知向量=(1,-3),=(2,-1),=(m+1,m-2),若点A、B、C能构成三角形,则实数m应满足的条件是() A
- 如下图,直径为1个单位长度的圆从原点沿数轴向右滚动一周(不滑动),圆上的一点由原点到达点O′,点O′的坐标是
- 在一定体积的密闭容器中进行如下反应:CO2(g)+H2(g)CO(g)+H2O(g);其化学平衡常数K和温度t的关系如下
- 下图反映了近几年中国第二、三产业在GDP增长中贡献率的变化状况。照此趋势,下列推测正确的是①中国制造业成本不断攀升,国际
- 某宾馆安排A、 B、 C、 D、 E 五人入住3个房间, 每个房间至少住1 人, 且A、 B 不能住同一房间, 则不同的
- 下列各句翻译不正确的一项是( ) A.既又与汝就食江南,零丁孤苦,未尝一日相离也——随后又和你到江南谋生,孤苦零丁,
- 化学反应前后,肯定没有变化的是A.原子数目B.分子数目C.元素种类D.物质种类
- 阅读下面的作品,完成后面题目。 请记住那些曾仰望星空的人 于建嵘 近日,有名校毕业的年轻法学博士来访,陪其参观宋庄美术馆
- 如图所示,长为L=75cm的平底玻璃管,底部放置一可视为质点的小球,现让玻璃管从静止开始以a1=16m/s2的加速度竖直
- 我国古代有很多德才兼备的人,他们通常被称为被称为“圣人”。被后人尊称为“书圣”的是 A.王羲之 B.苏
- 下列动物的行为对人类有利的是() A.苍蝇舔食垃圾 B.蝗虫吃农作物 C.蚊子吸血 D.青蛙捕食农田里的昆虫
- 下列各组词语中,有错别字的一组是( )A、沧海桑田 苍翠欲滴 层见叠出 花样迭出 B、傲慢无礼 无
- (本小题满分12分) 已知椭圆的左、右焦点分别为,离心率,且长半轴的平方等于焦距. (Ⅰ)求椭圆的标准方程; (Ⅱ)过焦
- 如图为一匀强电场,某带电粒子从A点运动到B点,在这一运动过程中克服重力做的功为3.0J,电场力做的功为2.0J。则下列说
- 推进依法治国,必须坚持法律面前人人平等这一原则。下列古语蕴含这一思想的是( ) ①法不阿贵,绳不绕曲
- 设二次函数的导数为,,对于任意的实数恒有,则的最小值是 A. B.
- 依次填入下列横线处的句子,与上下文衔接最恰当的一组是( ) 一眼看见那幅大地的水墨画,我还真有些忘情: 。 ①黝黑
- 假定你是李华,是2014年佛罗里达冬令营的组织者,请你给Joe回一封电子邮件,介绍冬令营的相关情况。 内容主要包括: 1
- 下图是“某地区1950~1980年人口增长图”,30年间该地区A.乡村人口增长了2000万人
 、溶液的密度均近似为
、溶液的密度均近似为  ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算: J。
J。
 的
的 
 (列式计算)。
(列式计算)。

 CO(g)+3H2(g) ΔH1=a kJ·mol-1 K1=1.198×
CO(g)+3H2(g) ΔH1=a kJ·mol-1 K1=1.198× 


 。随水蒸气分压
。随水蒸气分压  的变化如下图1,
的变化如下图1, 

 =3,CH4、H2O、O2反应的化学方程式是。
=3,CH4、H2O、O2反应的化学方程式是。





 和
和 的综合利用对温室气体减排具有重要意义。已知反应体系中主要涉及如下反应:
的综合利用对温室气体减排具有重要意义。已知反应体系中主要涉及如下反应:
 ;
;
 。
。





 ℃之后,温度升高积碳量减小的主要原因为。
℃之后,温度升高积碳量减小的主要原因为。

 。
。 kPa,容器内各气体分压与时间的关系如图所示。
kPa,容器内各气体分压与时间的关系如图所示。
 kPa2;若8min时改变的条件是缩小容器容积,该时刻将容器容积缩小到L,其中
kPa2;若8min时改变的条件是缩小容器容积,该时刻将容器容积缩小到L,其中 分压与时间关系可用图中曲线(填“
分压与时间关系可用图中曲线(填“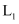 ”、“
”、“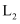 ”、“
”、“ ”或“
”或“ ”)表示。
”)表示。


