高考二轮复习知识点:盐类水解的原理1
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 多选题 | 详细信息 |
|
生产碳酸饮料时常加入防腐剂NaA,再加压充入CO2。已知室温下,HA的Ka=6.3×10-5 , H2CO3的Ka1=4.2×10-7 , Ka2=4.9×10-11 , 下列说法正确的是( )
A . 充入CO2能使溶液中c(A-)增大
B . 当c(H+)= 6.3×10-5 , 饮料中
 =1
C . 充入CO2时发生反应;CO2+H2O+A-=HA+HCO3-
D . 该饮料中粒子浓度关系为:c(HA)+c(H+)=c(OH-)+c(HCO3-)+2(CO32- ) =1
C . 充入CO2时发生反应;CO2+H2O+A-=HA+HCO3-
D . 该饮料中粒子浓度关系为:c(HA)+c(H+)=c(OH-)+c(HCO3-)+2(CO32- )
|
|
| 2. 综合题 | 详细信息 |
|
工业烟气可用氯酸氧化法脱硫,涉及反应:_______
 _______ _______  _______ _______  =_______ =_______  (未配平)。完成下列填空: (未配平)。完成下列填空:
|
|
| 3. 推断题 | 详细信息 |
|
短周期元素X、Y、Z、W、N的原子序数依次增大,其中X的一种同位素原子没有中子,Y的一种核素可做考古学家测定文物的年代,Z为地壳中含量最多的非金属元素,W的焰色反应为黄色,N原子为所在周期原子半径最小的原子(稀有气体除外)
|
|
| 4. 综合题 | 详细信息 | ||||||||
|
硫及其化合物在生产生活中有广泛的应用。请回答:
|
|||||||||
| 5. 综合题 | 详细信息 | ||||||||||||||||
|
废弃锌锰干电池中锰粉的主要成分是
 、MnO(OH)、炭粉、 、MnO(OH)、炭粉、  、 、  和 和  等,某兴趣小组利用锰粉制备 等,某兴趣小组利用锰粉制备  晶体并回收 晶体并回收  和 和  。流程如下: 。流程如下: 相关物质溶解度数据如下:
请回答:
|
|||||||||||||||||
| 6. 实验探究题 | 详细信息 | ||||||||||||||||||
|
某小组同学根据
 、 、  和 和  的氧化性推断溶液中 的氧化性推断溶液中  与 与  可能先后发生两个反应: 可能先后发生两个反应:  , ,  ,进行如下实验。 ,进行如下实验。
|
|||||||||||||||||||
| 7. 综合题 | 详细信息 |
|
钛白粉学名二氧化钛(TiO2)是性能最佳、应用最广、用量最大的白色颜料。钛铁矿(FeTiO3)中往往含有Fe2O3、MgO、CaO、Al2O3、SiO2等杂质。一种硫酸法钛白粉生产工艺如图:
②H2TiO3不溶于水和稀酸。
|
|
| 8. 多选题 | 详细信息 |
|
常温下,向
 溶液中逐滴加入0.2 溶液中逐滴加入0.2  溶液10.0 溶液10.0  ,溶液中微粒的物质的量(挥发的 ,溶液中微粒的物质的量(挥发的  未画出)随 未画出)随  的变化如下图所示。下列说法正确的是( ) 的变化如下图所示。下列说法正确的是( )
A . 随着盐酸的加入,溶液中水的电离程度先减小后增大
B .
 的水解常数 的水解常数  的数量级约为 的数量级约为  C . a点对应溶液中离子浓度:
C . a点对应溶液中离子浓度:  D . b点对应溶液中:
D . b点对应溶液中: 
|
|
| 9. 综合题 | 详细信息 | ||||||||||||||||||
|
工业上利用钴渣[主要成分为Co2O3、Co(OH)3 , 含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制备钴氧化物的工艺流程如下。
已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表。
|
|||||||||||||||||||
| 10. 多选题 | 详细信息 |
|
下列关于盐类水解的说法错误的是( )
A . 在纯水中加入能水解的盐一定促进水的电离
B . 加热
 溶液,溶液中 溶液,溶液中
 的值将减小
C . 同温时,等浓度的 的值将减小
C . 同温时,等浓度的  和 和  溶液, 溶液,  溶液的pH大
D . 在 溶液的pH大
D . 在
 溶液中加入稀 溶液中加入稀
 能抑制 能抑制
 水解 水解
|
|
- 山东省惠民县第二中学致远部2020-2021学年高二上学期化学10月月考试卷
- 2021年高考化学真题试卷(天津卷)
- 安徽省淮南市2021年高考化学二模试卷(4月)
- 湖南省百校联考(衡阳市二模)2022届髙三化学试题
- 广东省潮州市湘桥区2021-2022学年高二下学5月月考化学试题
- 四川省巴中市2020-2021学年高一下学期期末学情检测化学试题
- 四川省凉山州2021-2022学年高三上学期第一次诊断测试化学试题
- 陕西省汉中市2020~2021学年下学期期末校级联考高一化学试题
- 陕西省宝鸡市金台区2020-2021学年高二上学期化学期中考试试卷(文)
- 广东省乐昌第二高中2020-2021学年高一上学期化学期中考试试卷
- 江西省赣抚吉名校2021-2022学年高三上学期化学开学考试试卷
- 浙江省丽水市2020-2021学年高二下学期普通高中教学质量监控化学试题
- 下列有关pH或c(H+)变化的判断中,正确的是A.温度的升高,纯水的pH不变 B.加水稀释,碳
- I was busy yesterday, otherwise I ___ your birthday party. A
- 已知函数,若, ,则 .
- Duchenne muscular dystrophy(杜氏肌营养不良,DMD)是一种罕见的X染色体连锁的隐性遗传病,患
- (05年北京春季卷)(5分)原始的电话机将听筒和话筒串联成一个电路,当自己对着话筒讲话时,会从话筒中听到自己的声音,导致
- 民国时期,在社交礼仪上逐渐用西方的握手、鞠躬取代跪拜礼,称呼上用“先生”“同志”取代“老爷”“大人”,这一变化在本质上体
- 右边漫画《难博芳心》给我们的启示是( ) A.在市场经济条件下,诚信与欺诈是不可分离的 B.诚实信
- 在某温度下,NaOH的溶解度为20克,该温度下将40克NaOH放入110克水中,充分搅拌后,测的溶液的密度为1.2g/m
- 下列实验操作正确且能达到预期目的的是 实验目的 操 作 A 欲证明CH2=CHCHO中含有碳碳双键 滴入KMn
- 已知直线 y=ax(a≠0)与反比例函数 y=(k≠0)的图象一个交点 坐标为(2,4),则它们另一个交点的坐标是
- ______the boy is only five years old, he knows more about s
- 如图所示的电动机是一种使用广泛的动力机械,从能量转化的角度看.它主要是把电能转化为机械能,还有一部分能量在线圈中以热量的
- 现有一本故事书,姐妹俩商定通过摸球游戏定输赢(赢的一方先看),游戏规则是:用4个完全相同的小球,分别表上1、2、3、4后
- 在四边形ABCD中,AD∥BC,∠ABC=90°,AB=BC,E为AB边上一点,∠BCE=15°,且AE=AD.连接D
- 句中加点的词语使用正确的是 A.美国对恢复中国关贸总协定缔约国地位问题上故意设置重重障碍,激起了世界有正义感国家的强烈不
- 2.下列各句,没有语病、句意明确的一项是() A.现在全国各大医院的医疗水平、就医环境与以往相比均有提高,但药价始终居高
- 选词填空。 沉浸沉醉沉寂 (1)夜莺的歌声()了,长脚秧鸡不再欢嚷。 (2)()于盛夏的豪华,它从未感到/自己的喜悦消逝
- 如图所示是光的双缝干涉的示意图,下列说法中正确的是 ( ) A.单缝S的作用是为了增加光的强度.B.双缝S1、S
- 已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是( )
- 中新网2009年12月16日电 中国社科院工业经济研究所原所长吕政在第六期“经济每月谈”上表示,中国国民收入初次分配不
 也可用
也可用  和
和  的混合液脱除。
的混合液脱除。  溶液呈碱性的原因是(用离子方程式表示)。
溶液呈碱性的原因是(用离子方程式表示)。
 通入紫色石蕊试液,先变红后褪色
通入紫色石蕊试液,先变红后褪色 的降水,主要是由污染物
的降水,主要是由污染物  造成
造成
 、
、  、
、  为各步的平衡常数,且
为各步的平衡常数,且  (
(  表示
表示  ,则溶液
,则溶液 
 。
。 时,溶液中
时,溶液中  。如果溶液中
。如果溶液中 
 ,需加NaOH将溶液pH调整为约等于。
,需加NaOH将溶液pH调整为约等于。 。但高温时CO会与
。但高温时CO会与 

 时,反应25min,体系中
时,反应25min,体系中  的比值随温度变化如表所示:
的比值随温度变化如表所示:
 ,
,  。能提高
。能提高  ,将
,将  氧化为
氧化为 
 已知:
已知: 

 溶液呈绿色,
溶液呈绿色, 





 量不宜过少或过多 , 理由是。
量不宜过少或过多 , 理由是。 溶液、过量锌粉
溶液、过量锌粉 的
的  溶液、过量锌粉
溶液、过量锌粉 溶液,生成,证明有
溶液,生成,证明有  溶液和
溶液和  溶液替代实验Ⅱ中的
溶液替代实验Ⅱ中的  溶液:
溶液:
 溶液、过量锌粉
溶液、过量锌粉 溶液、过量锌粉
溶液、过量锌粉 ,
,  在溶液中呈棕色。
在溶液中呈棕色。 已知:①酸解后,钛主要以TiOSO4形式存在。强电解质TiOSO4在溶液中仅能电离出SO
已知:①酸解后,钛主要以TiOSO4形式存在。强电解质TiOSO4在溶液中仅能电离出SO  和一种阳离子。
和一种阳离子。



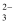 三种离子的还原性由强到弱的顺序是。氧化过程中加NaClO3被还原,产物中的氯元素处在最低价态,反应的离子方程式为。
三种离子的还原性由强到弱的顺序是。氧化过程中加NaClO3被还原,产物中的氯元素处在最低价态,反应的离子方程式为。
 =(保留两位有效数字)。
=(保留两位有效数字)。



