高考二轮复习知识点:盐类水解的原理3
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
I.2Al+Fe2O3
 Al2O3+2Fe在化学反应过程中产生超高热,曾用于钢轨焊接。完成下列填空: Al2O3+2Fe在化学反应过程中产生超高热,曾用于钢轨焊接。完成下列填空:
|
|
| 2. 实验探究题 | 详细信息 | |||||||||||||||||||||||||
|
为研究铁盐与亚硫酸盐之间的反应,某研究小组利用孔穴板进行了实验探究:
小组记录的实验现象如下表所示:
|
||||||||||||||||||||||||||
| 3. 综合题 | 详细信息 |
|
|
| 4. 单选题 | 详细信息 |
|
LiH2PO4是制备电池的重要原料。室温下,LiH2PO4溶液的pH随c初始(H2PO4–)的变化如图1所示,H3PO4溶液中H2PO4–的分布分数δ随pH的变化如图2所示,[
 ]下列有关LiH2PO4溶液的叙述正确的是( ) ]下列有关LiH2PO4溶液的叙述正确的是( )  
A . 溶液中存在3个平衡
B . 含P元素的粒子有H2PO4–、HPO42–、PO43–
C . 随c初始(H2PO4–)增大,溶液的pH明显变小
D . 用浓度大于1 mol·L-1的H3PO4溶液溶解Li2CO3 , 当pH达到4.66时,H3PO4几乎全部转化为LiH2PO4
|
|
| 5. 实验探究题 | 详细信息 |
|
焦亚硫酸钠(Na2S2O5)为白色或黄色结晶粉末或小结晶,其性质活泼,具有强还原性,是常用的食品抗氧化剂之一。制备该物质的反应方程式为: Na2SO3+SO2= Na2S2O5 , 某研究小组利用该反应在实验室制备焦亚硫酸钠并探究其有关性质。请回答下列问题:
|
|
| 6. 综合题 | 详细信息 |
|
钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O; ②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
|
|
| 7. 综合题 | 详细信息 |
|
人类对锡(50Sn)的使用有悠久的历史,可以追溯到大约公元前3000年,但这也是对锡的“异常”不断加深认识,不断“驯服”它的历史。
|
|
| 8. 综合题 | 详细信息 |
|
生活污水中氮是造成水体富营养化的主要原因。
完成下列填空:
|
|
| 9. 单选题 | 详细信息 |
|
HA是一元弱酸,难溶盐MA的饱和溶液中
 而变化, 而变化,  不发生水解。实验发现,298K时 不发生水解。实验发现,298K时  ,如下图中实线所示。 ,如下图中实线所示。 下列叙述错误的是( )
A . 溶液pH = 4 时.
 B . MA 的溶度积
B . MA 的溶度积  C . 溶液 pH = 7 时,
C . 溶液 pH = 7 时,  D . HA 的电离常数
D . HA 的电离常数 
|
|
| 10. 单选题 | 详细信息 |
|
鸟嘌呤(
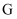 )是一种有机弱碱,可与盐酸反应生成盐酸盐(用 )是一种有机弱碱,可与盐酸反应生成盐酸盐(用  表示)。已知 表示)。已知  水溶液呈酸性,下列叙述正确的是( ) 水溶液呈酸性,下列叙述正确的是( )
A .
 水溶液的 水溶液的  B .
B .  水溶液加水稀释, 水溶液加水稀释,  升高
C . 升高
C .  在水中的电离方程式为: 在水中的电离方程式为:  D .
D .  水溶液中: 水溶液中: 
|
|
- 2020高考化学常考知识点专练 07:化学平衡
- 广东省汕头市潮南区2016-2017学年高一上学期化学期末考试试卷
- 人教版化学高二选修4第二章第二节影响化学反应速率的因素同步练习
- 湖南省怀化市2019-2020学年高一下学期化学期末考试试卷
- 2017年高考理综真题试卷(化学部分)(新课标Ⅲ卷)
- 2015-2016学年海南省国科园实验学校高二下学期期末化学试卷
- 浙江省台州市五校2019-2020学年高三上学期化学10月月考试卷
- 湖北省宜昌市2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年福建省八县一中高三上学期期中化学试卷
- 浙江省温州市新力量联盟2018-2019学年高二下学期化学期末考试试卷
- 宁夏吴忠市吴忠中学2018-2019学年高一上学期期末化学模拟试卷
- 浙江省2018年11月普通高校招生选考化学真题试卷
- ......
- 用配方法解方程x2﹣2x﹣2=0,下列配方正确的是() A.(x
- 1958年10月,山东范县县委书记作报告:“人人进入新乐园,吃穿喝用不要钱,……人人都说天堂好,天堂不如新乐园!”这一现
- 阅读下面的文言文,完成后面题目。 赵概,字叔平,南京虞城人。少笃学自力,器识宏远。中进士第,为集贤校理、开封府推官。奏事
- 常温下把铁片分别加入到下列溶液中,铁片能溶解,且溶液质量减轻的是( )。A.稀硫酸 B.浓硫酸
- 2009年7月5日,以热比娅为首的境外“疆独”组织“世界维吾尔代表大会”指挥策划了乌鲁木齐暴力事件,企图破坏国家统一和民
- 已知函数y=cos(ωx+φ)(ω>0,|φ|<)的部分图象如图所示,则() (A)ω=1,φ=(B)ω=1,φ=-(C
- 在复习《反比例函数》一课时,同桌的小明和小芳有一个问题观点不一致.小明认为如果两次分别从1~6六个整数中任取一个数,第一
- 下列疾病中,由病毒引起的是 A. 白化病 B. 炭疽病 C. 结核病
- 李冰主持修筑闻名世界的防洪灌溉工程是( ) A.灵渠 B.长城 C.郝江
- 下列关于分子和原子的叙述正确的是() A.分子是保持物质性质的最小微粒 B.分子大、原子小 C.物质都是由分子构成的 D
- 在探究超重和失重规律时,某体重为G的同学站在一压力传感器上完成一次下蹲动作。传感器和计算机相连,经计算机处理后得到压力F
- 心脏结构属于一心房、一心室的动物是 A 鱼类 B 两栖类 C 爬行类
- 地球同步卫星离地心的距离为r,运动速度为v1,加速度为a1;地球赤道上的物体随地球自转的向心加速度为a2;第一宇宙速度为
- (07年陕西卷) 如图,平面内有三个向量、、,其中与的夹角为120°,与的夹角为30°,且==1,=.若=的值为
- 已知a为实数,且函数f(x)=(x2-4)(x-a) (1)求导函数f′(x); (2)若f′(-1)=0,求函数f(x
- 静止在光滑水平面上的物体,同时受到在同一直线上的力F1、F2作用,F1、F2随时间变化的图象如图所示,图乙中的运动图像与
- 如图所示,风洞实验室中能模拟产生恒定向右的风力。质量的小球穿在长的直杆上并置于实验室中,球与杆间的动摩擦因数为0.5,当
- 如图表示细胞中部分生物膜之间结构和功能的联系,有关叙述正确的是() A.图中1是指细胞膜 B. 图中7是指内
- ---How beautifulLucy is! She looks smart _______ red.

 Ag+(aq)+Cl-(aq) Ksp=1.8×10-10
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10 。
。

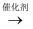 N2+2 O H-+4H2O
N2+2 O H-+4H2O 



