浙江省台州市五校2019-2020学年高三上学期化学10月月考试卷
浙江省台州市五校2019-2020学年高三上学期化学10月月考试卷
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高三上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
某温度下,反应SO2(g)+
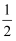 O2(g)⇌SO3(g) 的平衡常数K1=50,在同一温度下,反应SO3(g)⇌SO2(g)+ O2(g)⇌SO3(g) 的平衡常数K1=50,在同一温度下,反应SO3(g)⇌SO2(g)+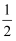 O2(g)的平衡常数K2的值为( ) O2(g)的平衡常数K2的值为( )
A . 2500
B . 100
C . 0.02
D . 0.001
|
|
| 2. 单选题 | 详细信息 |
|
对于可逆反应:2A(g)+B(g)
 2C(g) ΔH<0,下列各图正确的是( ) 2C(g) ΔH<0,下列各图正确的是( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 3. 单选题 | 详细信息 |
|
下列事实不能用勒夏特列原理解释的是( )
A . 氯水中有平衡:Cl2+H2O
 HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
B . 对CO(g)+NO2(g) HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
B . 对CO(g)+NO2(g)  CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C . 对2NO2(g) CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C . 对2NO2(g)  N2O4(g) △H<0, 升高温度平衡体系颜色变深
D . SO2催化氧化成SO3的反应,往往加入过量的空气 N2O4(g) △H<0, 升高温度平衡体系颜色变深
D . SO2催化氧化成SO3的反应,往往加入过量的空气
|
|
| 4. 单选题 | 详细信息 |
|
下列反应既属于氧化还原反应,又属于吸热反应的是( )
A . 铝片与稀盐酸的反应
B . Ba(OH)2·8H2O与NH4Cl的反应
C . 灼热的碳与CO2的反应
D . 甲烷在氧气中的燃烧反应
|
|
| 5. 单选题 | 详细信息 |
|
4P(红磷,s)⇌P4(白磷,s) ΔH=+17 kJ·mol-1 , 根据以上热化学方程式,下列推论正确的是( )
A . 当1 mol白磷完全转变成红磷时放出17 kJ热量
B . 正反应是一个放热反应
C . 当4 g红磷转变成白磷时吸收17 kJ热量
D . 白磷比红磷稳定
|
|
| 6. 单选题 | 详细信息 |
|
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。向1L 0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应ΔH1、ΔH2、ΔH3的关系正确的是( )
A . ΔH1>ΔH2>ΔH3
B . ΔH1<ΔH3<ΔH2
C . ΔH1<ΔH2<ΔH3
D . ΔH1>ΔH3>ΔH2
|
|
| 7. 单选题 | 详细信息 |
|
25℃、101kPa时,1g甲醇完全燃烧生成CO2和液态H2O,同时放出22.68kJ热量。下列表示该反应的热化学方程式中正确的是( )
A . CH3OH(l)+3/2O2(g) = CO2(g) +2H2O(l) △H=-725.8 kJ·mol-1
B . 2 CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(l) △H=+1451.6kJ·mol-1
C . 2 CH3OH+O2= 2CO2+4H2O △H=-22.68 kJ·mol-1
D . CH3OH(l)+3/2O2(g) = CO2(g)+2H2O(g) △H=-725.8 kJ·mol-1
|
|
| 8. 单选题 | 详细信息 |
|
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中错误的是( )
A . 该能量转化系统中的水也是可以循环的
B . 燃料电池放电时的负极电极反应式:2H2+4OH--4e-=4H2O
C . 燃料电池放电时的正极电极反应式:2H2O+O2+4e-=4OH-
D . 燃料电池系统产生的能量实际上来自于水
|
|
| 9. 单选题 | 详细信息 |
|
2010年上海世博会,上海将有千辆氢燃料电池车上路,参看某种氢燃料电池原理图,下列说法错误的是( )
A . 氢氧燃料电池是一种具有应用前景的绿色电源
B . 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
C . 氢燃料电池能量转换率比氢气直接燃烧高
D . 氢燃料电池工作时,发出淡蓝色火焰
|
|
| 10. 单选题 | 详细信息 |
|
下列叙述正确的是( )
A . 升高温度可降低活化能
B . 废电池需回收,主要是要利用电池外壳的金属材料
C . 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
D . 推广使用太阳能、风能、地热能、氢能,有利于缓解温室效应
|
|
高中化学 试卷推荐
- 北京市大兴区2021-2022学年高二上学期期中考试化学试题
- 福建省福州市八县(市)协作校2021-2022学年高二上学期期中联考化学试题
- 福建省三明市教研联盟校2021-2022学年高二上学期期中联考化学试题
- 江苏省常熟市2021-2022学年高二上学期期中考试化学试题
- 江苏省淮安市高中校协作体2021-2022学年高二上学期期中考试化学(选修)试题
- 江苏省宿迁市沭阳县2021-2022学年高二上学期期中调研测试化学试题
- 江苏省徐州市2021-2022学年高二上学期期中考试化学试题
- 辽宁省六校2021-2022学年高二上学期期中考试化学试题
- 山西省怀仁市2021-2022学年高二上学期期中化学试题
- 山西省太原市2021-2022学年高二上学期期中考试化学试题
- 福建省福州市福清市高中联合体2021-2022学年高一上学期期中考试化学试题
- 江苏省常熟市2021-2022学年高一上学期期中化学试题
最近更新
- 下列关于燃烧和灭火的说法,不正确的是A .将木柴架空燃烧,目的是增大可燃物与氧气的接触面积,促进燃烧B .扑灭电器、图书
- 现有白纸,溶质质量分数分别为:A、10%的NaOH溶液;B、5%的硫酸溶液;C、5%的紫色石蕊试液。试设计出《“雨”落叶
- 一个正比例函数与一个反比例函数图象交于点P(2,6),则这个正比例函数的关系式是 ,这个反比例函数的
- (8分)中学常见的某反应的化学方程式为A+B→C+D+H2O(未配平,反应条件略去)。请回答下列有关问题:(1)若A是铁
- 哺乳动物的生殖方式是胎生,对动物的意义是( )。 A. 降低出生个体的数目 B. 提高后代的成活率
- 设a=20.3,b=log21.5,c=ln0.7,则() A.a>b>c B.a>c>b C.b>a>c
- 若不等式(m-2)x>2的解集是x<,则m的取值范围是____________
- 读环境、资源和人口关系示意图,完成第1-2题。1.图中字母代表的含义不正确的是( ) A.a表示资源开发
- 函数在一个周期内的图象如图,此函数的解析式为( ) A. B. C. D.
- 见渔人,乃大惊,问所从来,具答之。便要还家,设酒杀鸡作食。村中闻有此人,咸来问讯。自云先世避秦时乱,率妻子邑人来此绝境,
- Theroom is too small for us____. A. to livein B.livin
- (03年全国卷文)等差数列中,已知为( ) (A)48 (B)49 (C)50
- — Lucy, how about going to the ? — Sounds great! Readi
- 下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿
- Generally speaking, there are three differentlearning types:
- We are used to____ after supper, but weused to ____TV in the
- 阅读文言文,回答下列各题。(共11分)(甲)嗟夫!予尝求古仁人之心,或异二者之为,何哉?不以物喜,不以己悲;居庙堂之高则
- 如图是一台投影仪的示意图,其中A是____________,它的作用是改变光的传播方向;B是____________,它
- 一个质量为0.2kg的小球从空中静止下落,与水平地面相碰后弹到空中某一高度,其速度随时间变化的关系如图所示,假设小球在空
- 我国始终致力于维护朝鲜半岛和平稳定、实现半岛无核化、通过对话协商解决问题,最终实现半岛长治久安。长期以来,我国为推动政治





