高考化学真题重组卷 7+4专题冲刺 专题14 化学键与晶体结构
高考化学真题重组卷 7+4专题冲刺 专题14 化学键与晶体结构
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列各组物质的晶体类型相同的是( )
A . SiO2和SO3
B . I2和NaCl
C . Cu和Ag
D . SiC和MgO
|
|
| 2. 单选题 | 详细信息 |
|
下列化学用语表达正确的是( )
A . F-的离子结构示意图:
 C . 丙炔的键线式:
C . 丙炔的键线式: 
|
|
| 3. 单选题 | 详细信息 |
|
下列有关N、P及其化合物的说法错误的是( )
A . N的电负性比P的大,可推断NCl3分子的极性比PCl3的大
B . N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C . NH3的成键电子对间排斥力较大,可推断NH3的键角比PH3的大
D . HNO3的分子间作用力较小,可推断HNO3的熔点比H3PO4的低
|
|
| 4. 单选题 | 详细信息 |
|
某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞结构图,图b表示晶胞的一部分。下列说法正确的是( )
A . 该晶胞的体积为a3×10-36cm-3
B . K和Sb原子数之比为3∶1
C . 与Sb最邻近的K原子数为4
D . K和Sb之间的最短距离为
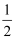 apm apm
|
|
| 5. 单选题 | 详细信息 |
|
甲烷单加氧酶(s—mmo)含有双核铁活性中心,是O2氧化CH4生成CH3OH的催化剂,反应过程如图所示。下列叙述错误的是( )
A . 基态Fe原子的核外电子排布式为[Ar]3d64s2
B . 步骤③有非极性键的断裂和极性键的形成
C . 每一步骤都存在铁和氧元素之间的电子转移
D . 图中的总过程可表示为:CH4+O2+2H++2e-
 CH3OH+H2O CH3OH+H2O
|
|
| 6. 综合题 | 详细信息 |
|
硒(
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(  )效应以来, )效应以来,  在发光材料、生物医学等领域引起广泛关注。一种含 在发光材料、生物医学等领域引起广泛关注。一种含  的新型 的新型  分子 分子  的合成路线如下: 的合成路线如下:
|
|
| 7. 实验探究题 | 详细信息 |
|
[选修3:物质结构与性质]
铁和硒(
|
|
| 8. 单选题 | 详细信息 |
 、 、 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在 属于第三代半导体材料,二者成键结构与金刚石相似,晶体中只存在 键、 键、 键。下列说法错误的是( ) 键。下列说法错误的是( )
A .
 的熔点高于 的熔点高于 B . 晶体中所有化学键均为极性键
C . 晶体中所有原子均采取
B . 晶体中所有化学键均为极性键
C . 晶体中所有原子均采取 杂化
D . 晶体中所有原子的配位数均相同 杂化
D . 晶体中所有原子的配位数均相同
|
|
| 9. 综合题 | 详细信息 |
|
研究笼形包合物结构和性质具有重要意义。化学式为
 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为 的笼形包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为 。回答下列问题: 。回答下列问题:
|
|
| 10. 单选题 | 详细信息 |
|
理论化学模拟得到一种
 离子,结构如图。下列关于该离子的说法错误的是( ) 离子,结构如图。下列关于该离子的说法错误的是( )
A . 所有原子均满足8电子结构
B . N原子的杂化方式有2种
C . 空间结构为四面体形
D . 常温下不稳定
|
|
高中化学 试卷推荐
- 湖南省怀化市2019-2020学年高一下学期化学期末考试试卷
- 2017年高考理综真题试卷(化学部分)(新课标Ⅲ卷)
- 2015-2016学年海南省国科园实验学校高二下学期期末化学试卷
- 浙江省台州市五校2019-2020学年高三上学期化学10月月考试卷
- 湖北省宜昌市2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年福建省八县一中高三上学期期中化学试卷
- 浙江省温州市新力量联盟2018-2019学年高二下学期化学期末考试试卷
- 宁夏吴忠市吴忠中学2018-2019学年高一上学期期末化学模拟试卷
- 浙江省2018年11月普通高校招生选考化学真题试卷
- 2020高考化学常考知识点专练 03:物质的量及相关计算
- 备考2018年高考化学一轮基础复习:专题17 化学反应中的热效应
- 2015-2016学年广东省汕头市高一下学期期末化学试卷
最近更新
- 北京晚报2010年7月26日报道,卫生部公布了《食用盐碘含量》的征求意见稿,面向 社会征求意见。对于食用盐中碘含量平均水
- On hearing the interesting story, they __________. A. burst
- __________him not to do so, hewouldn’t have made such a ser
- 阅读下列材料,结合所学知识回答问题。 为进一步净化网络环境, 国家9部委从2009年12月到2010年5月底,在全国范围
- 如图为“探究弹簧弹力与弹簧伸长量关系” 的实验装置图,弹簧的上端固定在铁架台上,下端装有指针及挂钩,指针恰好指向一把竖直
- Many a student ____ going to have themselves ______ in the h
- 小球以速度v水平抛出,小球只受到_________,所以小球在水平方向加速度为_________,水平方向分速度vx保持
- 20世纪中期,美国财政部长福勒得意地宣称:“各个行星围绕着太阳转,各国货币围绕着美元转。”这句话反映的实质问题是 A 美
- 临沂市以“提升群众幸福指数”为宗旨,扎实有效、持续不断地开展了全国文明城市创建活动,得到了千万临沂人民的衷心拥护和积极参
- 中国变革,启动积极的财政政策。增发国债和长期建设债券用于基础设施建设和西部开发,( a )公务员工资和城镇居民三
- 细胞有丝分裂过程中,染色单体形成和分离分别发生在 ( ) A.间期和前期
- 某媒体为了调查未成年人的自我保护意识和能力,对20名中小学生进行调查,当问到“你父母的同事或你家的邻居突然到学校来接你,
- The doctor said it would take six weeks to recover and I ___
- 阅读材料回答问题: 材料一 “行仁政而王,莫之能御也。” “处无为之事,行不言之教。”
- 化简得( )A. B. C. D.
- 为研究氢氧化钙、氢氧化钠两种溶液的化学性质,进行如下实验。(1)A、D中酚酞均变红色,说明两种溶液都呈______性(填
- 经济学中有“刘易斯拐点”之说,意指劳动力从无限供给到短缺的临界点。简而言之,在“刘易斯拐点”之前,是人求工作,不涨工资也
- 具有不同原子团的一组物质是( ) A.FeSO4和Fe2 (SO4) 3 B.KMnO4和
- 如图所示,台秤的托盘上放一个装有水的平底烧杯,一个不吸水的木块用细线系在烧杯底浸没在水中,剪掉木块以后,木块上浮至静止,
- 与鲁尔区兴起时间不同,但布局方式相同的是: A.英国苏格兰中部工业区 B.日本太平洋沿岸工业区 C.意大利塔



 的沸点低于
的沸点低于  ,其原因是。
,其原因是。
 键
键 键为非极性共价键
键为非极性共价键 与
与 

 (填“>”或“<”)。
(填“>”或“<”)。
 )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。  的立体构型为。
的立体构型为。
 ,晶体密度为
,晶体密度为  ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 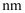 (列出计算式,
(列出计算式, 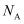 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 ;
; 分子
分子  离子(填“>”“<”或“=”),原因是。
离子(填“>”“<”或“=”),原因是。 是一种补铁剂。富马酸分子的结构模型如图所示:
是一种补铁剂。富马酸分子的结构模型如图所示:

 键与
键与  键的数目比为;
键的数目比为; ,将
,将  转化为
转化为  ,反应过程如图所示:
,反应过程如图所示:


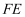 原子的配位数为;
原子的配位数为; 、
、  。阿伏加德罗常数的值为
。阿伏加德罗常数的值为  (列出计算式)。
(列出计算式)。
 原子的价电子排布式为,在元素周期表中位置为。
原子的价电子排布式为,在元素周期表中位置为。
 与
与 的配位数之比为;
的配位数之比为; ;晶胞中有d轨道参与杂化的金属离子是。
;晶胞中有d轨道参与杂化的金属离子是。
 )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的
)替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大
大 、
、 、
、 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是。




