高考二轮复习知识点:盐类水解的原理2
教材科目:化学
试卷分类:高考阶段
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 综合题 | 详细信息 |
|
SO2、Na2S2O3、Na2S、Na2SO3、Na2SO4等含硫化合物在工业上有广泛的用途。完成下列填空:
|
|
| 2. 综合题 | 详细信息 |
|
某化学兴趣小组进行了下列关于氯化铵的课外实验:
(实验操作) 浸过氯化钠溶液的布条很快烧光,浸过氯化铵溶液的布条不燃烧,冒出白烟。
|
|
| 3. 综合题 | 详细信息 |
|
Zn、Fe及其化合物在生产生活中应用比较广泛。工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量FeO和CuO等杂质)制取金属锌的工艺流程如下:
|
|
| 4. 综合题 | 详细信息 |
|
氯化亚铜(CuCl)是一种重要的化工产品。它不溶于H2SO4、HNO3 和醇,微溶于水,可溶于浓盐酸和氨水,在潮湿空气中易水解氧化成绿色的碱式氯化铜[Cu2(OH)4-nCln],n随着环境酸度的改变而改变。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如图:
|
|
| 5. 综合题 | 详细信息 | ||||||||||||
|
草酸(H2C2O4)是一种二元弱酸,广泛分布于动植物体中。
|
|||||||||||||
| 6. 综合题 | 详细信息 |
|
甲硅烷广泛用于电子工业、汽车领域,三氯氢硅(SiHCl3)是制备甲硅烷的重要原料。回答下列问题:
|
|
| 7. 实验探究题 | 详细信息 |
|
高铁酸钾(K2FeO4)是一种高效净水剂。已知:K2FeO4易溶于水,微溶于浓KOH溶液;在酸性或中性溶液中不稳定,在0~5℃的强碱性溶液中较稳定。某实验小组欲制备高铁酸钾并测定其纯度。
Ⅰ.制备高铁酸钾(夹持装置略)
|
|
| 8. 多选题 | 详细信息 |
|
室温下,用
 溶液滴定 溶液滴定  (二元弱酸)溶液的曲线如图所示(体积变化忽略不计)。下列说法错误的是( ) (二元弱酸)溶液的曲线如图所示(体积变化忽略不计)。下列说法错误的是( )
A . 点④所示溶液水的电离程度最大
B . 滴定过程中:
 一直保持不变
C . 点①所示溶液中: 一直保持不变
C . 点①所示溶液中:  D . 滴定过程中,存在以下关系:
D . 滴定过程中,存在以下关系: 
|
|
| 9. 综合题 | 详细信息 |
|
氯化亚铜(CuCl)是重要的化工原料,广泛用作有机合成催化剂。
资料 ①水溶液中存在平衡:2Cl-(aq)+CuCl(s) ②CuCl是难溶于水的白色固体,在热水中迅速水解生成Cu2O。 ③CuCl在潮湿的空气中易被氧化,生成的碱式盐为Cu2(OH)3Cl。 Ⅰ.实验室中用纯净的CuCl2固体可制备CuCl。取75gCuCl2固体于烧杯中,加入100mL0.2mol/L盐酸和水配成200mL溶液,然后在溶液中通入SO2气体。
|
|
| 10. 综合题 | 详细信息 |
|
在钢中加入一定量的钒,就能使钢的硬度、耐腐蚀性大增。工业上以富钒炉渣(主要成分为
 、 、  和 和  等)为原料提取五氧化二钒的工艺流程如下: 等)为原料提取五氧化二钒的工艺流程如下:
|
|
- 人教版化学高二选修5第四章第三节蛋白质和核酸同步练习
- 上海市崇明区2020年高考化学二模试卷
- 山西省太原市2020年高考化学二模试卷
- 2015-2016学年山东省泰安市高一下学期期末化学试卷
- 上海市松江区2017-2018学年高考理综-化学二模考试试卷
- 河南省平顶山市2017-2018学年高一下学期化学期末考试试卷
- 河北省承德市联校2017-2018学年高三上学期化学期末考试试卷
- 人教高中化学一轮复习:专题8
- 人教版化学高二选修1第三章第二节金属的腐蚀和防护同步练习
- 江苏省宿迁市沭阳县2016-2017学年高一上学期化学期中考试试卷
- 湖北省仙桃、天门、潜江2019-2020学年高二下学期化学期末考试试卷
- 2015-2016学年内蒙古包头市包钢四中高一下学期期中化学试卷
- _____,is there a restaurant in the neighborhood? A. Sorry
- 北宋王安石变法所要解决的核心问题是 ( ) A.加强北宋的军事力量
- 设,命题“若,则方程有实根”的逆否命题是() (A)若方程有实根,则 (B)若方程有实根,则 (C)若方程没有实根,则
- 蝗虫在生长过程中必须蜕皮的原因是( ) A.外骨骼不能随身体的生长而长大 B.外骨骼损坏,需形成新的外骨
- 听取和审议“一府两院”的工作报告,是每年人大会议上最为重要的议题,是人大对一府两院进行全面监督的基本形式。人大履行监督“
- 如图所示的区域中,左边为垂直纸面向里的匀强磁场,磁感应强度为 B ,右边是一个电场强度大小未知的匀强电场,其方向平行于O
- 集合A={a,b,c,d,e},集合B={m,n,f,h},则从集合A到集合B可以建立不同的映射个数为( )A.4
- 某校16岁中学生王某伙同他人撬开一教师宿舍,盗走价值3500元摩托车一辆。公安人员到王某居住地调查时,不开警车,不着警服
- 如图,已知四边形ABCD内接于圆O,连结BD,∠BAD=105°,∠DBC=75°. (1)求证:BD=CD; (2)若
- 下图是某种生物的精子细胞,根据图中染色体类型和数目,则来自同一个次级精母细胞的是( )A.①③ B.②⑤ C.①④
- 如图,小红在作线段AB的垂直平分线时,是这样操作的:分别以点A,B为圆心,大于线段AB长度一半的长为半径画弧,相交于点C
- 在R上定义运算:xy=x(1-y).若不等式(x-a)(x+a)<1对任意实数x恒成立,则() (A)-1<a<1
- 材料一 M县城镇和水系分布示意图材料二 M县处于我国亚热带季风气候区,境内最高海拔为1254米,最低海拔为24米,森
- (08年河西区质检三理)已知函数的图象上相邻的一个最高点与一个最低点恰好都在圆上,则的最小正周期为( )A. 4
- 与右图中阴影部分含义相符的一项是 A.太阳能 B.地热能 C.水能 D.潮汐能
- 下列操作不正确的是··························· ( ) A.未用完的药品应该倒入指定容器
- 完成下列反应的化学方程式,并在括号内注明反应的基本类型(指化合反应、分解反应、置换反应) ⑴铁丝在氧气中燃烧
- 读甲、乙两图.回答下面试题。甲河流域的植被遭到严重破坏,带来的后果是 ( ) A.水土流失,草场沙化
- Mr. Wilson invited some friends to lunch. She was eager to t
- 我国人口最多的省是( ) A.上海 B.广东 C.河南 D.四川






 SiH2Cl2(g)+SiCl4(g)为歧化制甲硅烷过程的关键步骤,此反应采用一定量的PAl00催化剂,在不同反应温度下测得SiHCl3的转化率随时间的变化关系如图所示。
SiH2Cl2(g)+SiCl4(g)为歧化制甲硅烷过程的关键步骤,此反应采用一定量的PAl00催化剂,在不同反应温度下测得SiHCl3的转化率随时间的变化关系如图所示。 


 CuCl
CuCl 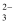 (aq)。
(aq)。


 ,该反应的化学方程式为。
,该反应的化学方程式为。
 代替NaCl与富钒炉渣焙烧制得偏钒酸钠。用
代替NaCl与富钒炉渣焙烧制得偏钒酸钠。用  ,为使钒元素的沉降率达到98%,要加入较多的
,为使钒元素的沉降率达到98%,要加入较多的  ,从平衡角度分析原因。
,从平衡角度分析原因。
 溶液。取20.00mL该溶液于锥形瓶中,用
溶液。取20.00mL该溶液于锥形瓶中,用  标准溶液进行滴定,经过三次滴定,达到滴定终点时平均消耗标准溶液的体积为20.00mL。
标准溶液进行滴定,经过三次滴定,达到滴定终点时平均消耗标准溶液的体积为20.00mL。  溶液为黄色,
溶液为黄色,  溶液为蓝色,而五氧化二钒则是红色的。
溶液为蓝色,而五氧化二钒则是红色的。 ,
, ;
;  。
。


