2020高考化学常考知识点专练 04:反应热
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
已知化学反应①C(s)+
 O2(g)=CO(g)△H=-Q1kJmol②2CO(g)+O2(g)=2CO2(g)△H=-Q2kJ/mol据此判断,下列说法正确的是(Q1、Q2均为正数,且其他条件相同)( ) O2(g)=CO(g)△H=-Q1kJmol②2CO(g)+O2(g)=2CO2(g)△H=-Q2kJ/mol据此判断,下列说法正确的是(Q1、Q2均为正数,且其他条件相同)( )
A . C的燃烧热为Q1kJ/mol
B . 2molCO(g)所具有的能量一定高于2molCO2(g)所具有的能量
C . 一定质量的C燃烧,生成CO2(g)比生成CO(g)时放出的热量多
D . C燃烧生成CO2气体的热化学方程式为:C(s)+O2(g)=CO2(g)△H=-(Q1+Q2)kJ/mol
|
|
| 2. 实验探究题 | 详细信息 |
|
“天宫一号”于2011年9月在酒泉卫星发射中心发射,标志着我国的航空航天技术迈进了一大步火箭的第一、二级发动机中,所用的燃料为偏二甲胼和四氧化二氮,偏二甲肼可用胼来制备。
|
|
| 3. 单选题 | 详细信息 |
|
已知充分燃烧a g乙炔(C2H2)气体时生成1 mol二氧化碳气体和液态水,并放出热量b kJ,则表示乙炔燃烧热的热化学方程式正确的是( )
A . 2C2H2(g)+5O2(g) =4CO2(g)+2H2O(g) ΔH=-4b kJ·mol-1
B . C2H2(g)+
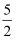 O2(g) =2CO2(g)+H2O(l) ΔH=-2b kJ·mol-1
C . C2H2(g)+ O2(g) =2CO2(g)+H2O(l) ΔH=-2b kJ·mol-1
C . C2H2(g)+ 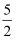 O2(g) =2CO2(g)+H2O(g) ΔH=+2b kJ·mol-1
D . 2C2H2(g)+5O2(g) =4CO2(g)+2H2O(l) ΔH=+4b kJ·mol-1 O2(g) =2CO2(g)+H2O(g) ΔH=+2b kJ·mol-1
D . 2C2H2(g)+5O2(g) =4CO2(g)+2H2O(l) ΔH=+4b kJ·mol-1
|
|
| 4. 综合题 | 详细信息 |
|
已知:在25
oC 101KPa时
①1g氢气完全燃烧生成气态水放出120.9 KJ的热量 ②2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ/mol ③Na2O2(s)+CO2(g)=Na2CO3(s)+ 在相同条件下根据以上信息回答下列问题:
|
|
| 5. 综合题 | 详细信息 | ||||||||
|
|||||||||
| 6. 综合题 | 详细信息 |
|
氮循环是指氮在自然界中的循环转化过程,含有较多蓝、绿藻类的酸性水体中存在如下图所示的氮循环。
请回答下列相关问题:
|
|
| 7. 单选题 | 详细信息 |
|
如图是反应CO(g)+2H2(g)=CH3OH(g)进行过程中的能量变化曲线。下列相关说法正确的是( )
A . 该反应是吸热反应
B . 使用催化剂后反应热减小
C . 热化学方程式为CO(g)+2H2(g)=CH3OH(g) ΔH=-510 kJ·mol-1
D . 曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化
|
|
| 8. 单选题 | 详细信息 |
|
高粱酿酒过程中的部分流程按顺序排列如下,其中能说明高粱转化过程中放出热量的是( )
A . A
B . B
C . C
D . D
|
|
| 9. 单选题 | 详细信息 |
|
根据下图所得判断正确的是( )
已知:H2O(g) = H2O(l) △H =﹣44 kJ/mol
A . 图 1 反应为吸热反应
B . 图 1 反应使用催化剂时,会改变其△H
C . 图 2 中若 H2O 的状态为液态,则能量变化曲线可能为①
D . 图 2 中反应为 CO2(g) + H2(g) = CO(g) + H2O(g) △H = + 41 kJ/mol
|
|
| 10. 单选题 | 详细信息 |
|
已知一定条件下断裂1 mol化学键生成气态原子需要吸收的能量如下:H—H 436 kJ;Cl—Cl 243 kJ;H—Cl 431 kJ。下列所得热化学方程式或结论正确的是( )
A . 氢分子中的化学键比氯气分子中的化学键更稳定
B . 2HCl(g) = H2(g) + Cl2(g)的反应热ΔH<0
C . H2(g) + Cl2(g) = 2HCl(g) ΔH=−183 kJ
D . 相同条件下,H2(g)+ Cl2(g) =2HCl(g)反应在光照和点燃条件下的ΔH不相等
|
|
- 2016-2017学年四川省成都市龙泉二中高三上学期期中化学试卷
- 北京市海淀区2020年高考化学一模试卷
- 吉林省长春市榆树市2019-2020学年高一上学期化学期末考试试卷
- 2016-2017学年湖北省襄阳市枣阳七中高三上学期开学化学试卷
- 专题20:化学键
- 2015-2016学年江西省赣州市于都三中高二下学期期中化学试卷
- 福建省莆田市2017-2018学年高考理综-化学二模考试试卷
- 北京市石景山区2017-2018学年高考理综-化学一模考试试卷(3月)
- 2016-2017学年湖北省重点高中联考高一下学期期中化学试卷
- 2015-2016学年四川省攀枝花十二中高一下学期期中化学试卷
- 江西省南昌市2017-2018学年高考理综-化学二模考试试卷
- 宁夏吴忠市吴忠中学2018-2019学年高一第一学期期化学模拟试卷
- 结构示意图 所表示的粒子是 A.分子 B.原子 C.阳离子
- 我国正处于社会主义初级阶段,大力发展生产力 ①体现了社会主义的本质要求 ②是解决我国社会主义主要矛盾的
- 若,则_______ ,___________ .
- 日本最著名的旅游胜地是( ) A.琉球群岛 B.富士山 C.濑户内海 D.金刚山
- 写木兰一家人高高兴兴迎接她回家的情景的句子:
- 下列各项中字形不合规范的一项是( ) A.长治久安 长年累月
- 西方的启蒙运动以解放人为目的,建立和发展了保护人的自由平等的普世思想。中国的新文化运动以“民主”和“科学”的名义批判传统
- 下列各组给定原子序数的元素,不能形成原子数之比为1:1稳定化合物的是 A.11和17
- 二战后,德国对法西斯文化进行了彻底的清算,崇尚民主平等和睦的文化,从此走上了和平发展的道路。而日本虽然在战后也走和平发展
- 已知冰的密度为0.9×103kg/m3,一定体积的水凝固成冰后,其体积将 () A.增加1/10 B.减
- (15分)在ABC中,C-A=, sinB=。 (I)求sinA的值; (II)设AC=,求ABC的面积。
- 如图所示,用电器正常工作时电流最小的是 ( )A.电熨斗B.电
- 阅读下面一段文言文,完成下列各题. 马周字宾王,博州茌平人。少孤,家窭(jù,家贫)狭。嗜学,善《诗》《春秋》。资
- 2009年1月13日,据新华网快讯,2008年全年,国家外汇储备增加4178亿美元,同比少增441亿美元,至2008年1
- 我国下列省级行政区域中,有两个简称的是( ) A.湖北、湖南 B.西藏、台湾 C.山西
- Yao-less Rockets KeepRising Houston Agencies (March9,2008)―
- 明朝后期,一条鞭法的实行是我国税制的又一重大变化,主要是因为 ①赋役合并 ②以钱募役
- 下列有关原子结构和元素周期律的表述正确的是 ①原子序数为15的元素的最高化合价为+3;②ⅦA族元素是同周期中非金属性最强
- 在一个算法的流程图中(图中∈),若当输入的值为10时,输出的结果为_____________。 说明:题中及图
- 物体受到两个互相垂直的作用力而运动,已知力F1做功6 J,物体克服力F2做功8 J,则力F1、F2的合力对物体做功(
 ΔH=-226 kJ/mol
ΔH=-226 kJ/mol
 2HNO2+2H2O+2H+ , 恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是(填标号)。
2HNO2+2H2O+2H+ , 恒温时在亚硝酸菌的作用下发生该反应,能说明体系达到平衡状态的是(填标号)。
 ]加入次氯酸钠固体,平衡时NO2-的去除率和温度投料比的关系如下图所示,a、b、c、d四点ClO-的转化率由小到大的顺序是 ,35℃时,该反应的平衡常数K= (保留三位有效数字)。
]加入次氯酸钠固体,平衡时NO2-的去除率和温度投料比的关系如下图所示,a、b、c、d四点ClO-的转化率由小到大的顺序是 ,35℃时,该反应的平衡常数K= (保留三位有效数字)。






