辽宁省大连市2017-2018学年高考理综-化学二模考试试卷
辽宁省大连市2017-2018学年高考理综-化学二模考试试卷
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列生活用品,主要由塑料制成的是( )
A . 车轮轮胎
B . 农用薄膜
C . 尼龙衣料
D . 棉T恤衫
|
|
| 2. 单选题 | 详细信息 |
|
设NA为阿伏加德罗常数的位,下列说法正确的是( )
A . 1molKMnO4固体完全分解制取O2 , 转移的电子数为2NA
B . 1L0.1mol/L的Na2CO3溶液中HCO3-和CO32-数目之和为0.1NA
C . 在密闭容器中,2molNO与1molO2充分混合后,气体分子数为3NA
D . 50mL 18.4mol/L浓硫酸与足量铜充分反应,生成SO2分子数目为0.46NA
|
|
| 3. 单选题 | 详细信息 |
|
喷普洛韦主要用于口唇或面部单纯疱疹,结构简式如图所示,下列说法错误的是( )
A . 喷普洛韦的分子式为C10H15N5O3
B . 喷普洛韦能发生取代反应
C . 1mol 该有机物与足量Na反应产生22.4LH2
D . 喷普洛韦分子中所有碳原子不可能都处于同一平面
|
|
| 4. 单选题 | 详细信息 |
|
短周期1-10号元素W、X、Y、Z的原子序数依次增大,W的最高正价和最低负价的代数和为0;X的一种核素在考古时常用来鉴定此文物的年代,Y的常见氢化物和最高价氧化物的水化物能反应生成一种离子化合物,工业上.采用液态空气分馏方法来生产Y的单质。根据以上叙述,下列说法中错误的是( )
A . 元素简单气态气化物的热稳定性:Z>Y>X
B . W可与同主族的元素形成离子化合物
C . W、X、Y、Z四种元素可形成水溶液显中性的盐
D . X、Z分别与W形成化合物的沸点一定有:X<Z
|
|
| 5. 单选题 | 详细信息 |
|
关于化学实验,下列说法正确的是( )
A . 图1操作可除去碱式滴定管胶管中的气泡
B . 图2装置课用作蒸馏时的接收装置
C . 图3可证明元素的非金属性:Cl>C>Si
D . 图4装置可用于除去Cl2中的水蒸气
|
|
| 6. 单选题 | 详细信息 |
|
如图是NO2和O2形成的原电池装置。下列说法错误的是( )
A . 石墨Ⅱ做正极,O2发生还原反应
B . 该电池放电时NO3-从右侧向左侧迁移
C . 当消耗1mol NO2时,电解质中转移1mol e
D . 石墨Ⅰ附近发生的反应为NO2+NO3--e-=N2O5
|
|
| 7. 单选题 | 详细信息 |
|
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系。下列说法正确的是( )
A . b点溶液中不可能存在NH3·H2O
B . b、c两点pH相同,但溶液的酸碱性不同
C . 通过降温的方法,可使溶液的状态中d点变为a点
D . a点溶液中可能大量共存的离子:Fe3+、Na+、Cl-、SO42-
|
|
| 8. 实验探究题 | 详细信息 |
|
软锰矿主要含有MnO2(约70%)、SiO2、Al2O3 , 闪锌矿主要含有ZnS(约80%)、FeS、CuS、SiO2。为了高效利用这两种矿石,科研人员开发了综合利用这两种资源的同槽酸浸工艺,主要流程如下图所示,回答下列问题:
|
|
| 9. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||
|
FeCl2是一种常用的还原剂。实验室用无水氯化铁和氯苯来制备无水FeCl2。反应原理:2FeCl3+C6H5Cl
 2FeCl2+C6H4Cl2+HCl 2FeCl2+C6H4Cl2+HCl
现设计如下方案:在A中放入16.25 g无水氯化铁和过量的氯苯,控制反应温度在128-139℃加热3 h.冷却、分离提纯得到粗产品;烧杯中所得盐酸(假设HCl完全被吸收)用AgNO3溶液滴定以测氯化铁转化率。 请回答下列问题:
|
|||||||||||||||||||||||||||||
| 10. 综合题 | 详细信息 |
|
H2S以及COS(羰基硫)是化学工作者重要的研究对象。请回答下列问题:
|
|
高中化学 试卷推荐
- 北京市西城区2017-2018学年高二下学期化学期末考试试卷
- 2017年北京市西城区高考化学一模试卷
- 安徽省池州市2018-2019学年高三上学期化学期末考试试卷
- 高中化学人教版(2019)选择性必修1 第四章第三节 金属的腐蚀与防护
- 2015-2016学年浙江省宁波市九所重点校高二上学期期末化学试卷
- 2016年浙江省杭州市高考化学二模试卷
- 人教版化学高二选修6第四单元实验4-4饮料的研究同步练习
- 2015-2016学年河北省衡水市景县中学高一下学期期中化学试卷
- 吉林松原油田高中2015-2016学年高一下学期化学开学考试试卷
- 2017-2018学年人教版选修4第三章《水溶液中的离子平衡》单元测试
- 人教版高中化学选修五 第五章 第三节 功能高分子材料
- 专题24:烯烃
最近更新
- 在下列句子的括号中,给加点字注音或根据拼音写汉字 ①通过多读好书,于和煦( )散文中感受温馨,于热辣杂文中感受ru
- 设a=0.32,b=20.3,c=log25,d=log20.3,则a,b,c,d的大小关系是__________(从小
- 下列文字表述与反应方程式对应且正确的是 A.0.5mol/LNaHSO4与0.5mol/LBa(OH)2混合至溶液呈中性
- 近来,越来越多的学生在校外租房而不愿住寝室。请根据下面提示,一分为二地写一篇短文,说说两者各自的好处与弊端,并发表你的观
- 如图,两个质量相同的小球P和Q,P球挂在一根长为L的细线上,Q球挂在橡皮绳上,现把两球拉到水平位置,并使橡皮绳刚好保持原
- 向一定量的Fe、FeO、Fe3O4的混合物中加入100mL2mol/L的盐酸,恰好使混合物完全溶解,放出224mL(标准
- “黄金搭档”维生素片中含Ca、Fe、Zn、Se等元素,其中属于组成生物体的大量元素的是() A.Ca
- (8分) 光电计时器是一种研究物体运动情况的常用计时仪器,其结构如图1所示,a、b分别是光电门的激光发射和接收装置,当有
- 对比是学习化学的重要方法.下列关于CO2与CO的比较错误的是() A.二氧化碳分子比一氧化碳分子多一个氧原子 B. CO
- 孔子生活的时代是( )A.春秋初期 B.春秋末期 C.战国时期 D.战国末期
- Setting _______ is very important, because they can help you
- 如图丁为电磁继电器自动报警装置,双金属片是在受热膨胀时自动接通电路时的装置。要求做到起火后能通过电铃报警。请将电路连接起
- 下图甲、乙两个玻璃瓶中分别装有等量的萌发种子和煮熟种子,加盖并放在温暖的地方一昼夜后,将燃烧的蜡烛同时放入甲、乙两瓶中,
- 某市出租车的收费标准是:起步价7元,超过3km时,每增加1km加收2.4元(不足1km按1km计).某人乘这种出租车从甲
- 下列各项中,有语病的一项是( ) A. 好莱坞大片在这几年越来越重视中国市场,通过各种方式来博得中国观众的欢心。
- 有暴力倾向,医生给病人注射一定量的某物质,使其出现暂时休克现象,若要使其迅速 苏醒,可注射另一种物质,这两种物质分别是(
- (2013临沂) 奇招击退红潮 丹丘生 ①在湖泊和海洋里,当藻类一生二、
- “新版人民币即将上市,先睹为快!”近日微信朋友圈中流传着这条微信,并被广泛转发。微信中附有500元等大面值的币样正反面
- A dark blue design will not on a blackboard. A. clear up
- 下列物质的转化能实现的是 【 】 A.H2SO4HCl B.CONa2CO3 C.Cu(OH)2





 MnO2+Zn+2H2SO4 , 写出阳极的电极反应式。
MnO2+Zn+2H2SO4 , 写出阳极的电极反应式。

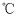 :时Ksp(AgCl,白色)=1.8×10-10 , Ksp(Ag2CrO4 , 砖红色)=3.4×10-11.
:时Ksp(AgCl,白色)=1.8×10-10 , Ksp(Ag2CrO4 , 砖红色)=3.4×10-11.  H2S(g)+CO(g) ΔH1=-17KJ/mol
H2S(g)+CO(g) ΔH1=-17KJ/mol 



