陕西省西安市临潼区2022届高三下学期第二次模拟考试理综化学试题
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
化学与生活紧密相关,下列叙述错误的是( )
A . “落红不是无情物,化作春泥更护花”蕴藏着自然界的碳、氮循环
B . “煤饼烧蛎房成灰”(蛎房即牡蛎壳),“灰”的主要成分是CaCO3
C . 电锯中的“烤蓝”工艺形成的致密氧化膜成分是Fe3O4
D . 服用阿司匹林(邻羟基苯甲酸)身体不舒服时,可以静脉注射NaHCO3溶液缓解
|
|
| 2. 单选题 | 详细信息 |
|
NA是阿伏加德罗常数的值,下列说法正确的是( )
A . 1mol重水比1mol水多2NA个中子
B . 46g分子式为C2H6O的有机物,含极性键数目为7NA
C . 1L1mol/L溴化铵水溶液中
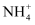 与H+数目之和为NA
D . 常温下,1molCl2与足量水反应转移的电子数目为NA 与H+数目之和为NA
D . 常温下,1molCl2与足量水反应转移的电子数目为NA
|
|
| 3. 单选题 | 详细信息 |
|
有机化合物Z可用于治疗阿尔茨海默症,其合成路线如下:
下列说法错误的是( )
A . 该反应为加成反应。
B . X、Y分子中含有的手性碳原子个数不同
C . Z的消去反应产物具有顺反异构体
D . Z的同分异构体不可能含两个苯环
|
|
| 4. 单选题 | 详细信息 |
|
某化合物结构如图所示,其中X。Y、W、Z是原子序数依次增大的短周期元素,且四种元素分布在三个周期,W的最外层电子数是Y的最外层电子数的2倍,Z和X同主族。下列说法正确的是( )
A . W与Z形成的化合物中只含离子键
B . 该化合物中Y都满足8电子稳定结构
C . X3YW3是弱酸
D . 离子半径:Z>W>Y
|
|
| 5. 单选题 | 详细信息 | ||||||||||||||||||||
|
下列实验操作、实验现象、解释或结论都正确且有因果关系的是( )
A . A
B . B
C . C
D . D
|
|||||||||||||||||||||
| 6. 单选题 | 详细信息 |
|
我国科研团队设计了一种表面锂掺杂的锡纳米粒子催化剂s—SnLi可提高电催化制甲酸盐的产率,同时释放电能,实验原理如图所示。下列说法错误的是( )
A . 放电时,每生成0.5molHCOO- , 整个装置内转移0.5NA个电子
B . 使用催化剂Sn或者s—SnLi均能有效减少副产物CO的生成
C . 放电时,正极电极周围pH升高
D . 使用s—SnLi催化剂,中间产物更不稳定
|
|
| 7. 单选题 | 详细信息 |
|
室温下,向20mL浓度均为0.1
 的 的 和 和 混合液中逐滴加入0.1 混合液中逐滴加入0.1 NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( ) NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( )
A . a点:
 B . 导电能力:b<c
C . c点:
B . 导电能力:b<c
C . c点: D . 由d点可得
D . 由d点可得
|
|
| 8. 综合题 | 详细信息 |
|
钒及其化合物在工业上有许多用途。从废钒(主要成分V2O3、V2O5、Fe2O3、FeO、SiO2)中提取五氧化二钒的一种工艺流程如图。
已知:①VOSO4能溶于水,VO2+与Fe不能反应。 ②有机溶剂H2R对VO2+及Fe3+萃取率高,但不能萃取Fe2+。 回答下列问题:
|
|
| 9. 实验探究题 | 详细信息 | |||||||||||||||
|
三氯氧磷(POCl3)可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化PCl3制备POCl3 , 反应原理为:P4(白磷)+6Cl2=4PCl3 , 2PCl3+O2=2POCl3。
已知:PCl3、POCl3的部分性质如下:
某化学兴趣小组模拟该工艺设计实验装置如图(某些夹持装置和加热装置已略去):
|
||||||||||||||||
| 10. 综合题 | 详细信息 |
|
乙烯是一种重要的基本化工原料,乙烯的产量可以衡量一个国家的石油化工发展水平,研究工业制取乙烯有重要的意义。
|
|
- 吉林省长春市第151中学2019-2020学年高二上学期化学期中考试试卷
- 河北省石家庄市2020年高考化学二模试卷
- 2019年高考化学真题分类汇编专题09:实验化学
- 2016年高考理综真题试卷(化学部分)(北京卷)
- 2017年高考真题分类汇编(化学):专题7 原电池、电解池工作原理及其应用
- 河北唐山市2020年高考化学一模试卷
- 江苏省南京师大附中2020年高考化学一模试卷
- 2015-2016学年云南省昭通市云天化中学高一下学期期中化学试卷
- 山东省日照市2019-2020学年高一下学期化学期末考试试卷
- 2015-2016学年河北省邯郸市鸡泽、馆陶、春光三县联考高一下学期期中化学试卷
- 2016-2017学年四川省德阳市中江县龙台中学高一上学期期中化学试卷
- 2018年高考理综化学真题试卷(北京卷)
- 关于人类活动对气候的影响的说法,正确的是( ) A、植树造林可以使气温升高 B、修建水库可使当地温
- 自2007年10月24日起,一颗飞往月球的卫星让国人的头高高扬起,是关注也是自豪。2007年11月26日9时41分,嫦娥
- 下列各句中,没有语病的一句是A.国家技术监督总局汪总工程师,对河南省铁路技术改造总公司就全省铁路电气化改造提 出设想的肯
- Always read the __ on tile bottle carefully and take the rig
- I don’t mean __ you because what I have said really means __
- 小明帮爷爷在院落装照明灯,为了延长灯的使用寿命,他将两盏标有“220V 60W”的白炽灯串联接在家庭电路中,通电后两灯
- 华为Mate20手机搭载了全球首款7纳米制程芯片,7纳米就是0.000000007米.数据0.000000007用科学记
- 花岗岩密度大、硬度高,表面耐磨,常用于建筑装修,厨房台面等.形成花岗岩的地质作用是 A.地震 B.变质作用
- ______good news! We have never heard ______ wonderful news.
- 如图所示,两根相距为L的竖直平行金属导轨位于匀强磁场 中,磁感应强度为B,导轨电阻不计,另两根与光滑轨道接触 的金属杆质
- 下图为某红绿色盲患者家系图,据图分析作答(相关基因用B、b 表示):(1)红绿色盲的的致病基因位于 (X染色体、
- 函数y=的定义域是 .
- We climbed higher _____ we might see the scenes better. A
- 爱是一朵无声花 葛闪 23年前,我在乡里邮局工作。 那是一个冬日的下午。邮局外,鹅毛般的大雪纷纷扬扬下了一天一夜,整个世
- 新版电视剧 《三国 》有许多雷人台词,其中包括刘备参加会盟时所说的“天 下兴亡,匹夫有责”。网友调侃称:“原作者应该穿越
- 将抛物线向上平移2个单位, 再向右平移3个单位,所得抛物线的解析式为( ).A. B.
- 下列各溶液中,微粒的物质的量浓度关系正确的是A 0.1mol/L的(NH4)2SO4溶液中,c(SO42-)>c(NH
- 下列日常生活中的变化现象,属于缓慢氧化的是( ) A.白炽灯泡通电发光发热 B.木炭燃烧
- .1992年,许多国家举行纪念哥伦布成功远航美洲的活动,但也引起美洲印第安人后裔的强烈不满。他们打出一条标语,上面写着:
- Persons with whom we can__________our innermost feelings are





 VOR+2H+。为了提高VO2+的产率,反萃取剂可选用。(供选物质:NaCl,NaOH,H2SO4 , 填写相应物质的化学式)
VOR+2H+。为了提高VO2+的产率,反萃取剂可选用。(供选物质:NaCl,NaOH,H2SO4 , 填写相应物质的化学式)
 , ClO
, ClO
 CH2=CH2(g)+4H2O(g) ΔH1
CH2=CH2(g)+4H2O(g) ΔH1





