高中化学人教版选修4 第一章 单元测试卷
高中化学人教版选修4 第一章 单元测试卷
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高二上学期
文件类型:.doc
发布时间:2026-04-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
下列说法不正确的是( )
A . 化学反应除了生成新物质外,还伴随着能量的变化
B . 放热反应都不需要加热就能发生
C . 吸热反应在一定条件(如高温、加热等)下也能发生
D . 化学反应是放热还是吸热,取决于生成物具有的总能量和反应物具有的总能量
|
|
| 2. 单选题 | 详细信息 |
|
已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。现有以下四个化学反应方程式:①H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);②H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l);③HCl(aq)+NH3·H2O(aq)=NH4Cl(aq)+H2O(l);④CH3COOH(aq)+NH3·H2O(aq)=CH3COONH4(aq)+H2O(l),其中放出的热量为57.3 kJ的是( )
A . ①和②
B . ③
C . ④
D . 以上都不对
|
|
| 3. 单选题 | 详细信息 |
|
对于:2C4H10(g)+13O2(g)=8CO2(g)+10H2O(l) ΔH=-5 800 kJ·mol-1的叙述错误的是( )
A . 该反应的反应热为ΔH=-5 800 kJ·mol-1 , 是放热反应
B . 该反应的ΔH与各物质的状态有关,与化学计量数也有关
C . 该式的含义为:25 ℃、101 kPa下,2 mol C4H10气体完全燃烧生成CO2和液态水时放出热量5800kJ
D . 该反应为丁烷燃烧的热化学方程式,由此可知丁烷的燃烧热为5 800 kJ·mol-1
|
|
| 4. 单选题 | 详细信息 |
|
下列关于反应能量的说法正确的是( )
A . Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s) ΔH=-216 kJ·mol-1 , 则反应物总能量>生成物总能量
B . 相同条件下,如果1 mol氢原子所具有的能量为E1 , 1 mol氢分子所具有的能量为E2 , 则2E1=E2
C . 101 kPa时,2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1 , 则H2的燃烧热为571.6 kJ·mol-1
D . H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1 , 则含1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量
|
|
| 5. 单选题 | 详细信息 |
|
分析下图的能量变化,确定该反应的热化学方程式书写正确的是( )
A . 2A(g)+B(g)=2C(g) ΔH<0
B . 2A(g)+B(g)=2C(g) ΔH>0
C . 2A+B=2C ΔH<0
D . 2C=2A+B ΔH<0
|
|
| 6. 单选题 | 详细信息 |
|
下列关于热化学反应的描述中正确的是( )
A . HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1 , 则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3) kJ·mol-1
B . CO(g)的燃烧热是283.0kJ·mol-1 , 则2CO2(g)=2CO(g)+O2(g)的ΔH=2×(+283.0) kJ·mol-1
C . 需要加热才能发生的反应一定是吸热反应
D . 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
|
|
| 7. 单选题 | 详细信息 |
|
表示戊烷燃烧热的热化学方程式正确的是( )
A . C5H12(l)+8O2(g)=5CO2(g)+6H2O(l) ΔH=-3 540 kJ·mol-1
B . C5H12(l)+8O2(g)=5CO2(g)+6H2O(g) ΔH=-3 540 kJ·mol-1
C . C5H12(l)+8O2(g)=5CO2(g)+6H2O(g) ΔH=+3 540 kJ·mol-1
D . C5H12(l)+8O2(g)=5CO2(g)+6H2O(l) ΔH=+3 540 kJ·mol-1
|
|
| 8. 单选题 | 详细信息 |
|
在36 g碳不完全燃烧所得气体中,CO占
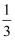 体积,CO2占 体积,CO2占 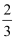 体积。且有: 体积。且有: C(s)+ CO(g)+ 与这些碳完全燃烧相比,损失的热量是( )
A . 172.5 kJ
B . 1 149 kJ
C . 283 kJ
D . 517.5 Kj
|
|
| 9. 单选题 | 详细信息 |
|
在1 200 ℃时,天然气脱硫工艺中会发生下列反应
①H2S(g)+ ②2H2S(g)+SO2(g)= ③H2S(g)+ ④2S(g)=S2(g) ΔH4 则ΔH4的正确表达式为( )
A . ΔH4=
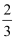 (ΔH1+ΔH2-3ΔH3)
B . ΔH4= (ΔH1+ΔH2-3ΔH3)
B . ΔH4= 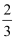 (3ΔH3-ΔH1-ΔH2)
C . ΔH4= (3ΔH3-ΔH1-ΔH2)
C . ΔH4=  (ΔH1+ΔH2-3ΔH3)
D . ΔH4= (ΔH1+ΔH2-3ΔH3)
D . ΔH4=  (ΔH1-ΔH2-3ΔH3) (ΔH1-ΔH2-3ΔH3)
|
|
| 10. 单选题 | 详细信息 |
|
已知:P4(g)+6Cl2(g)=4PCl3(g) ΔH=a kJ·mol-1 ,
P4(g)+10Cl2(g)=4PCl5(g) ΔH=b kJ·mol-1 , P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ·mol-1 , PCl3中P—Cl键的键能为1.2c kJ·mol-1。下列叙述正确的是( )
A . P—P键的键能大于P—Cl键的键能
B . 可求Cl2(g)+PCl3(g)=PCl5(s)的反应热ΔH
C . Cl—Cl键的键能为
 kJ·mol-1
D . P—P键的键能为 kJ·mol-1
D . P—P键的键能为  kJ·mol-1 kJ·mol-1
|
|
高中化学 试卷推荐
- 浙江省嘉兴市2019-2020学年高一下学期化学期末考试试卷
- 湖南省常德市2019-2020学年高一上学期化学期末考试试卷
- 福建省福州市2019-2020学年高一下学期化学期末考试试卷
- 湖南省常德市2019-2020学年高一下学期化学期末考试试卷
- 云南省腾冲市第八中学2017-2018学年高二上学期化学期中考试试卷
- 安徽省宿州市埇桥区2018-2019学年高二文)上学期化学期末考试试卷
- 2015-2016学年四川省德阳市高一上学期期末化学试卷
- 浙江省丽水市第二中学2019-2020学年高一上学期化学期中考试试卷
- 2018-2019学年度 高一年级上学期化学期末考试卷
- 吉林省扶余市第一中学2018-2019学年高一上学期化学期中考试试卷
- 河南省焦作市2016-2017学年高一上学期化学期中考试试卷
- 北京市丰台区2017-2018学年高考理综-化学二模考试试卷
最近更新
- 许多淡水鱼在人工饲养条件下不产卵,常取同种鱼的垂体研碎注射到鱼体内,使之能正常排卵。这主要是利用垂体分泌的
- 我市开发的多处温泉度假村是休闲度假的好地方。 (1)温泉水富含钾、钙、镁、氟、硅等,这里的“钾、钙、镁、氟、硅”是指(填
- It’s very____of you not to talk aloud while the baby is asle
- 某同学用嘴往气球里吹气,吹一段时间后感到头晕,其原因是( ) A.呼吸肌运动过于强烈,使呼吸中枢疲劳 B.呼吸肌运
- 阅读刘义庆的《丑女》一文,完成小题。(14分)许允妇①是阮卫尉女,德如妹,奇丑。交礼竟②,允无复入理③,家人深以为忧。会
- 2015年,我国围绕“和平发展”理念积极建构好中美、中俄“大国关系”这两个重“点”,围绕“合作共赢”理念,搭建“丝绸之路
- 中国于1937年7月郑重承诺:“取消一切推翻国民党政权的暴动政策及赤化运动,停止以暴力没收地主土地的政策,取消现在的苏维
- 2013年2月27日,十二届全国人大代表名单公布。各地区、各民族、各方面都有适当数量的代表,全国55个少数民族都有本民族
- 若△ABC的三条边a,b,c满足关系式:a4+b2c2-a2c2-b4=0,则△ABC的形状是_____.
- 一导线弯成如右图所示的闭合线圈,以速度v向左匀速进入磁感应强度为B的匀强磁场,磁场方向垂直平面向外。线圈总电阻为R,从线
- 《沁园春·雪》的部分词句描写与其地理要素对应正确的是()A.千里冰封,万里雪飘——
- 北大教授周其仁在接受《中国经济周刊》记者采访时表示,城镇化不以学者的意志为转移,也不以官员的意志为转移,人往哪儿流动是有
- 已知向量,,向量垂直于轴,则实数 ▲ .
- 下列变化中不需要破坏化学键的是 ( ) A.加热氯化铵 B.干冰气
- 直线x+2y=0被曲线x2+y2-6x-2y-15=0截得的弦长为
- 在阿房宫遗址出土的一块秦砖上,用小篆刻写了“海内皆臣,岁登成熟,道毋饥人”十二个字。其中“海内皆臣”这四个字最能表明秦朝
- 古希腊哲学家泰勒斯提出“水是万物的始基”。中国春秋时代《管子》一书中也指出“水者,何也?万物之本原也”。他们的观点属于
- 2009年3月1日,“嫦娥一号”卫星准确落向月球预定撞击点,为中国探月一期工程画上了圆满的句号。 下列关于“嫦娥一号”的
- 如图,共有12个大小相同的正方形,其中阴影部分的5个小正方形是一个正方体的表面展开图的一部分,请从其余的小正方形中选取一
- (08年宁夏卷)(物理─选修3-5)(9分)某同学利用如图所示的装置验证动量守恒定律。图中两摆摆长相同,悬挂于同一高度,

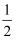 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1


