浙江省2018年4月普通高校招生选考科目-化学模拟试题
浙江省2018年4月普通高校招生选考科目-化学模拟试题
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
教材科目:化学
试卷分类:高考
文件类型:.doc
发布时间:2026-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | 详细信息 |
|
在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表。下列判断不正确的是( )
A . a=6.00
B . 同时改变反应温度和蔗糖的浓度,v可能不变
C . b<318.2
D . 不同温度时,蔗糖浓度减少一半所需的时间相同
|
|
| 2. 单选题 | 详细信息 |
|
下列叙述中正确的是( )
A . 实验室欲配制480mL0.10mol•L﹣1的CuSO4溶液,可用12.0g胆矾及相应容器配制
B . 将适量FeCl3饱和溶液滴入沸水中并不断搅拌可制得氢氧化铁胶体
C . 实验室中从海带里提取碘的过程是:灼烧→溶解→过滤→萃取
D . 用分液漏斗、烧杯、铁架台(带铁圈)、饱和Na2CO3溶液可除去乙酸乙酯中的乙酸
|
|
| 3. 单选题 | 详细信息 |
|
甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是( )
①甲由水电离出来的H+的物质的量浓度是乙的 ②物质的量浓度c(甲)=10c(乙) ③中和等物质的量的NaOH溶液需甲、乙两杯酸的体积,10V(甲)>V(乙) ④甲中的c(OH﹣)为乙中的c(OH﹣)的10倍.
A . ①②④正确
B . ①③正确
C . ②④正确
D . 只有①正确
|
|
| 4. 综合题 | 详细信息 |
|
某研究小组为了探究固体甲(二元化合物)和固体乙(无机矿物盐,含五种元素)的组成和性质,设计并完成了如下实验:
已知:向溶液1中连续滴加盐酸,先产生白色沉淀,后沉淀溶解;向溶液2中连续通入气体2,也是先产生白色沉淀,后沉淀溶解.请回答下列问题:
|
|
| 5. 实验探究题 | 详细信息 | ||||||||||||||||||||||||||||
|
对氯苯甲酸是合成非甾族消炎镇痛药的中间体,还能用于燃料和浓药的合成,实验室中制备对氯苯甲酸的反应、装置图如图2:
常温条件下的有关数据如表所示:
实验步骤:在规格为250mL的装置A中加入一定量的催化剂、适量KMnO4、100mL水;安装好装置,在滴液漏斗中加入6.00mL对氯甲苯,在温度为93℃左右时,逐滴滴入对氯甲苯;控制温度在93℃左右,反应2h,过滤,将滤渣用热水洗涤,使洗涤液与滤液合并,加入稀硫酸酸化,加热浓缩;然后过滤,将滤渣用冷水进行洗涤,干燥后称量其质量为7.19g. 请回答下列问题:
|
|||||||||||||||||||||||||||||
| 6. 单选题 | 详细信息 |
|
仪器名称为“蒸馏烧瓶”的是( )
A .
 C .
C . |
|
| 7. 单选题 | 详细信息 |
|
下列物质的分类合理的是( )
A . 氧化物:CO2、NO,SO2、H2O
B . 碱:NaOH,KOH,Ba(OH)2、Na2CO3
C . 铵盐:NH4Cl、NH4NO3、NH3•H2O
D . 碱性氧化物:Na2O,CaO,CO2、Al2O3
|
|
| 8. 单选题 | 详细信息 |
|
下列关于胶体和溶液的说法正确的是( )
A . 胶体区别于其他分散系的本质特征是分散质的微粒直径在1~100 nm之间
B . 溶液呈电中性,胶体带有电荷
C . 溶液中分散质微粒能透过滤纸,胶体中分散质微粒不能透过滤纸
D . 制备氢氧化铁胶体时,可以将饱和FeCl3溶液滴入沸水,然后长时间煮沸
|
|
| 9. 单选题 | 详细信息 |
|
下列说法正确的是( )
A . 化学键的形成一定伴随着电子的转移和能量变化
B . NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同
C . 24Mg32S晶体中电子总数与中子总数之比为1:1
D . 某晶体固态不导电水溶液能导电,说明该晶体是离子晶体
|
|
| 10. 综合题 | 详细信息 |
|
一定条件下,将一定体积的H2和Cl2的混合气体点燃,充分反应后,将混合气体通入含amol NaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含有Cl﹣、ClO﹣、ClO3﹣且三者物质的量之比为8:1:1,则:
|
|
高中化学 试卷推荐
- 黑龙江省齐齐哈尔市2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年山东省枣庄市滕州市高三上学期期中化学试卷(四)28
- 第27讲:有机合成与推断
- 2016年江西省宜春市万载二中实验班高考化学四模试卷
- 2019年高考化学真题分类汇编专题02:离子、溶液中物质的反应
- 2016年浙江省宁波市镇海中学高考化学二模试卷
- 江西省萍乡市2018-2019学年高考化学一模考试试卷
- 2018年高考化学真题分类汇编专题12:物质的分离、提纯和检验
- 专题23:烷烃
- 2015-2016学年湖北省襄阳市枣阳二中高一下学期期中化学试卷
- 备考2018年高考化学二轮专题复习 专题十三:化学实验基础
- 天津市咸水沽第二中学2020年高考化学模拟试卷
最近更新
- The birthrate is Europe has been in a steady decrease since
- 维新变法期间,由梁启超主编、被誉为“中国创始第一种有益之报”的是 A.《中外纪闻》
- 某实验小组的同学用氢氧化钡溶液和盐酸进行中和反应的实验时,向烧杯中的氢氧化钡溶液加入一定量稀盐酸后,发现忘记了滴加指示剂
- (07年浙江卷)年“”是“”的()A.充分而不必要条件 B.必要而不充分条件C.充分必要条件
- 人们认为烟火(如下图)就是喷气式火箭的前身中国是航天技术的故乡。这一起源至少可以追溯到A.隋朝
- 在下列各图中,每个图的两个变量具有相关关系的图是( ) (1)
- 将4.32g氧化亚铁跟稀硝酸发生氧化还原反应,若生成的氧化产物是硝酸铁,而还原产物是一氧化氮,则参加反应的硝酸共有
- —Miss Zhou is very popular with the students.—Yes. Her class
- 新中国成立初期,开展外交工作的首要目标是 A.打破帝国主义封锁 B.提高国际地位 C.在国际舞台上要站稳脚跟 D.一边倒
- 3. 下列各选项中,没有语病的一项是( ) A.在电影《祝福》中有这样一个情节:在祥林嫂捐了门槛之
- 阅读下段材料,回答问题。 上海目前每年消耗煤炭4 200多万吨,占全市能源总量的70%左右,其煤炭消耗量和消耗密度
- 现有下列物质:①氧气和臭氧 ②稀有气体 ③高锰酸钾加热制氧气后的剩余物 ④水和双氧水 ⑤冰和水的混合体 ⑥五
- 仿照下面的示例,自选话题,另写三句话,修辞及句式与示例相同。(6分) 他们在天上,愿为一颗星; 他们在地上,愿为一盏灯;
- Whathe said at the meeting suggested that he __________ wit
- 按要求写出下列名篇名句中的空缺部分。(两题任选一题)(5分) (1)杜甫在《客至》中,描写所居草堂环
- 孙中山将同盟会纲领阐述为“民族、民权、民生”的三民主义。以下最能体现“民生主义”的一项是( ) A、驱除鞑虏
- 希腊城邦政治的核心是 A、元老院 B、贵族 C、大法官 D、公民
- 1.下列词语中加横线字读音全都正确的一项是( ) A.跟帖(tiě) 弱冠(guàn) 闷葫芦(mēn)
- 下列激素中,对全身细胞都起作用的是( ) A.促甲状腺激素释放激素 B.促甲状腺激素 C.甲状腺激素
- 辣椒果皮的红色和黄色是一对相对性状。研究者进行杂交实验,结果如下表。据此推测亲代的基因组成(用R 、 r 表示)分别为亲

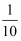 倍
倍




