电解质溶液的导电性 知识点题库
下列溶液中导电性最强的是( )
A . 1L 0.1mol/L醋酸
B . 0.5L 0.1mol/L H2SO4溶液
C . 1L 0.1mol/L盐酸
D . 2L 0.1mol/L H2SO3溶液
下列图示与对应的叙述相符的是( )
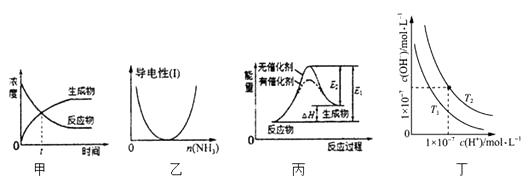
A . 图甲表示某可逆反应物质的浓度随时间的变化,且在t时刻达到平衡状态
B . 图乙表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化
C . 图丙表示某吸热反应分别在有、无催化剂的情况下,反应过程中的能量变化
D . 图丁表示不同温度下水溶液中H+和OH-浓度的变化曲线,图中温度丁T1<T2
化学中常用图像直观地描述化学反应的进程或结果。下列有些图像描述正确的是( )
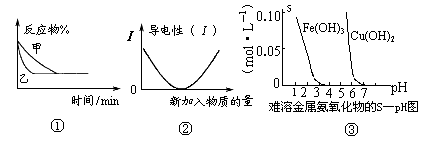
A . 当反应COCl2(g)  CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
B . 图1可能表示压强对可逆反应A(g)+2B(g)
CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
B . 图1可能表示压强对可逆反应A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强大
C . 图2可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D . 据图3,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右
3C(g)+D(s)的影响,乙的压强大
C . 图2可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D . 据图3,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右
 CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
B . 图1可能表示压强对可逆反应A(g)+2B(g)
CO(g)+Cl2(g);△H>0,达到平衡时①升温②减压③加催化剂都能提高COCl2转化率
B . 图1可能表示压强对可逆反应A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强大
C . 图2可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D . 据图3,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右
3C(g)+D(s)的影响,乙的压强大
C . 图2可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D . 据图3,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量Cu至pH在4左右
下列说法正确的是( )
A . 将AlCl3溶液加热蒸干得到纯净的氯化铝晶体
B . 强电解质都易溶于水,所以BaSO4是弱电解质
C . 强酸溶液一定比弱酸溶液导电性强
D . 电解质溶液的导电过程会发生化学变化
下列叙述正确的是( )
A . NaCl溶液在电流作用下电离成Na+与Cl-
B . 溶于水后能电离出H+的化合物都是酸
C . 氯化氢溶于水能导电,但液态氯化氢不能导电
D . 硫酸钡难溶于水,所以硫酸钡是非电解质
根据已经学过的化学知识,回答下列问题。
-
(1) I.现有下列十种物质:①蔗糖 ②熔融KNO3 ③石墨 ④铜丝 ⑤NaOH固体 ⑥SO3 ⑦BaSO4固体 ⑧K2O固体 ⑨液态H2SO4 ⑩液氯 上述物质中可导电的是(填序号,下同);上述物质中不能导电,但属于电解质的是。
-
(2) NaHSO4是一种酸式盐,请填写下列空白:
①写出NaHSO4在水中的电离方程式 。
②与0.1 mol·L-1的NaHSO4溶液的导电能力相同的硫酸钠溶液的物质的量浓度为:。
③NaHSO4溶液与NaHCO3溶液反应的离子方程式为。
-
(3) 粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用,①Na2CO3、②NaOH、③BaCl2、④HCl,用序号表示加入的先后顺序依次是。
-
(4) II.A,B,C,X均为中学常见物质,它们在一定条件下有如下转化关系(副产物已略去)。
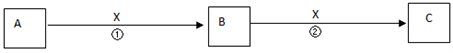
若X是氧气,则A不可能 (填序号)
A.C B.Si C.Na D.Mg
-
(5) 若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生了不溶于稀HNO3的白色沉淀,则B的化学式为;C溶液在贮存时应加入少量X,理由是(用离子方程式表示)。检验B溶液中阳离子的操作方法是。
-
(6) 若X是氢氧化钠溶液,A、B、C均为含铝元素的化合物,则反应②的离子方程式为。
在一定温度下,向不同的电解质溶液中加入新物质时溶液的导电性发生变化,其电流强度(I)随物质加入量(m)的变化曲线如图所示。其中与A图变化趋势一致的是(填编号,下同),与B图变化趋势一致的是,与C图变化趋势一致的是
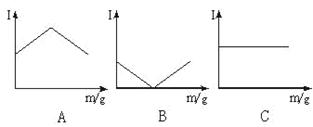
①H2SO4溶液中加入适量BaCl2固体
②氢硫酸(H2S)溶液中滴入稀NaOH溶液至过量
③澄清石灰水中通入CO2至过量
④NaOH溶液中通入适量Cl2
⑤Ba(OH)2溶液中滴入H2SO4溶液至过量
下列物质的导电性能最差的是( )
A . 熔化的氢氧化钠
B . 0.1mol·L-1盐酸
C . 0.1mol·L-1醋酸
D . 氯化钾固体
现有物质 ①铜 ②干冰
③盐酸
④液态醋酸 ⑤蔗糖
⑥NaHSO4 固体
⑦Ba(OH)2溶液
⑧ 熔融的
NaCl
-
(1) 能导电的是:属于电解质的是:
-
(2) 将NaHSO4固体溶于水,写出NaHSO4的电离方程式:
-
(3) ① 向Ba(OH)2溶液中逐滴滴加NaHSO4溶液至 Ba2+恰好完全沉淀,发生反应的离子方程式为: ;
②Ba2+恰好沉淀后继续滴加NaHSO4溶液时,发生反应的离子方程式为:
下列溶液中加入少量NaOH固体导电能力变化不大的是( )
A . NH3·H2O
B . CH3COOH
C . 盐酸
D . H2O
下列状态的物质,既能导电又属于电解质的是( )
A . 漂白粉
B . 钢
C . 液态氯化氢
D . 熔融的氯化钠
下列叙述中,正确的是( )
A . 用洁净的铂丝蕴取某无色溶液在无色火焰上灼烧,火焰呈黄色,该无色溶液一定为钠盐
B . 铜丝、石墨均能导电,所以它们都是电解质
C . NaCl溶于水,在通电条件下才能发生电离
D . 熔融的 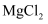 能导电,所以
能导电,所以 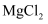 是电解质
是电解质
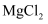 能导电,所以
能导电,所以 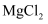 是电解质
是电解质
常温下,将一定浓度的盐酸和醋酸加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示。下列说法正确的是( )
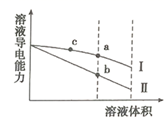
A . 两溶液稀释前的浓度相同
B . a、b、c三点溶液的pH由大到小顺序为b>a>c
C . b点的Kw值比a点的Kw值大
D . a点水电离的n(H+)小于c点水电离的n(H+)
某化学兴趣小组进行化学实验,按照图甲连接好线路发现灯泡不亮,按照图乙连接好线路发现灯泡亮,由此得出的结论正确的是( )
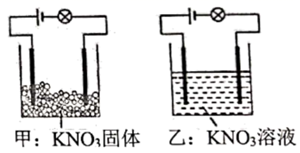
A . 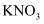 固体不导电,所以
固体不导电,所以 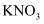 是非电解质
B .
是非电解质
B . 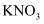 溶液可以导电,所以
溶液可以导电,所以 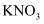 溶液是电解质
C .
溶液是电解质
C . 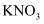 在水溶液中电离出了可以自由移动的离子
D .
在水溶液中电离出了可以自由移动的离子
D . 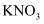 只有在溶液中才能导电
只有在溶液中才能导电
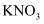 固体不导电,所以
固体不导电,所以 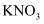 是非电解质
B .
是非电解质
B . 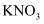 溶液可以导电,所以
溶液可以导电,所以 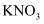 溶液是电解质
C .
溶液是电解质
C . 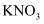 在水溶液中电离出了可以自由移动的离子
D .
在水溶液中电离出了可以自由移动的离子
D . 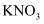 只有在溶液中才能导电
只有在溶液中才能导电
按要求填空:
-
(1) 写出下列物质溶于水或熔融状态下的电离方程式:
①CaCl2:;②NaHCO3:;③Ba(OH)2:;④熔融状态的KHSO4:。
-
(2) 现有以下物质:①NaCl晶体②液态HCl③CaCO3固体④熔融KCl⑤蔗糖⑥铜⑦CO2⑧H2SO4⑨KOH固体
a.以上物质中能导电的是(填字母序号,下同);
b.以上物质中属于电解质的是,属于非电解质的是;
c.以上物质中,溶于水且生成的水溶液能导电的物质是。
-
(3) 在反应KMNO3+HCl→KCl+MnCl2+Cl2↑+H2O(未配平)中,氧化产物是(填化学式),当有5molHCl被氧化时,被还原的KMnO4为mol。
-
(4) 现需配制0.1mol·L-1NaOH溶液450mL,如图是某同学转移溶液的示意图。
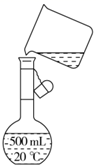
①根据计算用托盘天平称取NaOH固体的质量为g,为完成此溶液配制实验需要的玻璃仪器有;
②图中的不正确是;
③配制溶液时,下列操作会导致所配溶液的浓度偏低的是(填字母序号)。
a.洗涤烧杯和玻璃棒的溶液未转移入容量瓶中
b.定容时,眼睛俯视使溶液凹液面最低点与容量瓶刻度线相切
c.容量瓶中原残留有少量蒸馏水
d.定容后加水过量,又从容量瓶中取出部分溶液,使液面降至刻度线
浓度均为 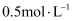 三种酸
三种酸  、
、  、
、 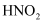 ,分别与
,分别与  溶液反应,导电能力与
溶液反应,导电能力与  的体积变化如图所示,下列说法正确的是( )
的体积变化如图所示,下列说法正确的是( )
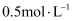 三种酸
三种酸  、
、  、
、 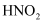 ,分别与
,分别与  溶液反应,导电能力与
溶液反应,导电能力与  的体积变化如图所示,下列说法正确的是( )
的体积变化如图所示,下列说法正确的是( ) 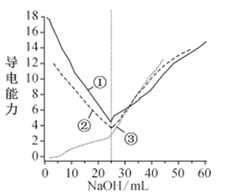
A . 曲线①是  变化图像
B . 曲线③是
变化图像
B . 曲线③是 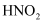 变化图像
C . 曲线②的拐点是滴定终点
D . 拐点后取决于
变化图像
C . 曲线②的拐点是滴定终点
D . 拐点后取决于  导电能力
导电能力
 变化图像
B . 曲线③是
变化图像
B . 曲线③是 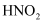 变化图像
C . 曲线②的拐点是滴定终点
D . 拐点后取决于
变化图像
C . 曲线②的拐点是滴定终点
D . 拐点后取决于  导电能力
导电能力
下列各实验过程中,溶液的导电能力变化不大的是:( )
A . 醋酸溶液中滴入氨水至过量
B . 澄清石灰水中通入CO2至过量
C . Ba(OH)2溶液中滴入H2SO4溶液至过量
D . NH4Cl溶液中加入NaOH固体至恰好反应
下列有关溶液导电能力的说法错误的是(忽略溶液混合时的体积变化)( )
A . 向氢氧化钡溶液中逐滴加入硫酸铜溶液至过量,溶液的导电能力先减弱后增强
B . 醋酸溶液中加入适量烧碱溶液,溶液的导电能力减弱
C . 盐酸的导电能力不一定比醋酸溶液强
D . 向氯化钠溶液中加入少量硝酸银溶液,溶液的导电能力几乎不变
常温下,向一定体积0.1 mol·L-1的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH[pOH=-lg c(OH-)]与pH的变化关系如图所示,则( )
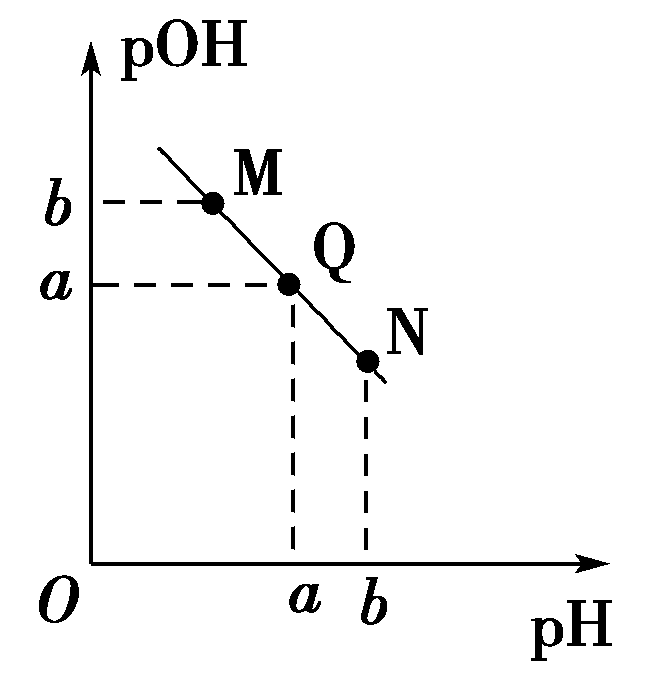
A . M点所示溶液的导电能力强于Q点
B . N点所示溶液中c(CH3COO-)>c(Na+)
C . Q点pH一定等于7
D . Q点消耗NaOH溶液的体积等于醋酸溶液的体积
同学利用如图装置试验物质的导电性。在烧杯中放入试剂X,将石墨电极插入其中连好电路,打开电源,小灯泡能发光的是( )
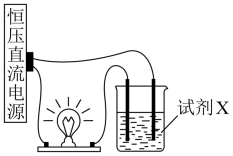
试剂X | NaCl固体 | 水 | 酒精 | 稀硫酸 |
选项 | A | B | C | D |
A . A
B . B
C . C
D . D
最近更新
- 被我们比喻为经济发展“先行官”的是 A.工业 B.农业 C.交通运输业
- 2014年全国两会政府工作报告指出,当前改革已进入攻坚期和深水区,必须紧紧依靠人民群众,以壮士断腕的决心,背水一战的气概
- 在强酸性无色透明溶液中能大量共存的离子组是()。A.K+、Na+、CO32-、MnO4- B.Mg2+、Na+、Cl-、
- 无论对儿童、青少年还是老年,钙的作用都是重要的。人体中最大的“钙库”是A.小肠 B.骨
- (8分)如图所示,质量不等的三个物块A、B、C用劲度系数完全相同的三个弹簧1、2、3依次连接着处于静止状态,A、B在水平
- 《中华人民共和国各级人大常委会监督法》规定,最高人民法院和最高人民检察院在具体应用法律时作出的解释(即司法解释),应当报
- 下列各组混合物,可以用分液漏斗分离的是 A.苯和乙醇 B.乙酸和水 C.硝基苯和苯
- 下列对中国传统文化主流思想──儒家思想的阐述,有误的是( ) A.春秋战国时期产生了我国的早期儒学 B.汉武
- 图(1)表示的是某综合商场今年1~5月的商品各月销售总额的情况,图(2)表示的是商场服装部各月销售额占商场当月销售总额的
- 根据你的经历与理解,选择中华民族的一个传统节日,写一段说明性文字。 要求:(1)说明顺序合理、清晰;(2)运用举例子、作
- 下列多项式乘法中不能用平方差公式计算的是( )A、 B、C、 D、
- 以下实验装置一般不用于分离物质的是( )
- 古诗文名句默写。(10分)(1)忽如一夜春风来,____________________。(岑参《白雪歌送武判官归京》)
- . 第六节 书面表达(共25分) 假设你是一名高中生,名叫李华,自认为符合2010年上海世博招聘志愿者的条件,请用英语写
- 基因型为YyRr的水稻自交,其子代中的表现型、基因型分别有() A.3种、9种 B.3种、1
- 晋太元中,武陵人捕鱼为业。缘溪行,忘路之远近。忽逢桃花林,夹岸数百步,中无杂树,芳草鲜美,落英缤纷。渔人甚异之。复前行,
- 如图所示,甲车从A处沿公路a向右行驶,同时乙车从B处出发,乙车行驶的速度与甲车行驶的速度相同,乙车要在最短的时间在公路a
- 为了获取大量可以饮用的水,自来水厂把天然水中的悬浮物及微生物除去要达到此目的,一般要经过的主要步骤是__________
- 三个互不相同的实数是等比数列{an}中的连续三项,并且它们依次又为一等差数列中的第2项,第9项和第44项,这三个数的和为
- 梁启超说:“史者何?记述人类社会赓续活动之体相,校其总成绩,求得因果关系,以为现代一般人活动之资鉴者也。”在这里,梁启超



