碳族元素简介 知识点题库
-
(1)
- 溶于海水的CO2主要以4种无机碳形式存在,其中HCO3-占95%,写出CO2溶于水产生HCO3-的方程式:
-
(2)
- 在海洋循环中,通过下图所示的途径固碳。
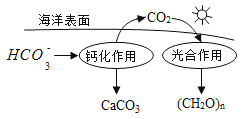
- ①写出钙化作用的离子方程式: .
②同位素示踪法证实光合作用释放出的O2只来自于H2O,用18O标记物质的光合作用的化学方程
式如下,将其补充完整: + =(CH2O)x+x18O2+xH2O
-
(3)
- 海水中溶解无机碳占海水总碳的95%以上,其准确测量是研究海洋碳循环的基础,测量溶解无机碳,可采用如下方法:
- ①气提、吸收CO2 , 用N2从酸化后的还说中吹出CO2并用碱液吸收(装置示意图如下),将虚线框中的装置补充完整并标出所用试剂。
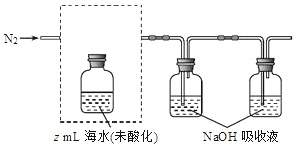
- ②滴定。将吸收液洗后的无机碳转化为NaHCO3 , 再用xmol/LHCl溶液滴定,消耗ymlHCl溶液,海水中溶解无机碳的浓度= mol/L。
-
(4)
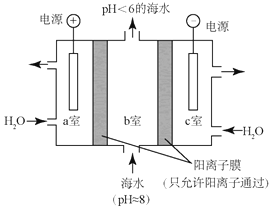
- 利用右图所示装置从海水中提取CO2 , 有利于减少环境温室气体含量。
- ①结合方程式简述提取CO2的原理: 。
②用该装置产生的物质处理b室排出的海水,合格后排回大海。处理至合格的方法是 。
(2)我国古代炼丹中经常使用到红丹,俗称铅丹.在一定条件下铅丹(用X表示)与硝酸能发生如下反应:X+4HNO3═PbO2+2Pb(NO3)2+2H2O.铅丹的化学式是 ,此铅丹中铅的化合价是 .由此反应可推测PbO是(填“酸”或“碱”) 性氧化物.
(3)砷酸钠在酸性条件下跟碘化钾溶液反应生成亚砷酸钠(Na3AsO3)、碘单质和水的离子反应方程式是 ,上述反应中电子转移数目是
 B .
B . 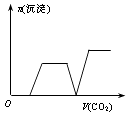 C .
C . 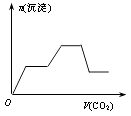 D .
D . 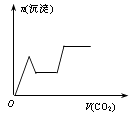
选项 | 实验操作 | 实验现象 | 结论 |
A | 向1mL2mol/LNaOH溶液中先滴加2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/LFeCl3溶液 | 先生成白色沉淀,后生成红褐色沉淀 | Ksp[Fe(OH)3]<Ksp[Mg(OH)2] |
B | 向NH3·H2O溶液中滴加少量AgNO3溶液 | 无明显现象 | NH3·H2O和AgNO3不反应 |
C | 将木炭和浓硫酸共热生成的气体通入澄清石灰水中 | 澄清石灰水变浑浊 | 该气体只含CO2 |
D | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀产生 | 该溶液中可能含有SO42- |
①饱和Na2CO3溶液 ②澄清石灰水 ③BaCl2溶液 ④K2SiO3溶液 ⑤NaAlO2溶液
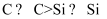 、
、 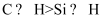 ,因此C2H6稳定性大于Si2H6
B . 立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度
C . SiH4中Si的化合价为+4,CH4中C的化合价为-4,因此SiH4还原性小于CH4
D . Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成
,因此C2H6稳定性大于Si2H6
B . 立方型SiC是与金刚石成键、结构均相似的共价晶体,因此具有很高的硬度
C . SiH4中Si的化合价为+4,CH4中C的化合价为-4,因此SiH4还原性小于CH4
D . Si原子间难形成双键而C原子间可以,是因为Si的原子半径大于C,难形成 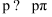 键
键
选项 | 陈述I | 陈述II |
A | “墨子”传信——用光导纤维传输量子光信号 | SiO2的导电能力强 |
B | “天问”飞天——用液氧液氢作推进剂 | 液氧、液氢均为纯净物 |
C | “天眼”探空——用钢索建成索网 | 合金钢比纯铁熔点高、硬度小 |
D | “蛟龙”入海——用蓄电池组提供能量 | 蓄电池组工作时可将化学能转化为电能 |
 与
与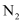 互为等电子体,具有相同的化学键特征,具有相同的化学性质
B . 碳、氮、氧三种元素对应的简单氢化物都可以作为配合物的配体
C . 碳、氮、氧三种元素对应的简单氢化物中中心原子的杂化方式都是
互为等电子体,具有相同的化学键特征,具有相同的化学性质
B . 碳、氮、氧三种元素对应的简单氢化物都可以作为配合物的配体
C . 碳、氮、氧三种元素对应的简单氢化物中中心原子的杂化方式都是 D .
D .  三种离子的
三种离子的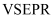 模型相同,离子立体构型相同
模型相同,离子立体构型相同
- 阅读下面的材料,完成后面的题。(12分) 材料一:今年6月5日是第42个世界环境日,联合国环境规划署确定今年的主题
- 2008年1月8日,中共中央、国务院在北京隆重举行国家科学技术奖励大会,授予闵恩泽、吴征镒两位院士2007年度国家科学技
- 9.北京大学曾是新文化运动的摇篮,蔡元培任北大校长期间,在办学上采取“兼容并包”的方针,在当时的主要目的是 A.吸引外来
- (10分)一颗人造卫星的质量为m,离地面的高度为h,卫星做匀速圆周运动,已知地球半径为R,地球表面重力加速度为g,求:(
- 实验室制取氢气,最好选用的试剂是 ( ) A.锌与浓硫酸 B.锌与稀硫酸 C.铁与稀硝酸 D.镁与浓盐酸
- 下列图形中,由,能得到的是
- 将二次函数化为的形式,则 .
- — How was your weekend? — It was ________. I had lots of fu
- (三)文言文阅读大脖子病人南岐在秦蜀①山谷中,其水甘而不良,凡饮之者辄病瘿②,故其地之民无一人无瘿者。及见外人至,则群小
- 已知数列是等比数列,且,,,则 .
- 鉴定一个正在进行有丝分裂的细胞是植物细胞还是动物细胞,最可靠的方法是检查 A.DNA的复制方式
- “航天员在飞天过程中为了维持太空舱里氧气的含量,可以利用镍铁氧体(NiFe2O4)作为催化剂,将呼出的二氧化碳转化为氧气
- 科学家采用“组合转化”技术,可将二氧化碳在一定条件下转化为重要的化工原料乙烯,其反应的微观过程如下图所示。下列说法不正确
- 下图是1785年的广州十三行,是清政府唯一特许经营管理对外贸易的机构。此种情况反映了清朝()A.实行“闭关锁国”政策
- 选择划线字注音正确的一项。(1)确凿 A.záo B.zuò C.zòu D.ziáo (2)桑葚 A.rèn B.sè
- 下图表示果实的形成,图中①、②、③、④分别为A.子房、胚、果实、受精卵 B.子房、胚珠、果皮、种子 C.胚珠、受精卵、果
- 英国著名的经济学家K·E·博尔丁提出了两种不同的经济模式,分别比喻为“牧童经济”,和“宇宙飞船经济”。 “牧童经济”使人
- 列实验过程中产生的现象与对应的图形相符合的是( )A.NaHSO3粉末加入HNO3溶液中 B.H2S
- 阅读下文,完成12-15题(12分) 黄帝将见大隗①乎具茨②之山,适遇牧马童子,问涂③焉,曰:“若知具茨之山乎?
- (08年绵阳市诊断三理)(12分)为坐标原点,和两点分别在射线≥上移动,且,动点满足,记点的轨迹为。(1)求的值;(2)



