探究卤素单质间的置换反应 知识点题库
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.图2中,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红色石蕊试纸.(已知常温下浓盐酸与高锰酸钾能反应生成氯气)
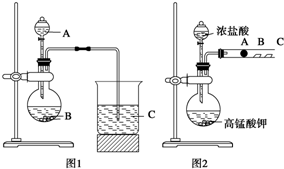
(1)甲同学实验中选用的物质化学式为:A ,B , C ;
(2)写出甲同学的实验中C处反应的离子方程式为 ,乙同学的实验中圆底烧瓶中发生反应的化学方程式为 ,B处的实验现象为 .
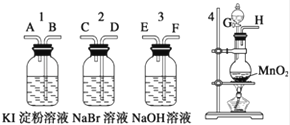
为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2 , 并将Cl2依次通入NaBr溶液和淀粉KI溶液中.有如图所示的仪器(橡胶塞均为双孔)及药品,试回答:
(1)若所制气体从左向右流向时,上述仪器接口的连接顺序为H接 、 接 、 接 .
(2)装置3的作用是 ,反应的离子方程式为 .
(3)装置1中产生的现象是 ,反应的化学方程式为 .
(4)通过本实验可得到的结论是 .
为验证卤素单质氧化性的相对强弱,某小组用图所示装置进行实验(夹持仪器已略去,气密性已检验).
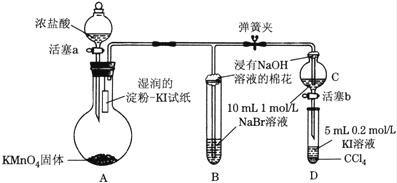
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ…
(1)验证氯气的氧化性强于碘的实验现象是 .
(2)B中溶液发生反应的离子方程式是 .
(3)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 .
(4)过程Ⅲ实验的目的是 .
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下随着核电荷数的增加, 的增多, 逐渐增大, 逐渐减弱,得电子能力逐渐减弱.
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性:Fe3+>Br2 , 故上述实验现象不是发生化学反应所致.则溶液呈黄色是含 (填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+ , 故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致.
(3)设计实验并验证:
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.供选用的试剂:
a.酚酞试液 b.四氯化碳 c.无水酒精 d.硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象.(试剂填序号)
选用试剂 | 实 验 现 象 | |
方案1 |
|
|
方案2 |
|
|
(4)应用与拓展:
①在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为 .
②在100mL FeBr2溶液中通入2.24LCl2(标准状况),溶液中有1/3的Br﹣被氧化成单质Br2 , 则原FeBr2溶液中FeBr2的物质的量浓度为 .
③若选用淀粉﹣碘化钾溶液验证上述猜想,是否可行? (填“是”或“否”),理由是 .
实验名称:ⅦA单质氧化性强弱比较
实验药品:NaBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸
实验设计:
实验步骤 | 实验结论 |
①氯水+1mLCCl4 , 振荡、静置, 观察四氯化碳层颜色 | 氧化性从强到弱的 顺序: Cl2>Br2>I2 |
②NaBr溶液+氯水+1mLCCl4 , 振荡、静置,观察四氯化碳层颜色 | |
③KI溶液+氯水+1mLCCl4 , 振荡、静置,观察四氯化碳层颜色 |
试回答:
(1)完成该实验所用到得实验仪器是 .
(2)CCl4在实验中所起的作用是 .
(3)该同学的实验设计不足之处是 ,改进的办法是 .
已知:①溴水为溴的水溶液,溴水为橙黄色,溴蒸气为红棕色,均有毒
②氯水为氯气的水溶液。
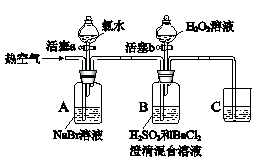
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为橙黄色 |
Ⅱ | 吹入热空气 | A中橙黄色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成橙黄色 |
请回答下列问题:
-
(1) A中反应的离子方程式是。
-
(2) 实验操作II吹入热空气的目的是。
-
(3) 装置C的作用是。
-
(4) 实验操作III,混合液逐渐变成橙黄色,其对应的离子方程式是。
-
(5) 由操作I得出的结论是,由操作III得出的结论是。
-
(6) 实验反思:实验操作III,开始时颜色无明显变化的原因是(写出一条即可):。
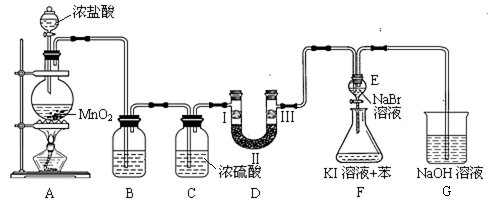
-
(1) 装置 B 中饱和食盐水的作用是。
-
(2) 装置 D 的作用是验证氯气是否具有漂白性,为此 D 中Ⅰ、Ⅱ、Ⅲ 处依次放入物质的组合应是(填字母编号)。
编号
Ⅰ
Ⅱ
Ⅲ
a
干燥的有色布条
碱石灰
湿润的有色布条
b
干燥的有色布条
无水氯化钙
湿润的有色布条
c
湿润的有色布条
碱石灰
干燥的有色布条
d
湿润的有色布条
无水氯化钙
干燥的有色布条
-
(3) 设计装置 F 的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开 E 中活塞,将装置 E 中少量溶液加入装置 F 中,振荡,观察到的现象是 ,该现象(填“能”或“不能”)说明溴单质的氧化性强于碘单质,原因是。
-
(4) 实验室也可以用高锰酸钾和浓盐酸反应来制备氯气,反应的化学方程式为:
2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
①在化学方程式上用双线桥法标出该反应中电子转移的方向和数目 。
②在该反应中,氧化剂是。
③上述反应中,有126. 4 g 的 KMnO4 参加反应,若将生成的氯气全部通入足量的石灰乳中,理论上可得到次氯酸钙多少克?
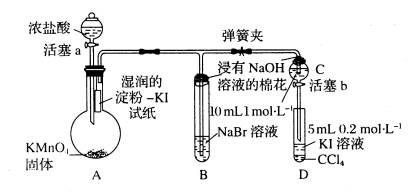
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为红棕色时,关闭活塞a。
IV.……
-
(1) A中产生黄绿色气体的化学反应方程式是。
-
(2) 验证氯气的氧化性强于碘的实验现象是。
-
(3) B中溶液发生反应的离子方程式是。
-
(4) 为验证溴的氧化性强于碘,过程Ⅳ的操作是,现象是。
-
(5) 过程III实验的目的是。
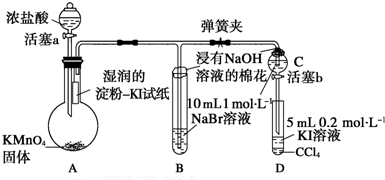
实验过程:
Ⅰ. 打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ. 当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ. 当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
-
(1) A中产生黄绿色气体,其电子式是。
-
(2) 验证氯气的氧化性强于碘的实验现象是。
-
(3) B中溶液发生反应的离子方程式是。
-
(4) 为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是。
-
(5) 过程Ⅲ实验的目的是。
-
(6) 氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,得电子能力逐渐减弱。
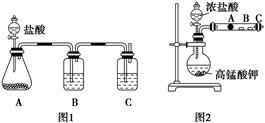
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
-
(1) 甲同学设计实验的依据是强酸制弱酸,请回答下列问题
A中锥形瓶装入的是碳酸钙固体,A中发生的离子方程式为:,
B应放入的物质是,其作用为;
C中是Na2SiO3溶液该反应的离子方程式为。
-
(2) 乙同学的实验原理是强氧化剂生成弱氧化剂。
如果A处的棉花由白色变成棕色,则A处的离子方程式为B处的现象是 。
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 酸性:HCl>H2S | 非金属性:Cl>S |
| B | 铁表面镀锌可以增强其抗腐蚀性 | 构成原电池且铁作负极 |
| C | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| D | 向NaI溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈紫红色 | I-还原性强于Cl- |
-
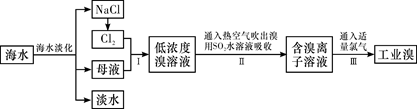
(1) 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序正确的是__________。A . NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 B . BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸 C . NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸 D . Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
-
(2) 步骤Ⅰ中已获得Br2 , 步骤Ⅱ中又将Br2还原为Br- , 其目的是。写出步骤Ⅱ中发生反应的离子方程式:。
-
(3) 制备钠单质的方法之一是将熔融NaCl进行电解,写出电解化学方程式:。
-
(4) 已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中的Cl-、Br-、I-的物质的量之比变成4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的_____。(填选项)A .
 B .
B .  C .
C . 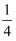 D .
D . 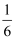
-
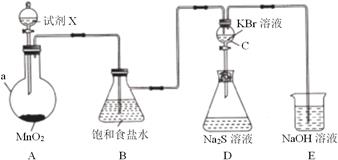
(1) 仪器a的名称是。试剂X 是。
-
(2) 写出装置A中发生反应的化学方程式。
-
(3) 装置E中NaOH溶液的作用是。
-
(4) 反应一段时间后,观察到装置C中溶液变为橙黄色,说明非金属性:ClBr( 填“>"或"<")。
-
(5) 打开装置C中的活塞,将装置C中的溶液逐渐滴人装置D中,振荡。观察到的现象是,写出可能发生反应的离子方程式:(写一个即可),根据此现象不一定能说明溴的非金属性比硫强,原因是。
下列说法错误的是( )
-
(1) I.将钠、镁各2 g分别投入盛足量冷水的烧杯中,实验结果:与冷水剧烈反应;另取镁、铝各2 g 分别投入足量0.05 mol/L盐酸中,与盐酸反应最剧烈。
-
(2) 向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明元素得电子能力>,反应的离子方程式为。
实验结论:随原子序数增大,同周期元素失电子能力依次(填“增强”或“减弱”,下同),得电子能力依次。
-
(3) II.利用如图装置可验证同主族元素非金属性的变化规律。
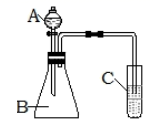
仪器A的名称为。
-
(4) 若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4.反应一段时间后,将C振荡、静置,观察到C中现象是。此装置存在的不足之处是。
选项 | 实验 | 现象 | 结论 |
A | 向 | 产生白色沉淀,且有无色气体生成 | 溶液中 |
B | 检验某无色溶液中是否含有 | 溶液变黄色且试管上部产生红棕色气体 | 该溶液中含有 |
C | 将铜粉放入稀硫酸溶液中并不断通入 | 铜粉快速溶解,溶液变为蓝色 | 形成 |
D | 向某钾盐中滴加浓盐酸,产生的气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为 |
- 在如图所示的电路中,E为电源电动势,r为电源内阻,R1和R3 均为定值电阻,R2为滑动变阻器。当R2的滑动触点在a端时合
- 第三节 完形填空(共20小题;每小题1.5分,满分30分) 阅读下面短文,从短文后所给各题的四个选项(A、B、C和D)中
- 某位启蒙思想家说:“立法权是国家的心脏,行政权是国家的大脑,大脑使各个部分运动起。大脑可能陷于麻痹,而人依然活着。一个人
- 艾瑞咨询公布的统计数据显示,2011年上半年,中国网络购物用户规模达到1.48亿,在网民中的渗透率达30.8%。伴随互联
- 已知,点(m,-1)与点(-2,n+1)是关于原点对称,则( ) A、m=-2,n=1 B、m=2,n=0 C
- .阅读材料,完成下列问题。 材料一:长江中下游部分省市分布图材料二:洞庭湖年输沙量和洞庭湖面积与容积的演变(资料来源:长
- 右图是A、B、C三种固体物质的溶解度曲线,请根据曲线回答:⑴t2℃时,将三种物质分别溶于100g水中制成饱和溶液,(此时
- —Weneed three single rooms for the first week in June. —____
- 如图8-8-5所示,摆的质量M=2.98 kg,摆线长 1 m,子弹的质量是20 g,以210 m/s的水平速度射入摆中
- 标有“6V 1.5W”的小灯泡,通过它的电流随两端电压变化的关系如图10所示,若把这样的三只灯泡串联起来,接在12V的
- 明清之际三位进步思想家的思想实质是儒家思想在新的历史条件下的活跃,他们使儒家更趋实事求是,与国计民生靠得更近,由此形成什
- 可用于判断碳酸氢钠粉末中是否混有碳酸钠的实验方法是( ) A.溶于水后滴加氯化钡稀溶液,观察有无白色沉淀生成 B.
- 在减数分裂的整个过程中,细胞分裂次数、染色体复制次数、着丝点分裂次数、DNA分子减半次数是
- 32. —Will it take me long to get to the Sunshine Hotel?
- 我国唐朝创制且闻名于世的陶器艺术珍品是( ) A.唐三彩B.青瓷 C.白瓷 D.青花瓷
- 维生素C主要存在于蔬菜、水果中,它能增加人体对疾病的抵抗能力。其结构简式为 请回答: (1)维生素C的分子式是
- 下列关于溶液的叙述正确的是 A.溶液一定是均一、稳定、无色、透明的液体 B.溶液中各部分性质相同 C.某物质的
- 财政教育经费投入不足,是长期以来制约我国教育事业发展的一个重要因素。面对这一问题,假如你是人大代表,可以 A.行使立法权
- “a>0且b>0”是“a+b≥2”成立的( ) A.充分不必要条件 B
- good picture! Who painted it? A. How B.What C. Ho
 溶液中滴入
溶液中滴入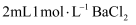 溶液
溶液 部分电离出
部分电离出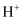 和
和 ,
,  与
与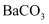 沉淀,促进了
沉淀,促进了 的电离,使
的电离,使
 , 取少量该溶液于试管中,加稀盐酸酸化,再加入
, 取少量该溶液于试管中,加稀盐酸酸化,再加入 溶液
溶液 , 再在溶液中滴加少量
, 再在溶液中滴加少量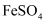 溶液
溶液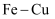 原电池,加快反应速率
原电池,加快反应速率 或
或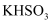 或者二者混合物
或者二者混合物


