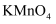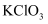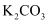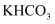化学实验操作的先后顺序 知识点题库
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
-
(1)
- 验证假设一
- 该小组设计实验验证了假设一,请在下表空白处填写相关实验现象
实验步骤
实验现象
结论
实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体
假设一成立
实验2:在盛有不含O2的25ml0.1mol/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体
-
(2)
为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如下图
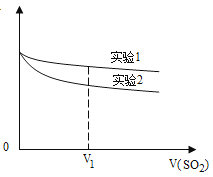
实验1中溶液pH变小的原因是 V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示) 。
-
(3) 验证假设二
请设计实验验证假设二,写出实验步骤,预期现象和结论。
实验步骤、预期现象和结论(不要求写具体操作过程)
-
(4) 若假设二成立,请预测:在相同条件下,分别通入足量的O2和KNO3 , 氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反应后两溶液的pH前者 (填大于或小于)后者,理由是 。
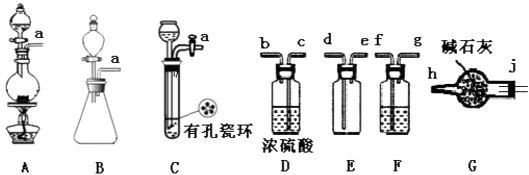
-
(1) 制备Cl2发生装置可以选用(填写字母代号),请写出发生反应的离子方程式:。
-
(2) 欲收集一瓶干燥的氯气,选择装置,其连接顺序为:a→(按气流方向,用小写字母表示)。
-
(3) 实验室可用下图装置制备亚硝酰氯(ClNO):
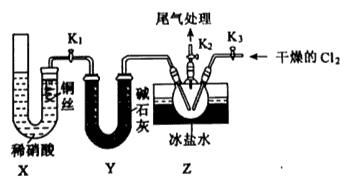
①实验室也可用B装置制备NO,X装置的优点为。
②检验装置气密性并装入药品,打开K2 , 然后再打开K1 , 通入一段时间气体,其目的为,然后进行其他操作,当Z有一定量液体生成时,停止实验。
③若无装置Y,则Z中ClNO可能发生反应的化学方程式为。
-
(4) 取Z中所得液体mg溶于水,配制成250mL溶液,取出25.00mL,以K2CrO4溶液为指示剂,用cmol•L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为22.50mL。则亚硝酰氯(ClNO)的质量分数为(用代数式表示)。[已知:Ag2CrO4为砖红色固体;Ksp(AgCl)=1.56×10-10 , Ksp(K2CrO4)=1×10-12]
-
(1) 从草木灰中提取钾盐的实验操作顺序如下:①称量样品,②溶解沉降,③,④,⑤冷却结晶。
-
(2) 用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示________(填字母)。A . 左盘重,样品轻 B . 左盘轻,砝码重 C . 右盘重,砝码轻 D . 右盘轻,样品重
-
(3) 在进行②③④操作时,都要用到玻璃棒,其作用分别是:②;③;④。
-
(4) 将制得的少量晶体放入试管,加蒸馏水溶解并把溶液分成三份,分装在3支试管里。
①在第一支试管里加入稀盐酸,可观察有生成,证明溶液中有离子。
②在第二支试管里加入足量稀盐酸后,再加入BaCl2溶液,可观察到有生成,证明溶液中有离子。
③在第三支试管里加入足量Ba(NO3)2溶液,过滤后,再向滤液中加入足量稀硝酸后,再加入AgNO3溶液,可观察到有生成,证明溶液中有离子。
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将过量的CO2通入CaCl2溶液中 | 无白色沉淀出现 | 生成的Ca(HCO3)2可溶于水 |
| B | 常温下将铁片插入浓硫酸中 | 无明显现象 | 铁片和浓硫酸不反应 |
| C | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| D | 向澄清石灰水加入某试剂的溶液少许 | 产生白色沉淀 | 该试剂中一定含有CO32— |
(方案1)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
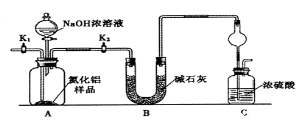
-
(1) 如图C装置中球形干燥管的作用是。
-
(2) 完成以下实验步骤:组装好实验装置,首先;再加入实验药品。接下来的实验操作是,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1 , 通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是。
-
(3) 由于装置存在缺陷,导致测定结果偏高,请提出改进意见。
-
(4) (方案2)用如下图装置测定m g样品中AlN的纯度(部分夹持装置已略去)。
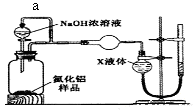
导管a的主要作用是。
-
(5) 为测定生成气体的体积,量气装置中的X液体可以是。(填选项序号)
a.CCl4 b.H2O c.NH4Cl溶液 d.

-
(6) 若mg样品完全反应,测得生成气体的体积为VmL,(已转换为标准状况),则AlN的质量分数为(用含V、m的代数式表示)。
 不参与反应
不参与反应  按体积比1:3混合通入含水
按体积比1:3混合通入含水 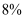 的碳酸钠中制备Cl2O(同时生成一种使澄清石灰水变浑浊的气体和一种盐),并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。(Cl2在CCl4中的溶解度较大)
的碳酸钠中制备Cl2O(同时生成一种使澄清石灰水变浑浊的气体和一种盐),并用水吸收Cl2O(不含Cl2)制备次氯酸溶液。(Cl2在CCl4中的溶解度较大) 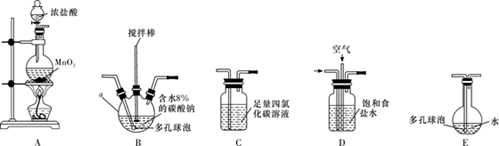
-
(1) 各装置的连接顺序为
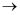
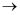
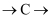 。
。
-
(2) 装置B中多孔球泡和搅拌棒的作用是;装置C的作用是。
-
(3) B中的化学方程式为。
-
(4) 反应过程中,装置B需放在冷水中,其目的是。
-
(1) 甲组做金属钠在空气中燃烧实验。实验室取用金属钠的方法是。
-
(2) 金属钠燃烧时会生成黑色固体,黑色固体的可能来源是、。
-
(3) 某同学想用金属钠和空气制备纯度较高的Na2O2(不考虑空气中的N2),可利用的装置如图。
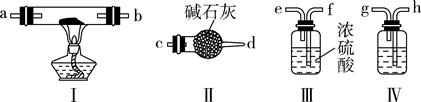
①装置Ⅳ中盛放的药品是,若没有该装置可能导致生成的Na2O2中含有,其反应的化学方程式为。
②若规定气流的方向为从左到右,各仪器连接的顺序是空气进入,接,接,接。(填字母)
③装置Ⅱ的作用是。
 制取、收集、吸收,以及
制取、收集、吸收,以及  的还原性探究进行了如下实验设计。
的还原性探究进行了如下实验设计。
-
(1) I.
 的收集和吸收
的收集和吸收 若用图甲装置,排空气法收集
 ,气体应从口进入(选填“A”或“B)。
,气体应从口进入(选填“A”或“B)。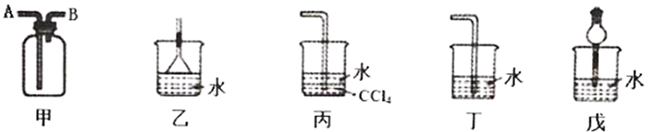
-
(2) 已知
 难溶于
难溶于  。图乙、丙、丁、戊四种装置中,不能用来吸收
。图乙、丙、丁、戊四种装置中,不能用来吸收  的是。
的是。
-
(3) II.
 的还原性探究利用下列装置,进行
的还原性探究利用下列装置,进行  还原
还原  的反应。
的反应。 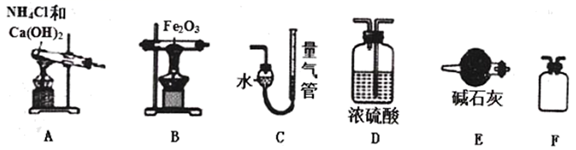
已知:
 与
与  反应的生成物为
反应的生成物为  和难溶于水的气体X,且X不被浓硫酸和碱石灰吸收。
和难溶于水的气体X,且X不被浓硫酸和碱石灰吸收。写出A装置发生反应的化学方程式。
-
(4) 按气流方向正确的装置连接顺序为A→→→→→C(填序号,每个装置只用一次)。
-
(5) 实验结束时,应首先(填序号)。
①熄灭A装置的酒精灯 ②熄灭B装置的酒精灯
-
(6) 若称取1.6克
 完全反应后,测得生成气体X的体积为
完全反应后,测得生成气体X的体积为 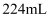 (已折算为标准状况),通过计算推测B中
(已折算为标准状况),通过计算推测B中  与
与  反应的化学方程式为。
反应的化学方程式为。
已知:①无水四氯化锡的熔点-33℃、沸点114.1℃;②四氯化锡易水解,易溶于有机溶剂。下列说法正确的是( )
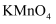 晶体,流程如下:
晶体,流程如下:

已知:①

②
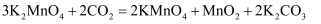
③
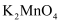 在中性或酸性介质中不稳定,快速发生歧化反应
在中性或酸性介质中不稳定,快速发生歧化反应
④部分物质的溶解性表:
| 温度 溶解度 物质 |
0℃ |
20℃ |
40℃ |
60℃ |
80℃ |
100℃ |
|
|
2.83g |
6.34g |
12.6g |
22.1g |
||
|
|
3.3g |
7.3g |
13.9g |
23.8g |
37.5g |
56.3g |
|
|
105g |
111g |
117g |
127g |
140g |
156g |
|
|
22.5g |
33.7g |
47.5g |
65.6g |
-
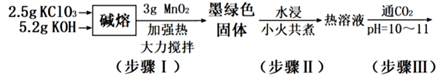
(1) 步骤I实验中所用坩埚是铁坩埚而不用瓷坩埚的原因是:
碱熔氧化过程,KOH的用量要过量,其目的是:
-
(2) 下列说法错误的是:___________A . 步骤I中,
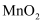 应分批加入,以提高原料利用率;过程中还需用铁棒不断搅拌,以防结块
B . 步骤III中,为使得
应分批加入,以提高原料利用率;过程中还需用铁棒不断搅拌,以防结块
B . 步骤III中,为使得
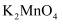 充分歧化,所通入
充分歧化,所通入
 最宜过量至溶液呈弱酸性
C . 步骤III中,为验证
最宜过量至溶液呈弱酸性
C . 步骤III中,为验证
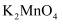 已经完全歧化,可用玻璃棒蘸取溶液于滤纸上,观察滤纸上是否有绿色痕迹
D . 步骤IV中,抽滤时为防止滤纸破损,可选择用双层普通滤纸或直接用砂芯漏斗
E . 步骤V中,经一系列操作获得的
已经完全歧化,可用玻璃棒蘸取溶液于滤纸上,观察滤纸上是否有绿色痕迹
D . 步骤IV中,抽滤时为防止滤纸破损,可选择用双层普通滤纸或直接用砂芯漏斗
E . 步骤V中,经一系列操作获得的
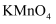 晶体常出现结块现象,应用研钵充分研磨后再密封保存
晶体常出现结块现象,应用研钵充分研磨后再密封保存
-
(3) 步骤V中为获得
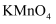 晶体,从下列选选项中选出合理的操作并排序:将滤液转移至蒸发皿中→→→→→干燥。
晶体,从下列选选项中选出合理的操作并排序:将滤液转移至蒸发皿中→→→→→干燥。
a.用少量冰水洗涤
b.先用冰水洗涤,再用乙醇洗涤c.蒸发溶剂至析出大量晶体,趁热过滤
d.缓慢降温结晶
e.减压过滤f.蒸发溶剂至溶液表面析出晶膜
-
(4) 产品纯度分析:取mg所得晶体,溶于水并加入酸酸化,定容至100mL。取25mL溶液于锥形瓶中,用
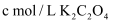 标准溶液进行滴定,消耗标准溶液VmL。
标准溶液进行滴定,消耗标准溶液VmL。
①酸化
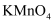 溶液可用代替稀硫酸
溶液可用代替稀硫酸②所得晶体的纯度为:(填写数学表达式,要求化简)
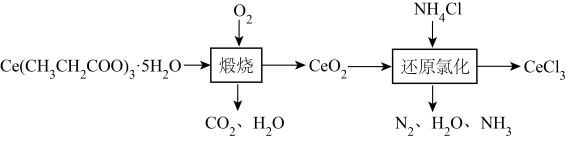
回答下列问题:
-
(1) “煅烧”时,生成CO2和H2O的物质的量之比为。
-
(2) 该小组欲用如图装置验证“煅烧”步骤的气体产物。

①按气流方向,上述装置的连接顺序为(填仪器接口的字母编号),试剂X为。
②该实验中需采用3.00mol•L-1H2O2溶液。欲配制100mL3.00mol·L-1H2O2溶液,需要量取溶质质量分数为34%的H2O2溶液(密度为1.13g·mL-1)的体积为mL(保留两位小数),量取34%的H2O2溶液时所使用的仪器为。
③装置D中石棉的作用为。
-
(3) “还原氯化”时,需要在加热条件下进行,该反应的化学方程式为。
-
(4) “还原氯化”时,加入过量的NH4Cl可有效抑制CeCl3的水解,解释其原因为。
已知:
苯胺 | 乙酸酐 | 冰醋酸 | 乙酰苯胺 |
沸点184℃,稍溶于水,易被氧化而变色。相对分子质量为93 | 沸点139℃,相对分子质量为102 | 沸点117.9℃,相对分子质量为60 | 无色晶体,沸点304℃,难溶于冷水,易溶于乙醇等有机溶剂。相对分子质量为135 |
(一)粗乙酰苯胺的制备
原理: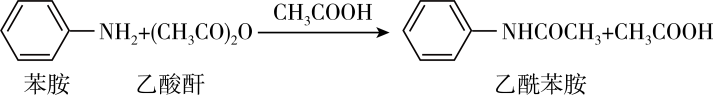
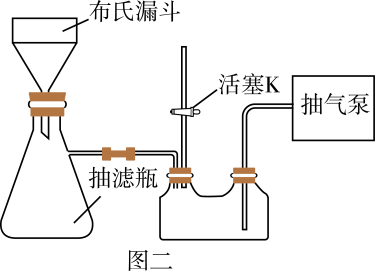
实验装置:如图一所示(夹持装置略)。
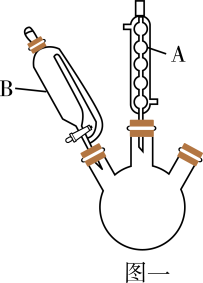
实验步骤:将35mL(38g)乙酸酐、37mL(39g)冰醋酸放入三颈烧瓶中,在B中放入25mL(25.5g)苯胺,逐滴滴加到三颈烧瓶中,边滴边振荡,滴加完毕小火加热30min。在搅拌下,趁热把反应混合物慢慢倒入500mL冷水中,析出固体。将混合物抽滤得到乙酰苯胺粗品。
(二)乙酰苯胺的提纯
①将粗乙酰苯胺晶体移入盛有500mL热水的烧杯中,加热至沸,使之溶解。
②稍冷后,加入适量粉末状活性炭,充分搅拌后趁热进行抽滤。
③将滤液转移到干净烧杯中,冷却、抽滤,用少量冷水洗涤、抽滤。
④将产物放在干净的表面皿中晾干、称重,质量为22.5g。
回答下列问题:
-
(1) 图一中装置A的名称是,其作用为。
-
(2) 本实验所用三颈烧瓶的适宜规格为____mL(填标号)。A . 100 B . 250 C . 500
-
(3) 制备粗品过程中将反应混合物倒入冷水中,目的是。
-
(4) “提纯”步骤②中加入活性炭的作用是。
-
(5) 用图二装置进行“提纯”步骤③中的抽滤和洗涤过程。请按正确的操作顺序补充完整(只进行一次洗涤操作):打开抽气泵→转移混合物至布氏漏斗→关闭活塞K→确认抽干→打开活塞K→→→确认抽干→打开活塞K→关闭抽气泵。本实验多次用到抽滤操作,其优点是。
-
(6) 本实验的产率为%(保留三位有效数字)。若要得到纯度更高的乙酰苯胺晶体,用于提纯的方法为。
-
(1) I.联氨制备(夹持及加热装置已省略):
①氯气和氨气在丙酮中生成丙酮联氮[(CH3)2C=NN=C(CH3)2]且有白烟生成。
②丙酮联氮水解可得到丙酮和水合肼(N2H4•H2O)。
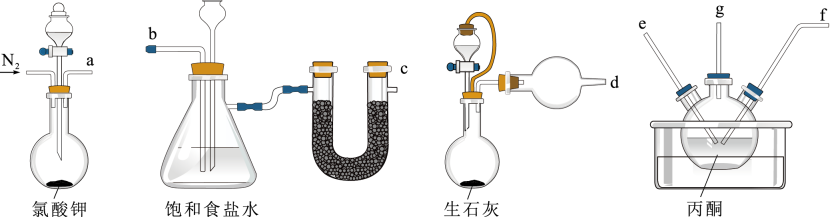
按照接口顺序a→ → → → ←d进行实验,反应前先通入一段时间的氮气排出空气,丙酮中生成丙酮联氮的化学方程式为。
-
(2) 盛放丙酮溶液的仪器名称为,饱和食盐水中长颈漏斗的作用是;反应过程中要控制氯气的通入量不能过量的原因是。
-
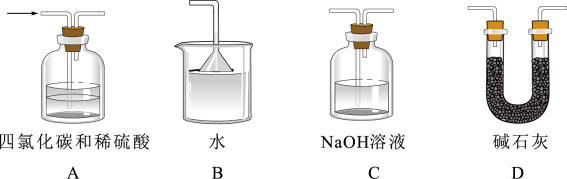
(3) 装置存在明显缺陷,g后所接装置图可以是(填标号)。
-
(4) II.产品纯度测定:
量取水解液50.0mL加水调至弱碱性,配成250mL溶液,移出25.00mL,再加入足量AgNO3溶液;充分反应后,过滤、洗涤、干燥、称量,得固体质量为0.216g。则水解液中肼的含量为g•L-1。
 与金属钠在高温下反应生成纳米石墨,设计如下装置:
与金属钠在高温下反应生成纳米石墨,设计如下装置: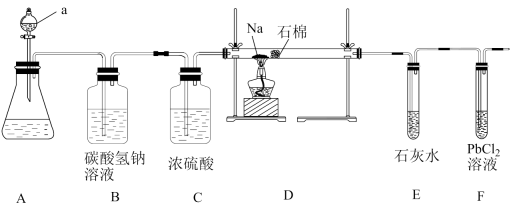
回答下列问题
-
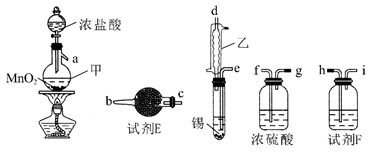
(1) 装置A中的a的仪器名称为。
-
(2) 实验时,在点燃酒精灯前必须进行的操作是。
-
(3) 装置E中出现现象时,再点燃酒精灯,以上操作的目的是。
-
(4) 待装置D加热一段时间后观察到钠块表面变黑,继续加热后,钠燃烧,有白烟生成。取残留固体溶于水,发现有黑色的不溶颗粒存在;取上层液体与过量的
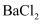 溶液反应发现有白色沉淀生成,根据以上信息,写出装置D中的反应方程式。
溶液反应发现有白色沉淀生成,根据以上信息,写出装置D中的反应方程式。
-
(5) 装置F中的
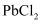 溶液吸收CO变黑色,可以处理产生的尾气,试用反应方程式分析CO产生的原因。
溶液吸收CO变黑色,可以处理产生的尾气,试用反应方程式分析CO产生的原因。
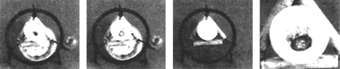
- 如图所示,用高压放电的电火花产生一个冲击波,再用椭球形凹面镜使声波反射后集中到胆结石上,就能使胆结石粉碎.这一现象主要说
- 下列句子中,没有语病的一句是( ) A.考古学家在清理墓穴时,搜集到大理石制工具,其中有砍刀器、石核等用石英沙岩打制而成
- 下图是中学教材中元素周期表的一部分,其中标出A-Q14种元素,试回答下列问题:[(1) (2)问用具体的元素符号或离子符
- Smoking is ________ in all areas of the office building.
- 固定在竖直平面的光滑圆弧轨道ABCD。其A点与圆心等高,D点为轨道最高点,DB为竖直直线,AC为水平线,AE为水平面。
- (12分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,右图是从铝土矿中制备铝的工艺流程:已知:铝土矿的主要成分
- 请根据下列两小题中预设的有关情景及要求,任选一题,设计一个“拒绝词”。 (1)有一位同学想在下午的上课时间到书店买一本重
- _____from the moon ,our earth with water ____70% of its surf
- 道尔顿的原子学说曾经起了很大作用,他的学说中,包括有下述三个论点,以现代的观点看,其中不确切的是( ) ①原子是不
- Let’s play computer games. _______.A.That sounds goodB.Let’s
- 若P(2,-1)为圆C:(x-1)2+y2=25的弦AB的中点,则直线AB的方程是() A.2x-y-5=0
- 分析表格数据,回答1~3题。 最冷月均温最热月均温年降水量东京(370N)3.70C25.10C1610mm北京(390
- 用如图实验装置验证m1 、m2组成的系统机械能守恒。m2从高处由静止开始下落,m1上拖着的纸带打出一系列的点,对纸带上的
- 取铜、锌混合粉末,在空气中充分灼烧后,加入稀硫酸至固体恰好溶解,再加入一定量的铁粉,充分反应后过滤,得到滤渣和滤液,(1
- 下列属于影响人口迁移的拉力因素的是 A.生活困难质量低 B.工作机会多 C.公共设施不足
- 现有一对表现型正常的夫妇生了一个患克氏综合征并伴有色盲的男孩,该男孩的染色体组成为44+XXY。下列分析说明,错误的是(
- 图1-64中均质球的质量为m,各接触处均光滑,试根据球的重力对支持物所产生的作用效果确定分力的方向,画出力的平行四边形.
- 下列关于动摩擦因数的说法中,正确的是() A.物体越重,物体与水平支持面之间的动摩擦因数越大 B.物体在一支持面上滑动,
- 如图,AB为半圆O的直径,AB=4,C为半圆上一点,过点C作半圆的切线CD,过点A作AD⊥CD于D,交半圆于点E,DE=
- 下列选项中属于腐朽文化的是 ①愚昧、庸俗的文化 ②殖民文化 ③黄赌毒文化 ④民俗文化 A.①②