探究沉淀溶解 知识点题库
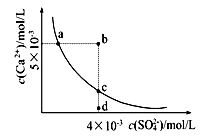
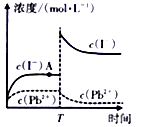
①CaSO4在稀硫酸中的溶解性比在纯水中的溶解性小
②a、c两点均可以表示CaSO4溶于水所形成的饱和溶液
③a点对应的Ksp不等于c点对应的Ksp
④b点对应的溶液将有沉淀生成
⑤向d点溶液加入适量CaCl2物体可以变到c点
⑥d点溶液通过蒸发溶剂可以变到c点
⑦常温下CaSO4溶于水的饱和溶液中,c(Ca2+)与c(SO42-)的乘积对应曲线上任意一点
⑧常温下,向100mL饱和CaSO4溶液中加入400mL0.01mol/LNa2SO4溶液,能使溶液由a点变为b点
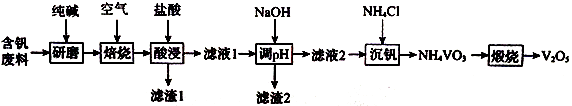
请回答下列问题;
-
(1) (研磨)的目的为。所加纯碱不宜过量太多,理由为。
-
(2) “焙烧”后所得混合物中除含Na2CO3、NaVO3、Fe2O3、NaAlO2外,还含有(填化学式)。
-
(3) “酸浸”时,VO3-转化为VO2+ , 转化反应的离子方程式为;滤渣1的主要成分为(填化学式)。
-
(4) 已知:常温下,Al(OH)3、Fe(OH)3 饱和溶液中金属阳离子浓度的负对数[-lg c(M3+ )]与pH 的关系如图所示:
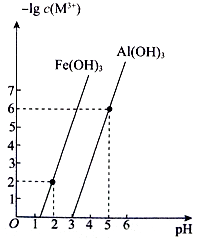
常温下,Ksp[Fe(OH)3]=;当调pH=4 时,溶液中Al3+(填“是”或“否”)沉淀完全。(已知;溶液中离子浓度小于等于10-5mol·L-1时,认为该离子沉淀完全)
-
(5) “煅烧”时,反应的化学方程式为。
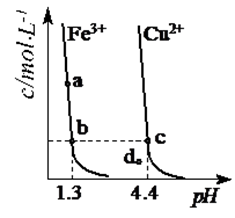
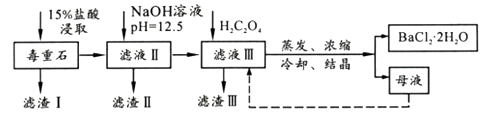
已知:①Ksp(BaC2O4)=1.6×10-7 , Ksp(CaC2O4)=2.3×10-9
②离子浓度小于至1×10-5认为沉淀完全。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.0 | 3.7 |
-
(1) 滤渣I的成分为(填化学式),过滤所需玻璃仪器有。
-
(2) 加入NaOH溶液后所得滤液III中,含有的Mg2+浓度为;加入H2C2O4时应避免过量,其原因是。
-
(3) BaCl2母液中除了含有Ba+、Cl-外,还含有大量的(填离子符号)。有人从“绿色化学”角度设想将“母液”沿虚线进行循环使用,请分析在实际工业生产中是否可行,(填“可行”或“不可行”),理由是。
-
(4) 滤渣III是结石的主要成分,现将滤渣III 经过洗涤干燥后在有氧环境下进行热重分析,取146.0g灼烧,所得参数如下表。
溫度(℃)
常温
190〜200
470〜480
质量(g)
146.0
128.0
100.0
滤渣III 的成分是(填化学式);200~470℃时发生反应的化学方程式为。
 =0.58)。下列分析错误的是( )
=0.58)。下列分析错误的是( )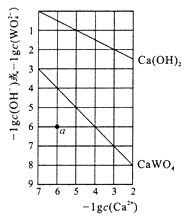
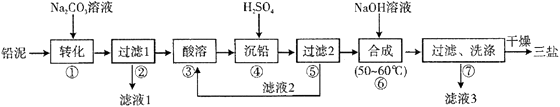
已知:Ksp(PbSO4)=1.82×10-8 , Ksp(PbCO3)=1.46×10-13;(2)铅与冷盐酸、冷硫酸几乎不起作用。请回答下列问题:
-
(1) 写出步骤①“转化”的化学方程式,该反应能发生的原因是。
-
(2) 步骤②“过滤1”后所得滤渣的主要成分为。
-
(3) 步骤③“酸溶”,最适合选用的酸为,为提高酸溶速率,可采取的措施是(任意写出一条)。
-
(4) 若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5mol·L-1 , 则此时c(SO42-)= mol·L-1。
-
(5) 从原子利用率的角度分析该流程的优点为。
-
(6) 步骤⑥“合成”三盐的化学方程式为。若得到纯净干燥的三盐49.5t,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为%(结果保留一位小数)
表1 浸出液成分
Al3+ | Fe3+ | Ca2+ | PO43- | Mg2+ | Mn2+ | Y3+ | |
浓度/(mg•L-1) | 7670 | 9460 | 550 | 640 | 5600 | 1500 | 70.2 |
-
(1) 浸出液可用有机溶剂(HR)进行萃取,实现Y3+的富集(已知:Y3+与Fe3+性质相似),原理如下:Fe3+ + 3HR
 FeR3 + 3H+ Y3+ + 3HR
FeR3 + 3H+ Y3+ + 3HR  YR3 + 3H+ (已知:FeR3、YR3均易溶于HR)
YR3 + 3H+ (已知:FeR3、YR3均易溶于HR)浸出液在不同pH下萃取的结果如图1。
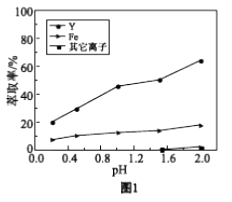
①用化学平衡原理解释,随pH增大,Y3+萃取率增大的原因。
②结合图1解释,工业上萃取Y3+之前,应首先除去Fe3+的原因是。
-
(2) 采用“中和沉淀法”和“磷酸法”可以除铁。
表2 Fe3+、Y3+去除率
终点pH
去除率/%
Fe3+
Y3+
3.0
87.84
19.86
3.5
92.33
23.63
4.5
99.99
44.52
5.0
99.99
89.04
中和沉淀法:向浸出液中加入NaOH除Fe3+ , 去除率如表2所示。
①该实验条件下,Fe3+去除率比Y3+大的可能原因。
磷酸法:将磷酸(H3PO4:三元弱酸)加入到浸出液中,再加入Na2CO3溶液,调pH为2.5,过滤除去磷酸铁沉淀(FePO4),滤液中剩余的Fe3+、Y3+浓度如表3。
表3 滤液中Fe3+、Y3+的浓度
Fe3+
Y3+
浓度/(mg•L-1)
508
68.9
② 配平“磷酸法”除铁过程中的离子方程式
Fe3+ + + = FePO4↓+ CO2↑+
③ 综合分析表1、表2、表3,工业上采用“磷酸法”除铁的原因。
-
(3) 经“磷酸法”除铁后,用有机溶剂HR萃取Y3+ , 可通过(填操作)收集含Y3+的有机溶液。
-
(4) 综合分析以上材料,下列说法合理的是。
a. 分析图1可知,pH在0.2~2.0范围内,有机溶剂中的Fe3+多于水溶液中的Fe3+
b. 表2中 Y3+损失率在20%左右的原因可能是生成的Fe(OH)3对Y3+的吸附
c. 表2中 pH在4.5~5.0范围内,Y3+损失率变大的可能原因:Y3+ + 3OH- = Y(OH)3↓
d. 有机溶剂萃取Y3+的优点是Ca2+、Mg2+、Mn2+等金属离子萃取率极低
请回答下列问题:
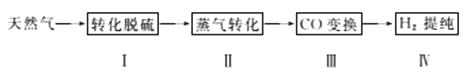
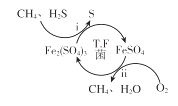
I.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如下。
-
(1) 过程i中H2S发生了 (选填“氧化”或“还原”)反应。
-
(2) 过程ⅱ的离子方程式是。
-
(3) 已知:①Fe3+在pH=l.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
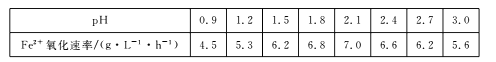
请结合以上信息,判断工业脱硫应选择的最佳pH范围,并说明原因:。
-
(4) Ⅱ.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合下图回答问题。
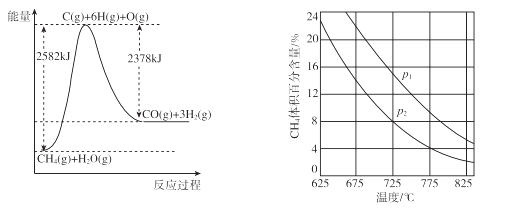
①该过程的热化学方程式是。
②比较压强p1和p2的大小关系:p1 p2(选填“>”“<”或“=”)。
-
(5) Ⅲ.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
Ⅳ.H2提纯:将CO2和H2分离得到H2的过程示意图如下。
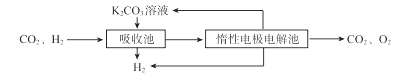
①吸收池中发生反应的离子方程式是 。
②结合电极反应式,简述K2CO3溶液的再生原理:。
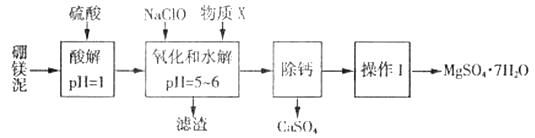
根据题意回答下列问题:
-
(1) 实验中需用1mol/L的硫酸800 mL,若用18.4 mol/L的浓硫酸来配制,则量取浓硫酸时,需使用的量筒规格为_______。(填字母)A . 10 mL B . 25 mL C . 50 mL D . 100 mL
-
(2) 加入的NaClO 可与酸解液中Mn2+ 反应:Mn2+ + ClO-+H2O= MnO2 ↓+ 2H+ + Cl- , 溶液中还有一种离子也会被NaClO氧化,该反应的离子方程式为。该步骤中,物质X是(填化学式)。
-
(3) “滤渣”中除MnO2、CaSO4 外还有。(填化学式)
-
(4) 已知MgSO4、CaSO4的溶解度如下表:
温度/℃
40
50
60
70
溶解度/g
MgSO4
30.9
33.4
35.6
36.9
CaSO4
0.210
0.207
0.201
0.193
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤:。
-
(5) “操作I”是将滤液经过一系列操作后真空干燥,采用“真空干燥”的原因是。
-
(6) 实验中提供的硼镁泥共100g,得到的MgSO4·7H2O 为147.6 g,则MgSO4·7H2O的产率为%。
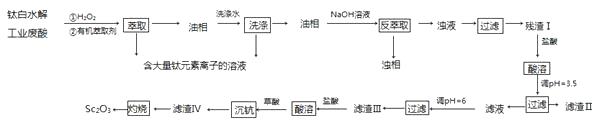
回答下列问题:
-
(1) 在钛白水解工业废酸中,加入双氧水是为了使TiO2+转化为难萃取的[Ti(O2)(OH(H2O)4]+。[Ti(O2)(OH(H2O)4]+中Ti 的化合价为+4,其中非极性键的数目为。
-
(2) 钪的萃取率(E%)与O/A 值[萃取剂体积(O)和废酸液体积(A)之比]的关系如左下图,应选择的最佳O/A值为;温度对钪、钛的萃取率影响情况见右下表,合适的萃取温度为10-15℃,其理由是。

-
(3) 洗涤“油相“可除去大量的钛离子。洗染水是用浓硫酸、双氧水和水按一定比例混合而成。混合过程的实验操作为。
-
(4) 25℃时,用氨水调节滤液的pH,当pH=3.5时,滤渣II的主要成分是;当pH=6时,滤液中Sc3+的浓度为。(Ksp[Fe(OH)3]=2.6×10-39 , Ksp[Sc(OH)3]=9.0×10-31)
-
(5) 写出用草酸(H2C2O4)“沉钪”得到Sc2(C2O4)3的离子方程式。
-
(6) 若从1m3该工厂的钛白水解度酸中提取得到24.4gSc2O3 , 则钪的提取率为(保留三位有效数字)。
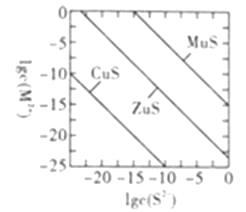
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 物质 | | | | 饱和溶液 | | | |
| 电导率 | 0 | 7 | 37 | 389 | 1989 | 1138 | 13 |
下列分析错误的是()
 固体中不存在自由移动的离子
B . 与①、②对比,可说明③中
固体中不存在自由移动的离子
B . 与①、②对比,可说明③中  发生了电离
C . ⑤、⑥等体积混合后过滤,推测滤液的电导率一定大于13
D . 将①中固体加入④中,发生反应:
发生了电离
C . ⑤、⑥等体积混合后过滤,推测滤液的电导率一定大于13
D . 将①中固体加入④中,发生反应: 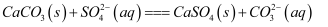
①向石灰水中通入过量的CO2 ②向Fe(OH)3胶体中逐滴加入稀盐酸至过量 ③向Ba(OH)2溶液中逐滴加入过量的稀硫酸 ④向AgCl胶体中逐滴加入过量的稀硝酸.
| 选项 | 实验 | 现象 | 结论 |
| A | 某溶液中加入Ba(NO3)2溶液,再加足量盐酸 | 先有白色沉淀生成,加盐酸后白色沉淀不消失 | 原溶液中有SO42- |
| B | 将湿润的淀粉碘化钾试纸放在盛有红棕色气体的集气瓶口 | 试纸变蓝 | 红棕色气体为溴蒸气 |
| C | 将碳酸钠与盐酸反应产生的气体通入盛有硅酸钠溶液的烧杯中 | 烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| D | 将0.1mol/LMgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成,后转变为蓝色沉淀 | 溶解度:Cu(OH)2<Mg(OH)2 |
| 目的 | 操作 | |
| A | 测定NaClO溶液的pH | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取待测液点滴于试纸的中部,与标准比色卡对比 |
| B | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液,观察溶液的变化 |
| C | 验证Ksp(AgCl)>Ksp(AgI) | 取2mL0.1mol·L-1AgNO3溶液,先后滴加3滴0.1mol·L-1NaCl溶液和5滴0.1mol·L-1KI溶液,先生成白色沉淀,后又产生黄色沉淀 |
| D | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 |
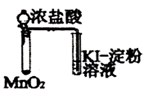 B . 证明在氢氧化钠的乙醇溶液中加热溴乙烷时有乙烯生成
B . 证明在氢氧化钠的乙醇溶液中加热溴乙烷时有乙烯生成 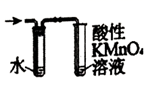 C . 制备氨气
C . 制备氨气  D . 比较Ksp(AgCl)、Ksp(AgBr)的相对大小
D . 比较Ksp(AgCl)、Ksp(AgBr)的相对大小 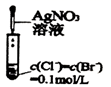
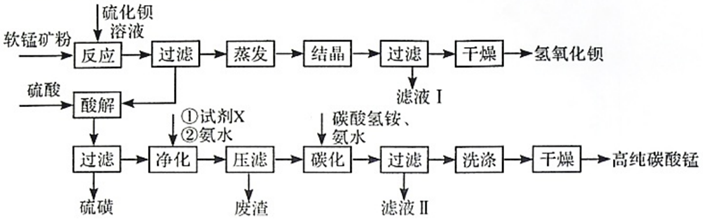 已知:25℃时相关物质的Ksp见下表
已知:25℃时相关物质的Ksp见下表
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mn(OH)2 |
| Ksp | 1×10-16.3 | 1×10-38.6 | 1×10-32.3 | 1×10-12.7 |
回答下列问题:
-
(1) MnO2与BaS溶液反应转化为MnO的化学方程式为,能否通过加热的方式加快该反应的速率,(填“能”或“否”)
-
(2) 保持BaS投料量不变,随软锰矿粉与BaS投料比增大,S的量达到最大值后无明显变化,而Ba(OH)2的量达到最大值后会减小,减小的原因是。
-
(3) 在实验室进行过滤操作时,除了使用铁架台和烧杯以外,还需要的玻璃仪器为。
-
(4) 净化时需先加入的试剂X为(填化学式) 。再使用氨水调溶液的pH,则pH的理论最小值为(当溶液中某离子浓度小于1.0×10-5mol•L-1时,可认为该离子沉淀完全)。
-
(5) 碳化过程中发生反应的离子方程式为。
- 我国的地形复杂多样、山区面积广大,尤其是纵横交错的山脉,构成了地形的骨架,高原、平原、盆地和丘陵镶嵌其间。下面图中表示黄
- 图7为一高山的等高线图,在登山比赛中,某运动员从A点到达B点,下列说法正确的是 A.运动员的体重增加
- 如果点P为反比例函数的图像上的一点,PQ垂直于x轴,垂足为Q,那么△POQ的面积为( )A、12
- 2011年3月2日,台州市出台第二套住房公积金贷款首付比例不低于60%,贷款利率按同期首套住房公积金贷款利率1.1倍执行
- 下列对相关实验的描述,正确的是() A. 鉴定可溶性还原糖时先加入斐林试剂甲液,再加入乙液 B
- 减数第一次分裂过程中,不可能出现的是 A.同源染色体联会
- 下列哪组气体都属于空气污染物() A.SO2、CO2、H2 B.CO2、NO2、N2 C.SO2、CO、N
- 已知A、B为原子序数小于20的元素,且A的原子序数为n,A2+离子比B2-离子少8个电子,则B的原子序数是: A.n +
- 设是上的任意函数,下列叙述正确的是( ) A、是奇函数; B、是奇函数; C、是
- 用电热壶烧开水时,壶中的水蒸气将壶盖顶起,这时水蒸气的内能转化为 能,此时水蒸气的内能 (
- 两个共点力F1和F2的大小为以下哪组数据时,其合力大小不可能为3N()A. F1=7N,F2=4N B. F1=3N,F
- My father read aninteresting book last night. The underline
- 有一固体混合物,可能由碳酸钠、硫酸钠、硫酸铜、氯化钙、氯化钠等物质组成。为鉴别它们,做了如下实验: (1)将固体混合物溶
- 云南一位村长说:“过去村委会主任是上面指派,只要把乡、镇的任务完成就行了。现在不同了,这个职务是老百姓给的,你得对百姓负
- 某研究小组发现染色体上抑癌基因邻近的基因能指导合成反义RNA,反义RNA可以与抑癌基因转录形成的mRNA形成杂交分子,从
- 264. The two brothers once quarreled _____ each other _____
- 下列离子方程式中不正确的是 A.亚硫酸钡与盐酸反应:BaSO3+2H+=Ba2++SO2↑+H2O B.氯气与水反应:C
- 参加四川抗震救灾的飞行员在刚跳离飞机,其降落伞尚未打开的一段时间内,下列说法正确的是A.空气阻力做正功 B.
- 由1,4,5,x这四个数字组成无重复数字的四位数,若所有四位数的各位数字之和为288,则x等于( )A.2
- 下列物质的用途主要由其化学性质决定的() A.用氮气保存食品 B.石墨用作电池的电极 C.发热病人用酒精擦身体降温
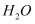
 NaCl溶液
NaCl溶液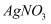 溶液
溶液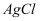 饱和溶液
饱和溶液


