离子浓度大小的比较 知识点题库
已知常温下,0.1mol•L﹣1的HA溶液中  =1×10﹣8 , 下列叙述中正确的是( )
=1×10﹣8 , 下列叙述中正确的是( )
 =1×10﹣8 , 下列叙述中正确的是( )
=1×10﹣8 , 下列叙述中正确的是( )
A . 0.01 mol•L﹣1HA的溶液中 c(H+)=l×10﹣4mol•L﹣1
B . pH=3的HA溶液与pH=ll的NaOH溶液等体积混合后所得溶液中:c(Na+)=c(A﹣)>c(OH﹣)=c(H+)
C . 浓度均为0.1 mol•L﹣1的HA溶液和NaA溶液等体积混合后所得溶液显酸性,则c(H+)﹣c(OH﹣)>c(A﹣)﹣c(HA)
D . pH=3的HA溶液与pH=11的NaOH溶液混合后所得溶液显碱性,则 c(Na+)>c(A﹣)>c(OH﹣)><c(H+)
向amol/L的氨水中加入等体积b mol•L-1的盐酸,下列关系错误的是( )
A . 当a=b时,c(H+)=c(OH-)+c(NH3·H2O)
B . 当a>b时,c(NH4+)+c(NH3·H2O) >c(Cl-)
C . 当a<b时,c(NH4+)>c(Cl-)>c(OH-)>c(H+)
D . 当a与b为任意比时,c(NH4+)+c(H+)=c(Cl-)+c(OH-)
已知亚硒酸(H2SeO3)为二元弱酸,常温下,向某浓度的亚硒酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中H2SeO3、HSeO3-、SeO32-三种微粒的物质的量分数与溶液pH 的关系如图所示。下列说法错误的是( )
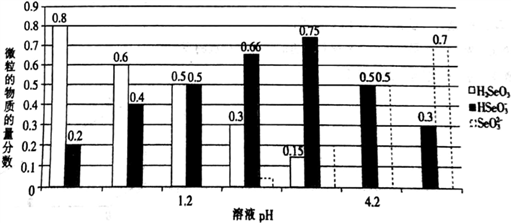
A . 常温下,亚硒酸的电离平衡常数K2=10-4.2
B . pH=1.2的溶液中:c(Na+)+c(H+)=c(OH-)+c(H2SeO3)
C . 将相同物质的量NaHSeO3和Na2SeO3 固体完全溶于水可配得pH为4.2的混合液
D . 向pH=1.2的溶液中滴加NaOH溶液至pH=4.2的过程中水的电离程度一直增大
常温下,向20 mL某浓度的硫酸中滴入0.1 mol·L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示。下列分析正确的是( )
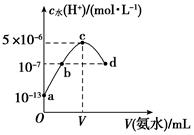
A . 该硫酸的浓度为1 mol·L-1
B . b点所示溶液中:c( 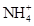 )=c(
)=c( 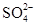 )
C . V=40
D . c点所示溶液中:c(H+)-c(OH-)=c(NH3·H2O)
)
C . V=40
D . c点所示溶液中:c(H+)-c(OH-)=c(NH3·H2O)
常温下有浓度均为0.5 mol/L的四种溶液:
①Na2CO3溶液 ②NaHCO3溶液 ③HCl溶液 ④氨水
-
(1) 上述溶液中,可发生水解的是(填序号,下同)。
-
(2) 上述溶液中,既能与氢氧化钠反应,又能和硫酸反应的溶液中离子浓度由大到小的顺序为。
-
(3) 向④中加入少量氯化铵固体,此时c(NH4+)/c(OH-)的值(填“增大”、“减小”或“不变”)。
-
(4) 若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积④的体积(填“大于”、“小于”或“等于”),此时溶液中离子浓度由大到小的顺序是。
-
(5) 取10 mL溶液③,加水稀释到500 mL,则此时溶液中由水电离出的c(H+)=。
关于小苏打水溶液的表述正确的是( )
A . c(Na+) = c(HCO3-) + c(CO32-) + c(H2CO3)
B . c(Na+)+c(H+) = c(HCO3-) + c(CO32-) + c(OH-)
C . HCO3-的电离程度大于HCO3-的水解程度
D . 存在的电离有:NaHCO3 = Na++ HCO3- ,HCO3- = H++ CO32-
工业上可由氢气、氮气合成氨气,溶于水形成氨水。一定温度下,向2L固定体积的密闭容器中加入N2(g)和H2(g),发生反应:N2(g)+3H2(g)  2NH3(g)+Q(Q>0),NH3物质的量随时间的变化如图所示。
2NH3(g)+Q(Q>0),NH3物质的量随时间的变化如图所示。
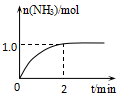
-
(1) 0~2min内的平均反应速率v(H2)=。
-
(2) 该温度下,反应的平衡常数表达式K=。
其平衡常数K与温度T的关系如下表:
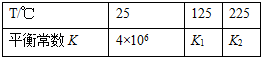
试判断K1K2(填写“>”、“=”或“<”)。
-
(3) 能说明该合成氨反应已达到平衡状态的是(选填编号)。
a.3v(N2)=v(H2)
b.容器内压强保持不变
c.混合气体的密度保持不变
d.25℃时,测得容器中c(NH3)=0.2mol·L-1 , c(H2)=c(N2)=0.01mol·L-1
常温下,某同学将盐酸与氨水等体积混合,两种溶液的浓度和混合后所得溶液的pH如表。
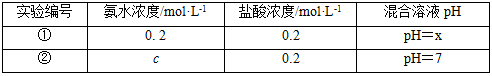
请回答:
-
(4) ①中所得混合溶液,pH7(填“>”、“<”或“=”);②中c 0.2(填“>”、“<”或“=”),所得混合溶液中各离子浓度大小关系为。
-
(5) 请你设计一个能证明一水合氨是弱电解质的简要方案。
25℃时,体积均为25.00mL,浓度均为0.0100mo1•L-1的HA、H3B溶液分别用0.0100mo1•L-1NaOH溶液滴定,溶液的pH随V(NaOH)变化曲线如图所示,下列说法正确的是( )
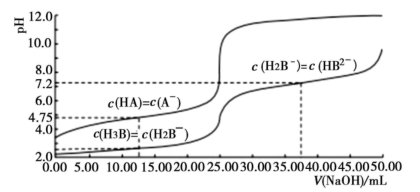
A . 25℃时,0.0100mo1•L-1Na2HB溶液的pH>7
B . 向HA溶液中滴加NaOH溶液至中性,c(A-)<c(HA)
C . NaOH溶液滴定HA溶液应选甲基橙作指示剂
D . 25℃时,H2B-离子的水解常数的数量级为10-3
25℃时,用浓度为0.01mol·L-1的HA溶液滴定20mL浓度为0.01mol·L-1的NaOH溶液,滴定曲线如图所示。下列说法错误的是( )
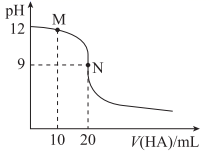
A . 应选用酚酞作指示剂
B . M点溶液中存在:c(Na+)>c(A-)
C . Ka(HA)≈2×10-8
D . N点溶液中存在:c(OH-)-c(H+)=c(HA)
连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
-
(1) 常温下,用0.01mol·L-1的NaOH溶液滴定10mL0.01mol·L-1H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
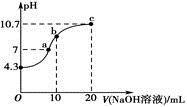
①写出H2N2O2在水溶液中的电离方程式:。
②c点时溶液中各离子浓度由大到小的顺序为。
③b点时溶液中c(H2N2O2)c(N2O22-)。(填“>”“<”或“=”,下同)
④a点时溶液中c(Na+)c(HN2O)+c(N2O22-)。
-
(2) 硝酸银溶液和连二次硝酸钠溶液混合,可以得到黄色的连二次硝酸银沉淀,向该分散系中滴加硫酸钠溶液,当白色沉淀和黄色沉淀共存时,分散系中
 =。[已知Ksp(Ag2N2O2)=4.2×10-9 , Ksp(Ag2SO4)=1.4×10-5]
=。[已知Ksp(Ag2N2O2)=4.2×10-9 , Ksp(Ag2SO4)=1.4×10-5]
-
(3) 有时我们将NaHCO3溶液中的平衡表示为:2HCO3-
 H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理___(填序号)
A . 适当浓度的盐酸 B . 适当浓度Ba(OH)2溶液 C . 适当浓度BaCl2溶液
H2CO3+CO32-;为了证明该平衡存在,你认为应向NaHCO3溶液中加入下列哪种试剂合理___(填序号)
A . 适当浓度的盐酸 B . 适当浓度Ba(OH)2溶液 C . 适当浓度BaCl2溶液
25℃时,向10 mL0.10 mol/L的一元弱酸HA(Ka=1.0×10-3)中逐滴加入0.10 mol/L NaOH溶液,溶液pH随加入NaOH溶液体积的变化关系如图所示。若溶液混合引起的体积变化可忽略,下列说法正确的是( )
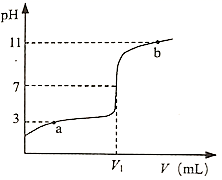
A . a点时,c(HA)+c(OH-)=c(Na+)+c(H+)
B . pH=7时,V1>10 mL
C .  点时,c(Na+)=c(HA)+c(A-)+c(OH-)
D . V=10 mL时,c(HA)+c(A-)+c(Na+)=0.20 mol/L
点时,c(Na+)=c(HA)+c(A-)+c(OH-)
D . V=10 mL时,c(HA)+c(A-)+c(Na+)=0.20 mol/L
 点时,c(Na+)=c(HA)+c(A-)+c(OH-)
D . V=10 mL时,c(HA)+c(A-)+c(Na+)=0.20 mol/L
点时,c(Na+)=c(HA)+c(A-)+c(OH-)
D . V=10 mL时,c(HA)+c(A-)+c(Na+)=0.20 mol/L
贵州长期受到酸雨污染的困扰,主要原因是企业和家庭直接使用燃煤时,废气未经处理直接排放到空气中,近年来,酸雨治理的成效非常显著。2020年6月份的某个雨天,遵义市气象台的实验人员收集了150mL雨水,并分析了雨水中的离子及其浓度,结果统计如下:
| 离子 | | Cl- | Na+ | | |
| 浓度/10-5mol/L | 5.1 | 4.3 | 4.8 | 2.1 | 2.0 |
则这次雨水的pH值约是(lg2=0.3) ( )
A . 4.5
B . 5.3
C . 5.6
D . 4.7
室温时,下列溶液中微粒的物质的量浓度关系正确的是( )
A . pH=8的NaClO溶液中:c(Na+)>c(ClO-)>c(OH-)>c(H+)
B . 新制氯水中:c(H+)=c(HClO)+c(ClO-)+c(OH-)
C . 0.1 mol/L HCl溶液与0.2 mol/L NH3·H2O溶液等体积混合后pH>7:c(NH3·H2O)>c(Cl-)>c(NH 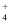 )>c(OH-)
D . 0.1 mol/L K2C2O4溶液与0.2 mol/L KHC2O4溶液等体积混合:4c(K+)=3[c(C2O
)>c(OH-)
D . 0.1 mol/L K2C2O4溶液与0.2 mol/L KHC2O4溶液等体积混合:4c(K+)=3[c(C2O  )+c(HC2O
)+c(HC2O  )+c(H2C2O4)]
)+c(H2C2O4)]
 )>c(OH-)
D . 0.1 mol/L K2C2O4溶液与0.2 mol/L KHC2O4溶液等体积混合:4c(K+)=3[c(C2O
)>c(OH-)
D . 0.1 mol/L K2C2O4溶液与0.2 mol/L KHC2O4溶液等体积混合:4c(K+)=3[c(C2O  )+c(HC2O
)+c(HC2O  )+c(H2C2O4)]
)+c(H2C2O4)]
常温下将  溶液滴加到
溶液滴加到  溶液中,混合溶液的
溶液中,混合溶液的  与离子浓度变化的关系如图所示(纵坐标为
与离子浓度变化的关系如图所示(纵坐标为  或
或  。下列叙述错误的是( )
。下列叙述错误的是( )
 溶液滴加到
溶液滴加到  溶液中,混合溶液的
溶液中,混合溶液的  与离子浓度变化的关系如图所示(纵坐标为
与离子浓度变化的关系如图所示(纵坐标为  或
或  。下列叙述错误的是( )
。下列叙述错误的是( ) 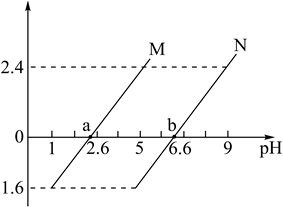
A . 曲线M表示  与
与  B . 图中a点对应溶液中:
B . 图中a点对应溶液中: 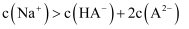 C .
C .  与
与 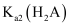 之比为
之比为 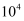 D .
D . 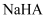 溶液中:
溶液中: 
 与
与  B . 图中a点对应溶液中:
B . 图中a点对应溶液中: 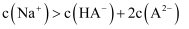 C .
C .  与
与 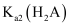 之比为
之比为 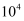 D .
D . 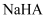 溶液中:
溶液中: 
常温下,向饱和氯水中逐滴滴入0.1 mol/L的氢氧化钠溶液,pH变化如下图所示,下列有关叙述正确的是( )
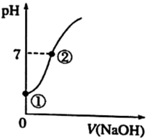
A . ①点所示溶液中只存在HClO的电离平衡
B . ①点所示溶液中: 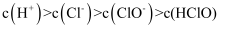 C . ②点所示溶液中:
C . ②点所示溶液中: 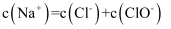 D . ①到②水的电离程度逐渐减小
D . ①到②水的电离程度逐渐减小
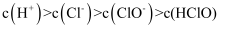 C . ②点所示溶液中:
C . ②点所示溶液中: 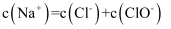 D . ①到②水的电离程度逐渐减小
D . ①到②水的电离程度逐渐减小
25℃,向20.00 mL 0.100 mol·L−1 CH3COOH中滴加0.100 mol·L−1 NaOH过程中,pH变化如图所示。
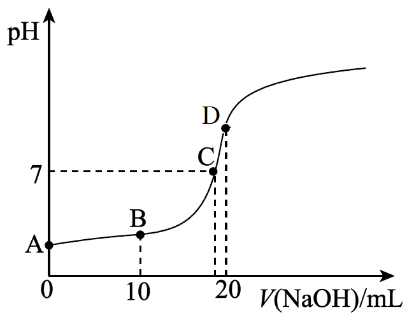
-
(1) A点溶液pH1.(填“>”、“<”或“=”)。
-
(2) 下列有关B点溶液的说法正确的是(填字母序号)。
a.溶质为:CH3COOH、CH3COONa
b.微粒浓度满足:c(Na+) + c(H+) = c(CH3COO−) + c(OH−)
c.微粒浓度满足:c(Na+) = c(CH3COOH) + c(CH3COO−)
-
(3) A、C两点水的电离程度:AC(填“>”、“<”或“=”)。
-
(4) 滴加 20 mL NaOH 溶液时,D点溶液的pH >7,原因是(用离子方程式表示)。
室温下,通过下列实验探究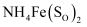 溶液的性质(假设实验前后溶液体积不变)。
溶液的性质(假设实验前后溶液体积不变)。
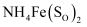 溶液的性质(假设实验前后溶液体积不变)。
溶液的性质(假设实验前后溶液体积不变)。实验 | 实验操作和现象 |
1 | 用pH试纸测定 |
2 | 向 |
3 | 向 |
4 | 向 |
下列说法正确的是( )
A .  溶液中存在
溶液中存在 B . 实验2中沉淀仅为
B . 实验2中沉淀仅为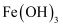 C . 实验3得到的溶液中有
C . 实验3得到的溶液中有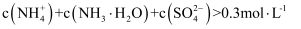 D . 实验4中发生反应的离子方程式为
D . 实验4中发生反应的离子方程式为
 溶液中存在
溶液中存在 B . 实验2中沉淀仅为
B . 实验2中沉淀仅为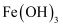 C . 实验3得到的溶液中有
C . 实验3得到的溶液中有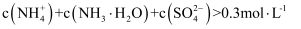 D . 实验4中发生反应的离子方程式为
D . 实验4中发生反应的离子方程式为
下列说法正确的是( )
A . 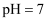 的溶液中
的溶液中 、
、 、
、 、
、 能大量共存
B . 相同温度下,
能大量共存
B . 相同温度下,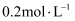 醋酸溶液与
醋酸溶液与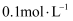 醋酸溶液中
醋酸溶液中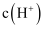 之比小于
之比小于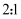 C . 等物质的量浓度①
C . 等物质的量浓度① 、②NH4Al(SO4)2溶液中
、②NH4Al(SO4)2溶液中 浓度的大小顺序为①>②
D . 常温下,
浓度的大小顺序为①>②
D . 常温下, 均为
均为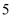 的氯化铵溶液和醋酸溶液中水的电离程度相同
的氯化铵溶液和醋酸溶液中水的电离程度相同
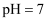 的溶液中
的溶液中 、
、 、
、 、
、 能大量共存
B . 相同温度下,
能大量共存
B . 相同温度下,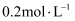 醋酸溶液与
醋酸溶液与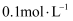 醋酸溶液中
醋酸溶液中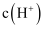 之比小于
之比小于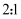 C . 等物质的量浓度①
C . 等物质的量浓度① 、②NH4Al(SO4)2溶液中
、②NH4Al(SO4)2溶液中 浓度的大小顺序为①>②
D . 常温下,
浓度的大小顺序为①>②
D . 常温下, 均为
均为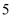 的氯化铵溶液和醋酸溶液中水的电离程度相同
的氯化铵溶液和醋酸溶液中水的电离程度相同
室温下,向20mL浓度均为0.1 的
的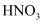 和
和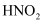 混合液中逐滴加入0.1
混合液中逐滴加入0.1 NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( )
NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( )
 的
的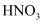 和
和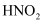 混合液中逐滴加入0.1
混合液中逐滴加入0.1 NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( )
NaOH溶液,溶液pH变化曲线如图。下列说法错误的是( )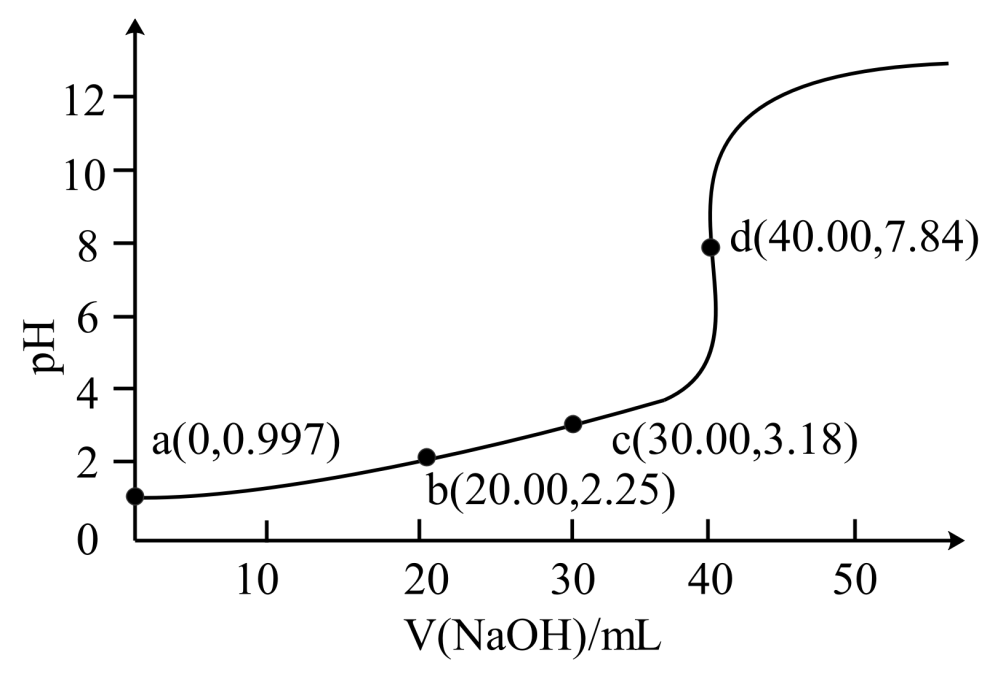
A . a点: B . 导电能力:b<c
C . c点:
B . 导电能力:b<c
C . c点: D . 由d点可得
D . 由d点可得
 B . 导电能力:b<c
C . c点:
B . 导电能力:b<c
C . c点: D . 由d点可得
D . 由d点可得
利用“价类二维图”对元素及其化合物进行相关归纳整理,是一种常用的学习研究方法。硫及其化合物的“价类二维图”如图所示,回答下列问题:
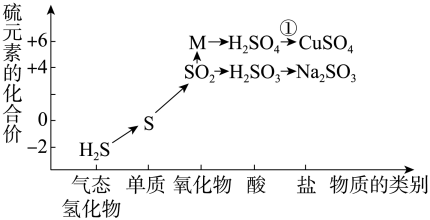
-
(1) M的化学式为,除去
 中少量的
中少量的 杂质可选择的试剂有(填正确答案标号)。
杂质可选择的试剂有(填正确答案标号)。A.饱和
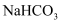 溶液 B.碱石灰 C.饱和
溶液 B.碱石灰 C.饱和 溶液 D.酸性高锰酸钾溶液
溶液 D.酸性高锰酸钾溶液 -
(2) 工业上实现①过程生产
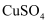 常采用废铜料与稀硫酸在通入空气并加热的条件下反应制取,其反应的离子方程式为。
常采用废铜料与稀硫酸在通入空气并加热的条件下反应制取,其反应的离子方程式为。
-
(3)
 的水溶液中各离子的浓度大小关系是,检验
的水溶液中各离子的浓度大小关系是,检验 溶液是否变质的方法是。
溶液是否变质的方法是。
-
(4) 实验室欲制备
 , 从氧化还原角度分析,下列合理的药品选择是____(填正确答案标号)。
A .
, 从氧化还原角度分析,下列合理的药品选择是____(填正确答案标号)。
A . 和
和 B .
B .  和
和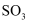 C .
C .  和S
D .
和S
D .  和
和
-
(5) 已知:常温下
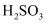 的电离平衡常数
的电离平衡常数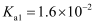 ,
, 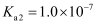 ,
, 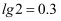 , 忽略第二步电离,则
, 忽略第二步电离,则 溶液的pH约为(保留1位小数)。
溶液的pH约为(保留1位小数)。
最近更新
- 如图所示,一质量为m的木块沿光滑的水平直轨道以速度v0=12m/s匀速运动,木块顶部边缘有一质量为m’的钢珠随它一起运动
- 【2013年·山东省东营市】 (二)(8分) (甲)……友人便怒:“非人哉!与人期行,相委而去。”元方曰:“君与家君期日
- 读某地区(35ºN)平面图,回答下列问题:(1)学校在科技园的 方向, 科技园在火车站的方向。 (2)若学校与火车站
- 、“一条条巨龙翻山越岭,为雪域高原送来安康,那是一条神奇的天路哎……把人间的温暖送到边疆,从此山不在高路不再漫长,各族儿
- 依次填入下列句子中的词语,恰当的一组是() ①记者从最高人民法院获悉,由最高法院近日核准死刑的丁广庆等6名毒贩,24日分
- 皇权和相权的矛盾是我国封建专制主义中央集权内部潜在的主要矛盾之一。下列封建王朝的政治举措旨在分割相权的是
- 有两盏白炽灯L1、L2,L1标有“PX220 100”字样,L,2标有“PX220 40”字样。将这两盏灯串联接在电压为
- 关于地理要素相互作用产生新功能叙述正确的是 A.生产功能是指自然地理环境具有合成有机物的能力 B.生产功能是指绿色植物生
- 人类的多指是由常染色体上的显性基因(G)控制的,有一对多指的夫妇生下一个正常的儿子,问这对夫妇的基因为() A.Gg和G
- Material Girl no more? Madonna says writing children’s books
- 19世纪英国诞生的一项伟大的理论,戳穿了“上帝创造了万物”的谬论,把越来越多的人从宗教神学的无知、愚昧和落后中解放出来。
- 单词拼写。根据每个句子中所给的汉语意思,写出单词的正确形式,每空只写一个单词 1. It’s an______(小时
- 读“北半球理想大陆自然带分布示意图”,完成下列问题。(1)图中A—B—C—D—E—F—G的更替反映了自然带的______
- 中国有七大方言:北方方言、吴方言、闽方言、粤方言、客家方言、赣方言、湘方言。这主要说明中华文化 ( ) A.源远流
- 被尊奉为中华民族人文始祖的是( ) A、尧 B、舜 C、黄帝
- 下列物质在核糖体上合成的是() ①性激素 ②胰岛素 ③淀粉 ④消化酶 ⑤纤维素 A.①② B
- 物体的速度方向、加速度方向与所受合外力的方向的关系是A. 速度方向、加速度方向与合外力方向三者总是相同的B. 加速度方向
- She raised her finger to her lips as _________ for silence.A
- (1)-5 ℃时,高氙酸钠(Na4XeO6)能跟浓硫酸反应生成XeO4气体。XeO4极不稳定,固体XeO4在-40 ℃也
- 第五部分 书面表达(满分25分) 目前世界各地甲型H1N1流感流行严重,各地学校都采取了一系列的防控措施。请



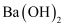 溶液,产生沉淀
溶液,产生沉淀 , 产生红褐色沉淀
, 产生红褐色沉淀


