影响盐类水解程度的主要因素 知识点题库
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH⇌CH3COO﹣+H+对于该平衡,下列叙述正确的是( )
A . 加入少量NaOH固体,平衡向正反应方向移动
B . 加水,反应速率增大,平衡向逆反应力向移动
C . 滴加少量0.1mol/L HCl溶液,溶液中c(H+)减少
D . 加入少量CH3COONa固体,平衡向正反应方向移动
在一定条件下,Na2S溶液存在水解平衡:S2﹣+H2O═HS﹣+OH﹣ . 下列说法正确的是( )
A . 稀释溶液,水解平衡常数增大
B . 通入H2S,HS﹣浓度增大
C . 升高温度,  减小
D . 加入NaOH固体,溶液pH减小
减小
D . 加入NaOH固体,溶液pH减小
 减小
D . 加入NaOH固体,溶液pH减小
减小
D . 加入NaOH固体,溶液pH减小
常温下向四份0.1mol•L﹣1的醋酸钠溶液中分别加入少量冰醋酸、硫酸氢钠固体、醋酸钠固体、氢氧化钠固体(忽略溶液体积及温度变化),则溶液中  变化正确的是( )
变化正确的是( )
 变化正确的是( )
变化正确的是( )
A . 增大、增大、不变、减小
B . 增大、减小、增大、减小
C . 减小、增大、增大、减小
D . 增大、减小、不变、减小
有关说法正确的是( )
A . 0.1mol/L NH4Cl溶液加蒸馏水稀释,溶液的pH不断减小
B . 常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后,溶液的pH<7
C . NH4HSO4溶液中滴加NaOH溶液至溶液pH=7,则c(Na+)=2c(SO42﹣)
D . 0.1mol/L的NaHA溶液,其pH=4时:c(HA﹣)>c(H+)>c(H2A)>c(A2﹣)
在蒸发皿中加热蒸干下列物质的溶液,再灼烧(溶液低于400℃)可以得到原溶质固体的是( )
A . AlCl3
B . NaHCO3
C . MgSO4
D . KMnO4
对于0.1mol·L-1 Na2SO3溶液,正确的是( )
A . 升高温度,溶液的pH降低
B . c(Na+)=2c(SO32-)+ c(HSO3-)+ c(H2SO3)
C . c(Na+)+c(H+)=2 c(SO32-)+ 2c(HSO3-)+ c(OH-)
D . 加入少量NaOH固体,c(SO32-)与c(Na+)均增大
对1L1 mol•L-1的NH4Cl溶液进行如下操作,溶液的pH增大的是( )
A . 加热
B . 加入少量的NH4Cl固体
C . 加水稀释
D . 再加1L 1mol•L NH4Cl溶液
下列反应的发生与沉淀溶解平衡或盐类水解平衡的移动无关的是( )
A . 盐酸与碳酸钙反应生成二氧化碳
B . 镁条与氯化铵溶液反应生成氢气
C . 硝酸银溶液与盐酸反应生成氯化银
D . 硫酸铝溶液和小苏打溶液反应生成二氧化碳
常温下2 mL 1 mol·L-1 NaHCO3溶液,pH约为8,向其中滴加几滴饱和CaCl2溶液,有白色沉淀和无色气体生成。下列说法中,错误的是( )
A . NaHCO3溶液中,HCO3-水解程度大于其电离程度
B . NaHCO3溶液中,c(Na+) > c(HCO3-) > c(OH-) > c(H+)
C . 最终所得的混合溶液中,c(Na+) + c(H+) = c(HCO3-) + 2c(CO32-)+ c(OH-)
D . 滴加饱和CaCl2溶液促进了HCO3-的电离
对常温下pH=3的CH3COOH溶液,下列叙述不正确的是( )
A . c(H+)=c(CH3COO-)+c(OH-)
B . 加入少量CH3COONa固体后,c(CH3COO-)降低
C . 该溶液中由水电离出的c(H+)是1.0×10-11 mol/L
D . 与等体积pH =11的NaOH溶液混合后所得溶液显酸性
室温下,下列溶液中粒子的物质的量浓度关系正确的是( )
A . 0.1mol/L NaHS溶液:c(H+)+c(Na+)=c(S2-)+c(HS-)+c(OH-)
B . 0.1mol/L Na2CO3溶液:c(H2CO3)+c(HCO3-)+c(CO32-)=0.2mol/L
C . pH=11的NaOH溶液与pH =3的CH3COOH溶液等体积混合:c(Na+)> c(CH3COO-)> c(OH-)> c(H+)
D . 浓度均为0.1 mol/L的 ① NH4Cl ②NH4Al(SO4)2 ③ NH4HCO3三种溶液,其中c(NH4+):②>①>③
根据下列操作及现象,所得结论正确的是( )
| 序号 | 操作及现象 | 结论 |
| A | 将0.1 mol·L-1 Na2CO3溶液稀释到0.01 mol·L-1 , 测得pH变小 | 稀释后CO32-的水解程度减小 |
| B | 向某无色溶液中滴加盐酸酸化的BaCl2溶液,产生白色沉淀 | 原溶液中一定含有SO42- |
| C | 向25 mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 向溴水中加入少量苯,振荡静置后水层为无色 | 苯与Br2发生了加成反应 |
A . A
B . B
C . C
D . D
测定0.1mol·L-1Na2SO3溶液先升温再降温过程中的pH,数据如下。
| 时刻 | ① | ② | ③ | ④ |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比试验,④产生白色沉淀多。下列说法错误的是()
A . Na₂SO3溶液中存在水解平衡:SO32-+H2O  HSO-3+OH-
B . ④的pH与①不同,是由于SO32-浓度减小造成的
C . ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D . ①与④的Kw值相等
HSO-3+OH-
B . ④的pH与①不同,是由于SO32-浓度减小造成的
C . ①→③的过程中,温度和浓度对水解平衡移动方向的影响一致
D . ①与④的Kw值相等
下列关于物质结构和元素性质说法正确的是( )
A . 非金属元素之间形成的化合物一定是共价化合物
B . 乙醇可与水以任意比例混溶,是因为与水形成氢键
C . 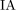 族与
族与 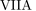 族元素原子之间形成的化学键一定是离子键
D . 同主族元素的简单阴离子还原性越强,水解程度越大
族元素原子之间形成的化学键一定是离子键
D . 同主族元素的简单阴离子还原性越强,水解程度越大
下列说法正确的是( )
A . 氢氧燃料电池工作时,若消耗标准状况下11.2 L H2 , 则转移电子数为6.02×1023
B . 常温下,将稀CH3COONa溶液加水稀释后,n(H+)﹒n(OH-)不变
C . 合成氨生产中将NH3液化分离,可加快正反应速率,提高H2的转化率
D . 反应2NaCl(s)=2Na(s)+Cl2(g)的ΔH<0,ΔS>0
工业上用铝土矿(主要成分为Al2O3 , 含Fe2O3等杂质)为原料冶炼铝的工艺流程如下:
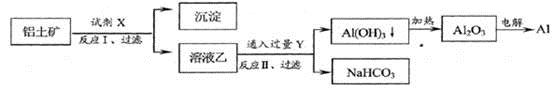
对上述流程中的判断正确的是( )
A . 试剂X为稀硫酸
B . 结合质子( H+)的能力由强到弱的顺序是:AlO2-> OH- >CO32-
C . 反应II中生成Al(OH)3的反应为:CO2+AlO2- +2H2O =Al(OH)3↓+HCO3-
D . Al2O3熔点很高,工业上还可采用电解熔融AlCl3冶炼Al
有关下列两种溶液的说法中,正确的是( )
①0.1mol/L CH3COONa溶液 ②0.1mol/L CH3COOH溶液
A . 相同温度下,溶液中水的电离度:溶液①>溶液②
B . 等体积混合溶液①和溶液②,所得溶液中c(Na+)>c( CH3COO-)>c(H+)>c(OH-)
C . 加水稀释溶液①,溶液中  不变
D . 向溶液①中加入少量的CH3COONa固体则
不变
D . 向溶液①中加入少量的CH3COONa固体则  减小
减小
 不变
D . 向溶液①中加入少量的CH3COONa固体则
不变
D . 向溶液①中加入少量的CH3COONa固体则  减小
减小
实验测得 10 mL 0. 50 mol•L -1NH4Cl溶液、10 mL 0. 50 mol•L -1CH3COONa溶液的pH分别随温度与稀释加水量的变化如图所示。已知25℃时CH3COOH和NH3•H2O的电离常数均为1. 8×10-5.下列说法错误的是( )
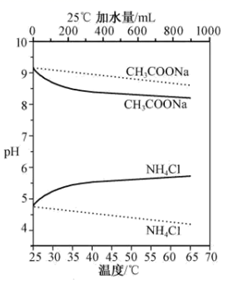
A . 加水稀释初期两种盐的水解率变化程度比稀释后期大
B . 图中虚线表示pH随加水量的变化,实线表示pH随温度的变化
C . 将NH4Cl溶液加水稀释至浓度 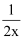 mol・L-1溶液pH变化值小于lgx
D . 将稀释相同倍数的NH4Cl与CH3COONa溶液混合,混合液中 c(CH3COO-)= c(NH
mol・L-1溶液pH变化值小于lgx
D . 将稀释相同倍数的NH4Cl与CH3COONa溶液混合,混合液中 c(CH3COO-)= c(NH  )
)
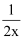 mol・L-1溶液pH变化值小于lgx
D . 将稀释相同倍数的NH4Cl与CH3COONa溶液混合,混合液中 c(CH3COO-)= c(NH
mol・L-1溶液pH变化值小于lgx
D . 将稀释相同倍数的NH4Cl与CH3COONa溶液混合,混合液中 c(CH3COO-)= c(NH  )
)
一定条件下,在某Na2S的稀溶液中,下列说法错误的是( )
A . 加水稀释溶液,  增大
B . 通入少量HCl气体,水电离的c(OH-)减小
C . 加入少量NaOH固体,c(Na+)+c(H+)>2c(S2-)+c(OH-)+c(HS-)
D . 适当升高温度,溶液中c(S2-)浓度减小
增大
B . 通入少量HCl气体,水电离的c(OH-)减小
C . 加入少量NaOH固体,c(Na+)+c(H+)>2c(S2-)+c(OH-)+c(HS-)
D . 适当升高温度,溶液中c(S2-)浓度减小
 增大
B . 通入少量HCl气体,水电离的c(OH-)减小
C . 加入少量NaOH固体,c(Na+)+c(H+)>2c(S2-)+c(OH-)+c(HS-)
D . 适当升高温度,溶液中c(S2-)浓度减小
增大
B . 通入少量HCl气体,水电离的c(OH-)减小
C . 加入少量NaOH固体,c(Na+)+c(H+)>2c(S2-)+c(OH-)+c(HS-)
D . 适当升高温度,溶液中c(S2-)浓度减小
某化学兴趣小组在学习完温度对盐类水解的影响后,测定了0.1mol·L-1Na2CO3溶液的pH随温度的变化,结果如下图所示。下列分析正确的是( )
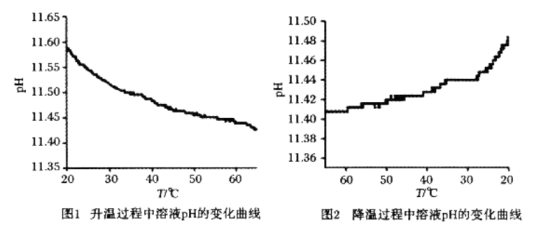
A . 升温前溶液呈碱性的原因是:CO +2H2O
+2H2O H2CO3+2OH-
B . 常温下,0.1 mol·L-1Na2CO3溶液中:c(Na+)>2c(CO
H2CO3+2OH-
B . 常温下,0.1 mol·L-1Na2CO3溶液中:c(Na+)>2c(CO )+c(HCO
)+c(HCO )
C . 温度升高,Na2CO3水解程度增大,溶液pH增大,故图1实验数据一定不符合题意
D . 降低温度,Na2CO3水解平衡移动和水的电离平衡移动对溶液pH的影响一致
)
C . 温度升高,Na2CO3水解程度增大,溶液pH增大,故图1实验数据一定不符合题意
D . 降低温度,Na2CO3水解平衡移动和水的电离平衡移动对溶液pH的影响一致
 +2H2O
+2H2O H2CO3+2OH-
B . 常温下,0.1 mol·L-1Na2CO3溶液中:c(Na+)>2c(CO
H2CO3+2OH-
B . 常温下,0.1 mol·L-1Na2CO3溶液中:c(Na+)>2c(CO )+c(HCO
)+c(HCO )
C . 温度升高,Na2CO3水解程度增大,溶液pH增大,故图1实验数据一定不符合题意
D . 降低温度,Na2CO3水解平衡移动和水的电离平衡移动对溶液pH的影响一致
)
C . 温度升高,Na2CO3水解程度增大,溶液pH增大,故图1实验数据一定不符合题意
D . 降低温度,Na2CO3水解平衡移动和水的电离平衡移动对溶液pH的影响一致
最近更新
- 某市政府宣布缓建、移建“海沧PX项目”。据有关资料,“海沧PX项目’,投资108亿,如果建成投产,每年能为该市带来800
- 甲乙两家企业,生产同一种商品,并以相同的价格出售这一商品,甲企业盈利,乙企业亏本。 请问:(1)其中可能的原因是什么?
- 下图是我国新疆某地局部示意图,A、B为绿洲中两个分布在河流沿岸的聚落。近十几年来,A聚落规模不断扩大,B聚落规模不断缩小
- 已知:的名称为4—苯基—2—丁醇。下列关于该有机物说法中,正确的是( )A.的名称为3—苯基—2—丙醇 B.与互为
- _______ your opinions are worth considering, the committee f
- 电子数相等的微粒叫等电子体,下列微粒组是等电子体的是( )A.N2O4和NO2 B.
- 天下英雄谁敌手,曹、刘。 。(辛弃疾《南乡子•登京口北固亭有怀》)
- 把下面的句子排列组成语意连贯的一段话。(只填序号。) ①发思古之幽情 ②不约而同地都把长江奔流视为历史变化的象征 ③永恒
- 2008年8月1 2日,备受关注的中国农村小额人身保险项目正式进入试点阶段国人寿9款产品正式上市试销,首批试点地区为山西
- 下图表示某绿色植物细胞内部分物质的转变过程,有关叙述正确的是( )A.图中①、②两物质依次是H2O和O2 B.图中
- 仅用蒸馏水,不能鉴别的一组物质是( ) A.苯和四氯化碳
- 如今,“打包”的现象越来越流行。人们在餐馆就餐后,将剩菜“打包”带走是很平常的事情。这说明 ( ) A.人们的生活水
- 如图,正三棱柱的各棱长都为2,分别为AB、A1C1的中点,则EF的长是( ) A.2 B.
- 写作(40分) 题目:家庭给我的 要求:①写一篇记叙文,不少于500字。 ②空白处可填:“喜
- 两物体甲和乙在同一直线上运动,它们在0~0.4 s时间内的v-t图象如图所示.若仅在两物体之间存在相互作用,则物体甲与乙
- 在马克思主义哲学看来,物质是( ) A.构成事物的最小的不可分割的微粒 B.看得见摸得着的有形的实体 C.在人的意识
- 在极坐标系中,已知到直线l:的距离为3. (1)求m的值. (2)设P是直线l上的动点,点Q在线段OP上,满足,求点Q的
- Like a backward tape, time returns to my mom's teens.She
- 酒精测试仪用于对机动车驾驶人员是否酗酒及其他严禁酒后作业人员的现场检测,它利用的是一种二氧化锡半导体型酒精气体传感器.酒
- 空气成分中,体积分数约占78%的是 A.氧气 B.氮气 C.二氧化碳



