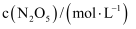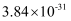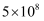化学反应速率与化学平衡的综合应用 知识点题库
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼(CH3)2N﹣NH2 , 氧化剂是液态四氧化二氮.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体.已知室温下,1g燃料完全燃烧释放出的能量为42.5kJ,请写出该反应的热化学方程式
(2)298K时,在2L的密闭容器中,发生可逆反应2NO2(g)⇌N2O4(g)△H=﹣a kJ•mol﹣1 (a>0).N2O4的物质的量浓度随时间变化如图1.达平衡时,N2O4的浓度为NO2的2倍,回答下列问题.
①298k时,该反应的平衡常数为
②在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图2所示.下列说法正确的是
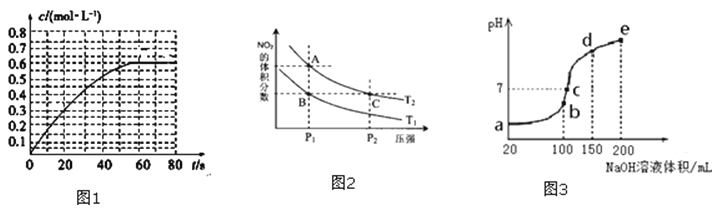
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B<C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
③若反应在398K进行,某时刻测得n(NO2)=0.6mol n(N2O4)=1.2mol,则此时V(正) V(逆)(填“>”、“<”或“=”).
(3)NH4HSO4在分析试剂、医药、电子工业中用途广泛.现向100mL 0.1mol•L﹣1NH4HSO4溶液中滴加0.1mol•L﹣1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示.试分析图中a、b、c、d、e五个点,
①水的电离程度最大的是
②其溶液中c(OH﹣)的数值最接近NH3•H2O的电离常数K数值的是
③在c点,溶液中各离子浓度由大到小的排列顺序是
I. 利用反应:6NO2 + 8NH3  7N2 + 12 H2O处理NO2。
7N2 + 12 H2O处理NO2。
II. 一定条件下NO2与SO2可发生反应:NO2(g)+SO2(g)  SO3(g)+NO(g) −Q (Q>0) 。
SO3(g)+NO(g) −Q (Q>0) 。
III. CO可用于合成甲醇,反应方程式为:CO(g) + 2H2(g)  CH3OH(g) 。
CH3OH(g) 。
-
(1) 硫离子最外层电子的电子排布式为,氨气分子的电子式为,氨气分子属于分子(填“极性”或者“非极性”)。
-
(2) C、O、S、N这四种元素中属于同周期元素的非金属性由强到弱的顺序为,能证明其递变规律的事实是()
a、最高价氧化物对应水化物的酸性 b、气态氢化物的沸点
c、单质与氢气反应的难易程度 d、其两两组合形成的化合物中元素的化合价
-
(3) 对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2) =。
-
(4) 对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是
a. 体系压强保持不变
b. NO2浓度保持不变
c. NO2和SO3的体积比保持不变
d. 混合气体的平均相对分子质量保持不变
-
(5) 请写出II中反应的平衡常数表达式K=。如果II中反应的平衡常数K值变大,该反应
a.一定向正反应方向移动
b. 平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动
d. 平衡移动时,逆反应速率先增大后减小
-
(6) 对于III中的反应,CO在不同温度下的平衡转化率与压强的关系如图示。
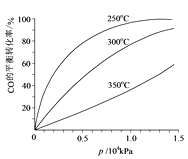
实际生产条件控制在250℃、1.3×104 kPa左右,简述选择此压强的理由:。
 HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
B . 对CO(g)+NO2(g)
HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅
B . 对CO(g)+NO2(g)  CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C . 对2NO2(g)
CO2(g)+NO(g),平衡体系增大压强可使颜色变深
C . 对2NO2(g)  N2O4(g) △H<0, 升高温度平衡体系颜色变深
D . SO2催化氧化成SO3的反应,往往加入过量的空气
N2O4(g) △H<0, 升高温度平衡体系颜色变深
D . SO2催化氧化成SO3的反应,往往加入过量的空气
 CH3OH(g)+H2O(g),下列说法正确的是( )
CH3OH(g)+H2O(g),下列说法正确的是( )

-
(1) 甲醇燃料电池(DNFC)被认为是21世纪电动汽车最佳候选动力源。在25℃、101kPa下,1g甲醇(CH3OH)燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为。
-
(2) 工业上一般可采用下列反应来合成甲醇:CO(g)+2H2(g)⇌CH3OH(g),现实验室模拟该反应并进行分析,如图是该反应在不同温度下CO的转化率随时间变化的曲线。
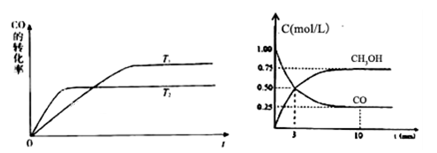
①该反应的焓变△H0(填“>”“<”或“=”).
②T1和T2温度下的平衡常数大小关系是K1K2(填“>”“<”或“=”)
③现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2 , 测得CO和CH3OH(g)的浓度随时间变化如图所示.从反应开始到平衡,CO的平均反应速率v(CO)=,该反应的平衡常数为K=。
-
(1) 汽车尾气中的 NO和CO可在催化剂作用下生成无污染的气体而除去。在密闭容器中充入10 mol CO和8 mol NO发生反应,测得平衡时NO的体积分数与温度、压强的关系如图。
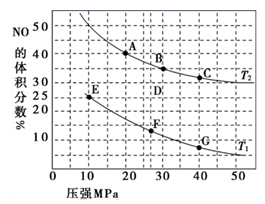
①已知该反应在较低温度下能自发进行,则反应 2NO(g)+2CO(g)
 N2(g)+2CO2 (g),ΔH0(填“>” “=”或“<”)。
N2(g)+2CO2 (g),ΔH0(填“>” “=”或“<”)。②该反应达到平衡后,为同时提高反应速率和CO的转化率,可采取的措施有 (填字母序号)
a.改用高效催化剂 b.缩小容器的体积 c.增加 NO 的浓度 d.升高温度
-
(2) 在有氧条件下,新型催化剂M能催化NH3与NOx反应生成N2 , 将一定比例的O2、NH3 和NOx的混合气体匀速通入装有催化剂M的反应器中反应,反应相同时间,NOx的去除率随反应温度的变化曲线如图所示。

解释在50 ℃~150 ℃范围内随温度升高,NOx 的去除率迅速上升的原因是
-
(3) NH3催化还原氮氧化物技术是目前应用最广泛的烟气脱氮技术:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) ΔH<0。密闭容器中,在相同时间内,在催化剂 A作用下脱氮率随温度变化如图所示。
5N2(g)+6H2O(g) ΔH<0。密闭容器中,在相同时间内,在催化剂 A作用下脱氮率随温度变化如图所示。 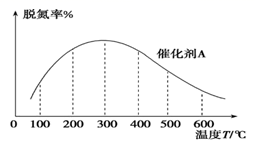
现改用催化能力稍弱的催化剂B进行实验,请在上图中画出在催化剂 B作用下的脱氮率随温度变化的曲线(不考虑温度对催化剂活性的影响)。
-
(4) 某研究小组利用反应:C(s)+2NO(g)
 N2(g)+CO2(g) △ H= -34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得 NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) △ H= -34.0 kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒压测得 NO的转化率随温度的变化如图所示: 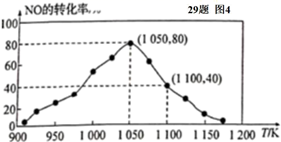
①由图可知,在 1050 K 前,反应中 NO的转化率随温度升高而增大,其原因为; 在 1100 K 时,N2的体积分数为。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作 Kp )。在 1050 K、1.1×106 Pa 时,该反应的化学平衡常数 Kp=(已知:气体分压(P分) =气体总压(Pa)×体积分数)
-
(1) 已知:CO2(g)+H2(g)
 H2O(g) +CO(g) ΔH1= + 41.1 kJ•mol-1 CO(g)+2H2(g)
H2O(g) +CO(g) ΔH1= + 41.1 kJ•mol-1 CO(g)+2H2(g)  CH3OH(g) ΔH2=-90.0 kJ•mol-1
CH3OH(g) ΔH2=-90.0 kJ•mol-1 写出CO2催化氢化合成甲醇的热化学方程式:。
-
(2) 为提高CH3OH产率,理论上应采用的条件是_______________________(填字母)。A . 高温高压 B . 低温低压 C . 高温低压 D . 低温高压
-
(3) 250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),下图为不同投料比[n(H2)/n(CO2)]时某反应物X 平衡转化率变化曲线。
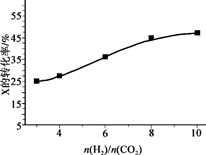
① 反应物X 是(填“CO2”或“H2”)。
② 判断依据是。
-
(4) 250℃、在体积为 2.0L 的恒容密闭容器中加入6mol H2、2mol CO2和催化剂,10min 时反应达到平衡,测得 c(CH3OH) = 0.75 mol·L-1。
① 前 10min 的平均反应速率 v(H2)=mol·L-1·min-1。
② 经计算化学平衡常数 K =。
③ 催化剂和反应条件与反应物转化率和产物的选择性有高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
实验编号
温度(K)
催化剂
CO2转化率(%)
甲醇选择性(%)
A
543
Cu/ZnO 纳米棒
12.3
42.3
B
543
Cu/ZnO 纳米片
11.9
72.7
C
553
Cu/ZnO 纳米棒
15.3
39.1
D
553
Cu/ZnO 纳米片
12.0
70.6
(注:甲醇选择性是指的是转化的CO2中生成甲醇的百分含量)
根据上表所给数据,用CO2生产甲醇的最优选项为(填字母)。
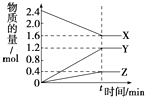
 a Z(g)。起始时容器的体积为V L,达到平衡时X、Y、Z的物质的量之比为1:3:2,且容器的体积仍然为V L。请回答下列问题:
a Z(g)。起始时容器的体积为V L,达到平衡时X、Y、Z的物质的量之比为1:3:2,且容器的体积仍然为V L。请回答下列问题: 
-
(1) a = ;
-
(2) 平衡时Y的转化率=
-
(3) X的状态为,Y的状态为(填“气态”或“非气态”)
-
(4) 下列叙述中,能说明上述反应达到平衡状态的是(填编号)
a.气体密度不变 b.单位时间内消耗2mol X,同时生成amol Z
c.Y的转化率不再变化 d.Z的浓度不再变化
e.气体的质量不随时间的变化而变化
-
(1) Ⅰ.①图1是由
 制取C的太阳能工艺。已知过程1中
制取C的太阳能工艺。已知过程1中 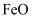 与
与  反应时
反应时  ,则
,则  的化学式为。
的化学式为。
②过程1生成
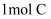 的反应热为
的反应热为  ;过程2产生
;过程2产生 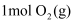 的反应热为
的反应热为  。则制取C的反应
。则制取C的反应 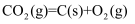 的
的 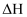 为。
为。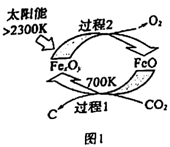
-
(2) Ⅱ.以
 和
和  为原料合成尿素的化学方程式为
为原料合成尿素的化学方程式为  。
。
合成的粗尿素中含有
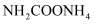 杂质。通过控制温度和压强,可将
杂质。通过控制温度和压强,可将 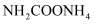 分解为
分解为  和
和  。研究温度和压强对
。研究温度和压强对 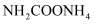 分解率的影响,结果如下:
分解率的影响,结果如下: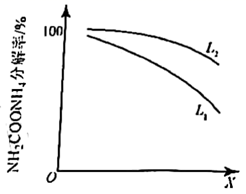
若X代表压强,则温度:
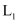
 (填“>”或“<”)。
(填“>”或“<”)。 -
(3) 工业上含尿素的废水需经处理后才能排放。如图为一种电化学降解尿素的装置示意图,该过程中,尿素降解的产物之一为
 :
:
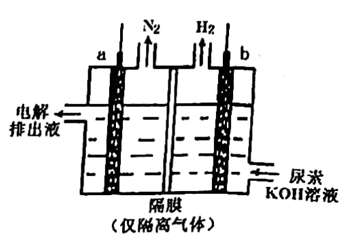
写出尿素被降解的电极反应式:。
-
(4) Ⅲ.在200℃时,向
 带气压计的恒容密闭容器中通入
带气压计的恒容密闭容器中通入 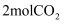 和
和 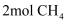 发生反应
发生反应  ,测得初始压强为
,测得初始压强为  ,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。
,反应过程中容器内总压强(P)随时间(t)变化(反应达到平衡时的温度与起始温度相同)如图所示。
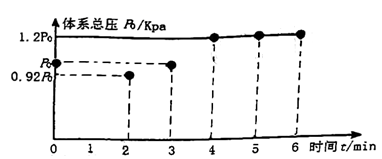
该反应过程中从
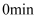 到
到 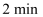 压强变小原因是。
压强变小原因是。 -
(5)
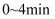 内,反应的平均反应速率
内,反应的平均反应速率  。
。
-
(6) 用平衡分压代替平衡浓度表示的化学平衡常数
 。[气体分压
。[气体分压 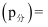 气体总压
气体总压  气体体积分数]
气体体积分数]
-
(1) 甲醇制取绿色能源氢气的部分反应过程如图1所示:
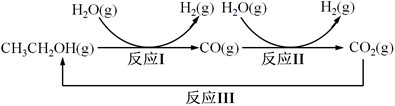
图1
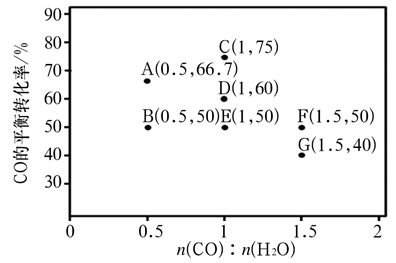
图2
已知:Ⅰ.CH3OH(g)
 CO(g)+2H2(g)△H1=+90.4kJ•mol-1
CO(g)+2H2(g)△H1=+90.4kJ•mol-1Ⅱ.CO(g)+H2O(g)
 CO2(g)+H2(g)△H2=-41kJ•mol-1
CO2(g)+H2(g)△H2=-41kJ•mol-1反应Ⅲ的热化学方程为。
-
(2) 在恒压密闭容器中,反应Ⅱ的进气比
 同时,测得相应的CO的平衡转化率如图2所示(各点对应的反应条件除温度可能不同外,其余都相同)
同时,测得相应的CO的平衡转化率如图2所示(各点对应的反应条件除温度可能不同外,其余都相同) ①图中A、D和F三点对应的反应温度TA、TD、TF的关系是,其原因是。
②CO的平衡转化率与进气比、反应温度之间的关系是。
③C、D两点对应的反应速率大小:vCvD(填“>”“<”或“=”)。
已知反应速率v=v正-v逆=k正•x(CO)•x(H2O)-k逆•x(CO2)•x(H2),其中k为反应速率常数、x为物质的量分数,在达到平衡状态为D点的反应过程中,当CO的转化率刚好达到20%时,
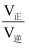 =(结果保留3位有效数字)。
=(结果保留3位有效数字)。
-
(1) 已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)→CH2ClCHClCH3(g) ΔH=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)→CH2=CHCH2Cl(g)+HCl(g) ΔH=-100kJ·mol-1
①写出相同条件下CH2=CHCH2Cl和HCl合成CH2ClCHClCH3的热化学方程式。
②已知①中的正反应的活化能E正为132kJ·mol-1 , 请在下图中标出①中逆反应的活化能E逆及数值。
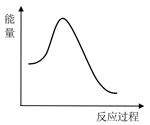
-
(2) 温度为T℃时向容积为2L的密闭容器中投入3molH2和1molCO2发生反应CO2(g)+3H2(g)⇌ CH3OH(g)+H2O(g) ΔH1=-49.4kJ·mol-1 , 反应达到平衡时,测得放出热量19.76kJ,求平衡时:
①H2的转化率为
②T℃时该反应的平衡常数K=(列计算式表示)。
-
(3) 目前有Ni-CeO2催化CO2加H2形成CH4的反应,历程如图所示,吸附在催化剂表面的物种用*标注。
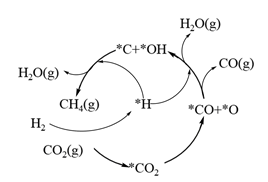
①写出上述转换中存在的主要反应的化学方程式。
②有人提出中间产物CO的处理,用反应2CO(g)=2C(s)+O2(g) ΔH>0来消除CO的污染,请用文字说明是否可行。
-
(4) T℃,HCOOH与CH3COONa溶液反应:HCOOH+CH3COO-⇌HCOO-+CH3COOH,该反应的K=12.5,则该温度下醋酸的电离常数Ka(CH3COOH)=(T℃时Ka(HCOOH)=2×10-4)。
 CH3CH2OH(g)+ 3H2O(g)。下列叙述正确的是( )
CH3CH2OH(g)+ 3H2O(g)。下列叙述正确的是( )
-
(1) 工业上用SiO2与碳反应制粗硅的反应为:SiO2(s)+2C(s)=Si(s)+2CO(g) ΔH。
已知:2C(s)+O2(g)=2CO(g) ΔH1=-221kJ·mol-1
Si(s)+O2(g)=SiO2(s) ΔH2=-911kJ·mol-1
则ΔH=。制备粗硅的反应能自发进行的条件是(填“高温”、“低温”或“任意温度”)。
-
(2) 由SiO2生成Si的部分反应机理如下:
反应1:SiO2(s)+C(s)
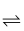 SiO(g)+CO(g)
SiO(g)+CO(g)反应2:SiO(g)+2C(s)
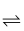 SiC(s)+CO(g)
SiC(s)+CO(g)反应3:……
在压强为10MPa条件下,测得反应平衡体系中SiO(g)和CO(g)的分压比
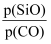 随温度的变化关系如图所示。
随温度的变化关系如图所示。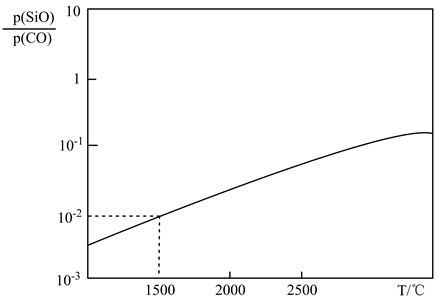
假设体系中只有SiO和CO为气体,则在1500℃时,用各物质的平衡分压表示反应1的平衡常数Kp=MPa2(列出计算式即可)。
-
(3) 硅烷法制备多晶硅的核心反应为:2SiHCl3(g)
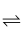 SiH2Cl2(g)+SiCl4(g)。在恒容密闭容器中加入一定量的SiHCl3 , 分别在50℃和70℃进行反应,测得SiHCl3的转化率随时间的变化关系如图所示。
SiH2Cl2(g)+SiCl4(g)。在恒容密闭容器中加入一定量的SiHCl3 , 分别在50℃和70℃进行反应,测得SiHCl3的转化率随时间的变化关系如图所示。
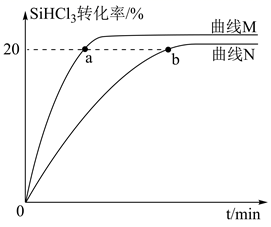
已知:50℃时,平衡常数为0.02;70℃时,平衡常数为0.04。
①代表温度为70℃的曲线是(填“M”或“N”)。
②a点和b点对应的容器中,
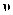 正(a)
正(a)
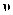 正(b)(填“>”、“<”或“=”),理由是。
正(b)(填“>”、“<”或“=”),理由是。③曲线M对应的SiHCl3平衡转化率为。(保留两位有效数字)
④已知:该反应的速率
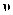 正=k正•x2(SiHCl3),
正=k正•x2(SiHCl3),
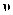 逆=k逆•x(SiH2Cl2)•x(SiCl4),k正、k逆分别为正、逆反应速率常数,x为物质的量分数,且平衡常数K=
逆=k逆•x(SiH2Cl2)•x(SiCl4),k正、k逆分别为正、逆反应速率常数,x为物质的量分数,且平衡常数K=
 。则b点时的
。则b点时的
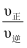 =。
=。
 是一种新型硝化剂,在一定温度下可发生如下反应:
是一种新型硝化剂,在一定温度下可发生如下反应:
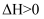 。
。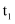 温度时,向密闭容器中通入一定量的
温度时,向密闭容器中通入一定量的 气体,反应时间以及对应
气体,反应时间以及对应 的浓度数据见下表:
的浓度数据见下表:时间/s | 0 | 500 | 1000 | 1500 |
| 5.00 | 3.52 | 2.50 | 2.50 |
下列说法正确的是( )
 的生成速率为
的生成速率为 B .
B . 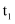 温度下该反应平衡时
温度下该反应平衡时 的转化率为29.6%
C . 达到平衡后其他条件不变,将容器的体积压缩到原来的1/2,则
的转化率为29.6%
C . 达到平衡后其他条件不变,将容器的体积压缩到原来的1/2,则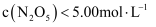 D .
D . 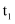 温度下的平衡常数为
温度下的平衡常数为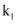 ,
,  温度下的平衡常数为
温度下的平衡常数为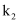 , 若
, 若 , 则
, 则
-
(1) 次氯酸钠氧化法可以制备Na2FeO4。
已知:2H2(g) +O2(g)=2H2O(l) ΔH=a kJ·mol-1
NaCl(aq)+H2O(l)=NaClO(aq)+ H2(g) ΔH =b kJ·mol-1
4Na2FeO4 (aq) + 10H2O(l)=4Fe(OH)3(s) +3O2 (g)十8NaOH(aq) ΔH=c kJ·mol-1
反应2Fe(OH)3(s)十3NaClO(aq) + 4NaOH(aq)=2Na2FeO4 (aq) + 3NaCl(aq) +5H2O(l)的 △H=kJ·mol-1。
-
(2) 光气(COCl2)是重要的含氯化合物。常用于医药、农药制造,工业上利用一氧化碳和氯气反应制备,反应方程式为CO(g)+Cl2(g)
 COCl2(g)。在1 L恒温恒容密闭容器 中充入2.5molCO和1.5molCl2 , 在催化剂作用下发生反应,测得CO及COCl2的物质的量随时间变化如图1所示:
COCl2(g)。在1 L恒温恒容密闭容器 中充入2.5molCO和1.5molCl2 , 在催化剂作用下发生反应,测得CO及COCl2的物质的量随时间变化如图1所示: 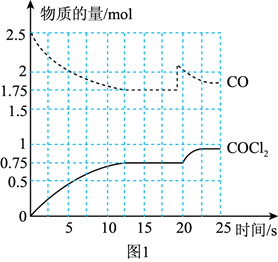
①0~15s内,Cl2的平均反应速率为mol· L-1·min-1
②第一次平衡时,CO的平衡转化率为;此温度下,该反应的平衡常数KC=(保留两位有效数字)。
③在第20 s时,改变的条件是。
-
(3) 工业上常用氯苯(C6H5-Cl)和硫化氢(H2S)反应来制备一种用途广泛的有机合成中间体苯硫酚(C6H5-SH) ,但会有副产物苯(C6 H6)生成。
Ⅰ.C6H5-Cl(g)+H2S(g
 C6H5-SH(g)+HCl(g) ΔH1= -16.8 kJ·mol-1;
C6H5-SH(g)+HCl(g) ΔH1= -16.8 kJ·mol-1; Ⅱ.C6H5- Cl(g)+ H2S(g)=C6H6(g)+HCl(g)+
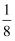 S8(g) △H2= - 45.8 kJ·mol-1。
S8(g) △H2= - 45.8 kJ·mol-1。①将一定量的C6H5-Cl和H2S的混合气体充入恒容的密闭容器中,控制反应温度为T(假设只发生反应Ⅰ),下列可以作为反应Ⅰ达到平衡的判据是(填字母)。
A.气体的压强不变 B.平衡常数不变
C. v正(H2S)= v逆(HCl) D.容器内气体密度不变
②现将一定量的C6H5-Cl和H2S置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20 min测定生成物的浓度,得到图2和图3。
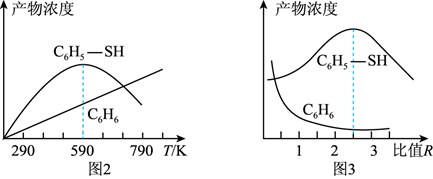
(R为H2S与C6H6-Cl的起始物质的量之比),图2显示温度较低时C6H5-SH浓度的增加程度大于C6H6 , 从活化能角度分析其主要原因是;结合图2和图3,该模拟工业生产制备C6H5 - SH的适宜条件为。
-
(1) 氢气是一种环保的气体,不会污染大气且热值高。相关化学键的键能表示如表:
化学键
O=O
H—H
O—H
键能E/(kJ·mol-1)
a
b
c
则氢气燃烧热的△H=kJ/mol(用含a、b、c代数式表示)
-
(2) 催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1。在T1℃时,将0.10molCO与0.40molH2O充入5L的容器中,反应平衡后H2的物质的量分数x(H2)=0.08。
CO2(g)+H2(g) ΔH2=-41.2kJ·mol-1。在T1℃时,将0.10molCO与0.40molH2O充入5L的容器中,反应平衡后H2的物质的量分数x(H2)=0.08。①反应平衡常数K=。(结果保留2位有效数字)
②保持K不变,提高CO平衡转化率措施有:。(任意一条)
③由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用如图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为。(填字母)
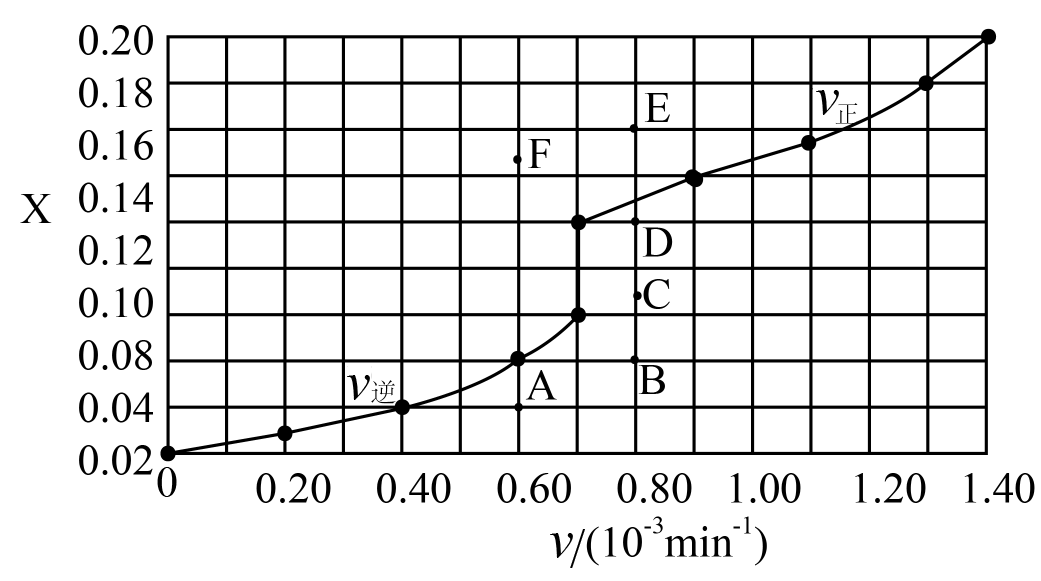
④研究表明,CO催化变换反应的速率方程为:v=k[x(CO)•x(H2O)-
 ],式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,KP为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的KP(填“增大”或“减小”或“不变”)。根据速率方程分析,T>Tm时v逐渐减小的原因是。
],式中,x(CO)、x(H2O)、x(CO2)、x(H2)分别表示相应的物质的量分数,KP为平衡常数,k为反应的速率常数,温度升高时k值增大。在气体组成和催化剂一定的情况下,反应速率随温度变化的曲线如图所示。温度升高时,CO催化变换反应的KP(填“增大”或“减小”或“不变”)。根据速率方程分析,T>Tm时v逐渐减小的原因是。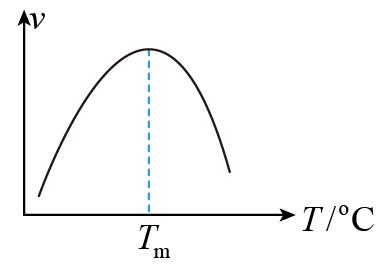
-
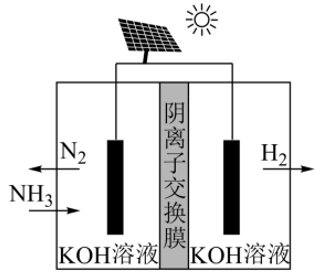
(3) 氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示。阳极的电极反应式为。
反应 | 大气固氮 | 工业固氮 | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
平衡常数/K |
| 0.1 |
| 0.507 | 0.152 |
-
(1) 分析上表数据,回答下列问题。
①大气固氮反应不适合大规模工业生产,可能原因是;
②工业固氮需在高温、有催化剂的条件下进行,主要目的是。
-
(2) 工业固氮反应中,其他条件相同时,分别测定
 的平衡转化率在不同压强下随温度变化的曲线,则下图中正确的是图(填“甲”或“乙”),p1、p2的大小关系为。
的平衡转化率在不同压强下随温度变化的曲线,则下图中正确的是图(填“甲”或“乙”),p1、p2的大小关系为。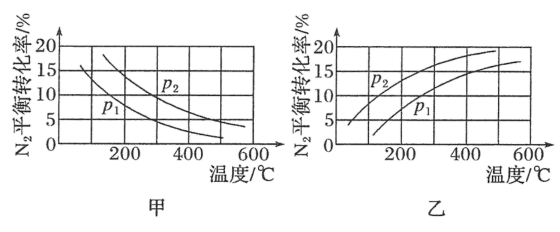
-
(3) 在一定温度下,将
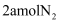 和
和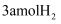 混合置于一体积不变的密闭容器中发生反应
混合置于一体积不变的密闭容器中发生反应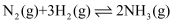 , 达到平衡后,测得气体总物质的量为4amol。计算:
, 达到平衡后,测得气体总物质的量为4amol。计算:①平衡时,
 的转化率为;
的转化率为;②平衡时,若容器中气体总压强为P,则压强平衡常数Kp=(用平衡分压代替平衡浓度计算,平衡分压=总压×物质的量分数。
- 暑假期间李丽要去参观艺术宝库莫高窟,你您告诉她应该去哪儿吗?A.山西大同B.甘肃敦煌C.河南洛阳D.陕西西安
- 植物进行呼吸作用的主要场所是() A.叶绿体B.线粒体C.细胞质D.细胞核
- 糖类的概念从分子结构上看,糖类可定义为_______、_______和它们的脱水缩合物。
- 他被称为是站在文明门槛上的一位伟人,他还具有“部落联盟首领”和“奴隶制国家国王”的双重身份。“他”是( ) A.黄帝
- 下列对实验现象的预测不正确的是( )A.向Na2SiO3溶液中通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失B.向
- 阅读下面的文字,按提示和要求作文。 钥匙是开锁的工具,它更是解决问题的方法、策略、条件、思想……生活中,书籍是一
- 用18O标记的H2O浇灌植物,在光照充足的条件下,植物体内及周围空气中存在18O同位素的物质及其相应生理过程的叙述中,不
- 对下列电解质溶液的叙述错误的是 A.等物质的量浓度的Na2CO3和NaHCO3混合液中:c(Na+)>c(HCO3
- 下列各组物质性质的比较中,不正确的是 A.热稳定性:SiH4<PH
- 镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳,越来越成为人们研制绿色原电池的关注焦点。其中一种镁
- 下图是世界某地一月等温线图,其中①是25℃等温线,②是20℃等温线,回答下列各题。②等温线明显与海岸线平行的主要原因是
- 下面各组词语中,有两个错别字的一组是() A.抵砺 再接再励 严厉 励精图治 B.卓见 真知灼见 流传 流传千古 C.妥
- 2010年8月20日,为期3天的第四届国际生态城市建设论坛在河北承德闭幕。承德市凭借突出的生态优势以及建设生态城市的丰富
- 某文具厂加工一种文具2500套,加工完1 000套后,由于采用了新设备,每天的工作效率变为原来的1.5倍,结果提前5天完
- 成都所属的干湿地区是( ) A、湿润地区 B、半湿润地区 C、干旱地区 D、半
- 反应5NH4NO32HNO3+4N2↑+9H2O中,还原产物与氧化产物的物质的量之为() A.2∶1 B.
- 关于易燃和易爆物品的生产、使用、运输、贮存方法不正确的是()。 A.存放时要露天放置,紧密堆积 B.搬运取用时要轻拿轻放
- 如图所示温度计的使用情况中正确的是( )
- ____team wins on Saturday will go through to the national ch
- 现有一束由a粒子、质子、电子组成的粒子束各自以一定的初速度垂直进入一正交的匀强磁场和匀强电场正方体区域,则下列判断正确的