化学平衡移动原理 知识点题库
-
(1)
某经济开发区将钛冶炼厂与氯碱厂、甲醇厂组成了一个产业链(如图1所示),大大地提高了资源利用率,减少了环境污染.
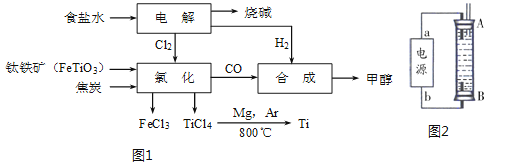
①由CO和H2合成甲醇的方程式是:CO(g)+2H2(g)⇌CH3OH(g).
已知该反应在300℃时的化学平衡常数为0.27,该温度下将2mol CO、3mol H2和2mol CH3OH充入容积为2L的密闭容器中,此时反应将 (填“向正反应方向进行”、“向逆反应方向进行”或“处于平衡状态”).
②写出钛铁矿经氯化得到四氯化钛的化学方程式:
③若不考虑生产过程中物质的任何损失,该产业链中每合成38.4t甲醇,至少需额外补充H2 t.
-
(2) 将两个石墨电极插入H2SO4溶液中,向两极分别通入C3H8和O2 , 构成丙烷燃料电池.
①负极电极反应式是: ;
②某同学利用丙烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如图2所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色.下列说法中正确的是 (填序号)
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H++2e﹣═H2↑
-
(3) 将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g)⇌CO2(g)+H2(g),得到如下三组数据:
实验组
温度/℃
起始量/mol
平衡量/mol
达到平衡所需时间/min
H2O
CO
CO2
1
650
2
4
1.6
5
2
900
1
2
0.4
3
3
900
1
2
0.4
1
①该反应的正反应为 (填“吸”或“放”)热反应;
②实验2中,平衡常数K= ;
③实验3跟实验2相比,改变的条件可能是 (答一种情况即可).
 Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是( )
Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是( )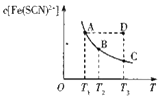
 2B(g)+E(g) ΔH>0,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
2B(g)+E(g) ΔH>0,达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是( )
 NaUr(s) + H+(aq) +Q (Q>0),下列说法错误的是( )
NaUr(s) + H+(aq) +Q (Q>0),下列说法错误的是( )
 2NO2(g),当c(N2O4)∶c(NO2)=1∶2时,该可逆反应到达限度
C . 碱性N2H4—空气燃料电池工作时,正极电极反应式为O2+2H2O+4e-=4OH-
D . N2H4的水溶液中存在:N2H4+H2O
2NO2(g),当c(N2O4)∶c(NO2)=1∶2时,该可逆反应到达限度
C . 碱性N2H4—空气燃料电池工作时,正极电极反应式为O2+2H2O+4e-=4OH-
D . N2H4的水溶液中存在:N2H4+H2O  N2H
N2H 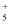 +OH- , 向稀溶液中加水稀释,
+OH- , 向稀溶液中加水稀释, 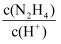 的值变大
的值变大
 2CuBr(s)+Br2(g)达到平衡。保持温度不变,缩小容器体积,体系重新达到平衡,下列说法正确的是( )
2CuBr(s)+Br2(g)达到平衡。保持温度不变,缩小容器体积,体系重新达到平衡,下列说法正确的是( )
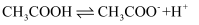 ΔH>0,25℃时,Ka=1.75×10-5 , 是该温度下醋酸的电离平衡常数(Ka)。下列说法正确的是( )
ΔH>0,25℃时,Ka=1.75×10-5 , 是该温度下醋酸的电离平衡常数(Ka)。下列说法正确的是( )
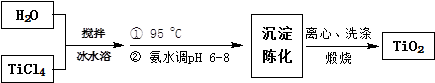
 溶液中再加入
溶液中再加入  B .
B . 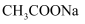 溶液加热
C . 氨水中加入少量
溶液加热
C . 氨水中加入少量  固体
D . 醋酸溶液加热
固体
D . 醋酸溶液加热
①CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H1=-49.5 kJ/mol
②CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4 kJ/mol
③CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
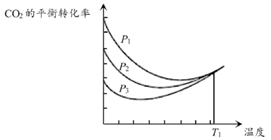
不同压强下,按照n(CO2):n(H2)=1:3投料,CO2平衡转化率随温度变化关系如图。下列说法正确的是( )
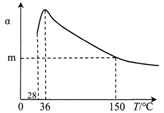
| 名称 | 熔点/℃ | 沸点/℃ | 燃烧热 ∆H /kJ•mol-1 |
| 正戊烷 | -130 | 36 | –3506.1 |
| 异戊烷 | -159.4 | 27.8 | –3504.1 |
下列说法错误的是( )
-
(1) 上述四种气体中直接排入空气时会引起酸雨的有(填化学式)。
-
(2) 已知:2SO2(g)+O2(g)
 2SO3(g) ∆H=- 196.6 kJ∙mol-1
2SO3(g) ∆H=- 196.6 kJ∙mol-1 2NO(g)+ O2(g)
 2NO2(g) ∆H=-113.0 kJ∙mol-1
2NO2(g) ∆H=-113.0 kJ∙mol-1①反应:NO2(g)+ SO2(g)
 SO3(g)+ NO(g)的∆H=kJ∙mol-1。
SO3(g)+ NO(g)的∆H=kJ∙mol-1。②一定条件下,将NO2与SO2以体积比1:1置于恒温恒容的密闭容器中发生反应:NO2(g)+ SO2(g)
 SO3(g)+NO(g),下列能说明反应达到平衡状态的是(填字母)。
SO3(g)+NO(g),下列能说明反应达到平衡状态的是(填字母)。a.混合气体的密度保持不变 b.SO2的物质的量保持不变
c.容器内混合气体原子总数不变 d.每生成1molSO3的同时消耗1mol NO
③测得②中反应达到平衡时NO与NO2的体积之比为37:13,则在该温度下反应:NO2(g)+ SO2(g)
 SO3(g)+NO(g)的平衡常数K=
SO3(g)+NO(g)的平衡常数K= -
(3) CO可用于合成甲醇,其反应的化学方程式为CO(g) +2H2(g)
 CH3OH(g)。 在一容积可变的密闭容器中充有10molCO与20molH2 , 在催化剂作用下发生反应生成甲醇。CO的平衡转化率(
CH3OH(g)。 在一容积可变的密闭容器中充有10molCO与20molH2 , 在催化剂作用下发生反应生成甲醇。CO的平衡转化率( 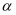 )与温度(T)、压强(p)的关系如图所示。下列说法正确的是_______(填字母)。
)与温度(T)、压强(p)的关系如图所示。下列说法正确的是_______(填字母)。 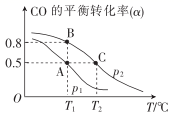 A . 合成甲醇的反应为吸热反应 B . 压强为p1>p2 C . A,B,C三点的平衡常数为KA= KB> KC D . 若达平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积也为10 L
A . 合成甲醇的反应为吸热反应 B . 压强为p1>p2 C . A,B,C三点的平衡常数为KA= KB> KC D . 若达平衡状态A时,容器的体积为10 L,则在平衡状态B时容器的体积也为10 L
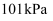 和
和 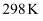 下,
下, 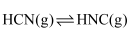 异构化反应过程的能量变化如图所示。下列说法错误的是( )
异构化反应过程的能量变化如图所示。下列说法错误的是( ) 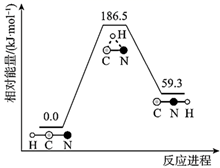
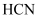 比
比 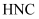 稳定
B . 该异构化反应的
稳定
B . 该异构化反应的 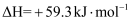 C . 低温下有利于
C . 低温下有利于 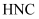 的生成
D . 使用催化剂可以改变反应的活化能
的生成
D . 使用催化剂可以改变反应的活化能
 NO2+SO2
NO2+SO2
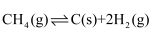
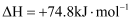 , 以下叙述正确的是( )
, 以下叙述正确的是( )
 的生成速率是
的生成速率是 消耗速率的2倍时,说明反应达到了平衡状态
B . 反应达平衡时,恒温恒容下加入
消耗速率的2倍时,说明反应达到了平衡状态
B . 反应达平衡时,恒温恒容下加入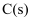 , 会加快逆反应速率,使平衡逆向移动
C . 反应达平衡时,恒温恒压下通入惰性气体,正反应速率减慢,平衡正向移动
D . 正反应活化能小于逆反应活化能
, 会加快逆反应速率,使平衡逆向移动
C . 反应达平衡时,恒温恒压下通入惰性气体,正反应速率减慢,平衡正向移动
D . 正反应活化能小于逆反应活化能
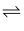 2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是( )
2CO(g)+2H2(g) ΔH>0。温度为T℃时,该反应的平衡常数为K。下列说法正确的是( )
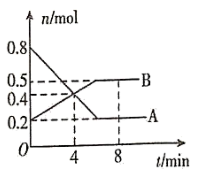
 2B(g)
B . 4min时,A,B速率关系为v(A)=v(B)
C . 8min时,A,B气体物质的量不再变化,反应停止
D . 8min后升高温度,平衡会发生移动
2B(g)
B . 4min时,A,B速率关系为v(A)=v(B)
C . 8min时,A,B气体物质的量不再变化,反应停止
D . 8min后升高温度,平衡会发生移动
 4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2 , 平衡时测得NH3的转化率为60%。下列有关氨催化氧化反应的说法正确的是( )
4NO(g)+6H2O(g) ΔH<0。在T℃时,向1L密闭容器中投入4molNH3、5molO2 , 平衡时测得NH3的转化率为60%。下列有关氨催化氧化反应的说法正确的是( )
- 美国历史学家斯塔夫里阿诺斯说:“奥斯曼及其后继者的力量大部分来自源源而来的伊斯兰教勇士。他们不断地从中东各地前来与伊斯兰
- 已知函数,则方程 的根的个数不可能为( ) A.6个 B.5个 C.4个
- 在如图所示的一些常见物质之间的转化关系中(有些反应中的水、部分产物及反应条件未列出)。 已知反应①是工业制硫
- 下列说法正确的是A.物质的量浓度均为0.1mol·L-1的(NH4)2SO4、(NH4)2Fe(SO4)2两种溶液中,c
- 用配方法解下列方程,其中应在左右两边同时加上4的是 ( ) A. B. C. D.
- 在用“打点计时器验证机械能守恒定律”的实验中,质量为m=1.00kg的重物拖着纸带竖直下落,打点计时器在纸带上打下一系列
- 2012年10月25日,我国在西昌卫星发射中心成功将一颗北斗导航卫星发射升空并送入预定转移轨道。这是一颗地球静止轨道卫
- When you think about math, you probably don’t think about br
- 下列各项成语意思相近的一项是( ) A.大吹大擂 大言不惭 大摇大摆
- 专家表示:“老百姓对食品、药品、日用品安全性信任的重建,是一个反复、长期的过程。”这是因为() ①认识具有反复性、上升性
- 如图,AB为⊙O的直径,劣弧,BD∥CE,连接AE并延长交BD于D. (1)求证:BD是⊙O的切线; (2)若⊙O的半径
- 根尖吸收水分和无机盐的主要部位是A.根冠 B.成熟区 C.
- Having a goodEnglish dictionary is important if you wan
- 作文(40分) 题目:妈妈的眼睛 作文要求:(1)要有真情实感,要努力做到有新意有创见。(2)除诗歌外文体不限。(3)字
- 已知函数 (I)求函数的最小正周期; (Ⅱ)求使函数取得最大值的的集合.
- (6分)取一定量的CuO粉末与0.5 L稀硫酸充分反应后,将一根50 g铁棒插入上述溶液中,至铁棒质量不再变化时,铁棒增
- William Shakespeare occupies a(n) ______ place in drama. A.
- In some foreign countries, some people don't like the number
- 过犹不及在哲学上符合( )的辩证关系 A内因和外因 B量变和质变 C认识和实践
- 和谐社会的重要内容之一是社会公平,教育公平是社会公平的基础。中国古代儒家学派 创始人孔子的思想中,对今天倡导教育公平有



