化学反应速率和化学计量数的关系 知识点题库
在一固定容积的密闭容器中,充入2molA和1molB发生反应:2A(g)+B(g) x C(g),达到平衡时,C的物质的量浓度为0.9mol/L。若维持容器体积和温度不变,按0.6 molA, 0.3molB和1.4 molC为起始物质,达到平衡后,C的物质的量浓度也为0.9mol/L,则x的值为( )
x C(g),达到平衡时,C的物质的量浓度为0.9mol/L。若维持容器体积和温度不变,按0.6 molA, 0.3molB和1.4 molC为起始物质,达到平衡后,C的物质的量浓度也为0.9mol/L,则x的值为( )
A . 只能为2
B . 只能为3
C . 只能为4
D . 可能为2或3
氨分解反应在容积为2L的密闭容器内进行.已知起始时氨气的物质的量为4mol,5秒末为2.4mol,则用氨气表示该反应的速率为( )
A . 0.32 mol•L﹣1•s﹣1
B . 0.16 mol•L﹣1•s﹣1
C . 1.6 mol•L﹣1•s﹣1
D . 0.8 mol•L﹣1•s﹣1
对于反应A2+3B2=2C来说,以下化学反应速率的表示中,反应速率最快的是( )
A . v(B2)=0.8 mol/(L•s)
B . v(A2)=0.4 mol/(L•s)
C . v(C)=0.6 mol/(L•s)
D . v(B2)=4.2 mol/(L•s)
将等物质的量A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5分钟后,测得D的浓度为0.5mol/L,且c(A):c(B)=3:5,C的平均反应速率是0.1mol/(L•min).求:
(1)反应开始前放入容器中A、B物质的量.
(2)B的平均反应速率.
(3)x值是多少?
已知4NH3+5O2═4NO+6H2O,同一反应速率若分别用v(NH3)、v(O2)、v(H2O)、v(NO)(mol•L﹣1•min﹣1)来表示,则正确关系是( )
A . 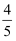 v(NH3)=v(O2)
B .
v(NH3)=v(O2)
B . 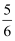 v(O2)=v(H2O)
C .
v(O2)=v(H2O)
C . 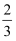 v(NH3)=v(H2O)
D .
v(NH3)=v(H2O)
D . 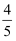 v(O2)=v(NO)
v(O2)=v(NO)
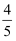 v(NH3)=v(O2)
B .
v(NH3)=v(O2)
B . 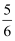 v(O2)=v(H2O)
C .
v(O2)=v(H2O)
C . 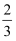 v(NH3)=v(H2O)
D .
v(NH3)=v(H2O)
D . 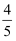 v(O2)=v(NO)
v(O2)=v(NO)
将4mol A气体和2mol B气体在2L的密闭容器内混合,并在一定条件下发生如下反应:2A(g)+B(g)⇌2C(g),若经2s后测得C的浓度为0.6mol/L,现有下列几种说法:
①用物质A表示的反应的平均速率为0.3mol/(L.s)
②用物质B表示的反应的平均速率为0.6mol/(L.s)
③2s内物质A与B的平均速率满足:2v(A)=v(B)
④2s时物质B的浓度为0.7mol/L
其中正确的是( )
A . ①③
B . ①④
C . ②③
D . ③④
可逆反应:3A(g)+B(g)⇌2C(g)+2D(g) 在不同条件下的反应速率分别为:(1)v(A)=0.6mol•L﹣1•min﹣1 ;(2)v(B)=0.007mol•L﹣1•S﹣1;(3)v(C)=0.4mol•L﹣1•min﹣1 ;(4)v(D)=0.80mol•L﹣1•min﹣1 ,
此反应在不同条件下进行最快的是( )
A . (1)
B . (2)
C . (3)
D . (4)
对于反应N2(g)+3H2(g)⇌2NH3(g) 来说,以下化学反应速率的表示中,反应速率最快的是( )
A . v(H2)=0.8mol/(L•s)
B . v(N2)=0.4mol/(L•s)
C . v(NH3)=0.6mol/(L•s)
D . v(H2)=4.2mol/(L•min)
一定条件下,将1mol X气体和1mol Y气体充入一1L的恒容密闭容器中,发生反应:X(g)+2Y(g)⇌3Z(g),1s后测得c(Y)=0.6mol•I﹣1 , 则0~1s内Y的平均反应速率为( )
A . 0.2 mol•L﹣1•s﹣1
B . 0.4 mol•L﹣1•s﹣1
C . 0.6 mol•L﹣1•s﹣1
D . 0.8 mol•L﹣1•s﹣1
某温度时,在一体积不变的容器中充入A、B各1mol,反应进行到10s时,测得容器中含有A:0.8mol;B:0.4mol;C:0.4mol.据此回答该反应的化学方程式为( )
A . A+3B═C
B . 2A+B═C
C . A+3B═2C
D . A+3B═3C
已知某反应的各物质浓度数据如下:
aA(g)+ | bB(g) | 2C(1.0g0) | |
起始(mol/L) | 3.0 | 1.0 | 0 |
2 s末浓度(mol/L) | 1.8 | 0.6 | 0.8 |
据此可推算出上述反应化学方程式中,各物质的化学计量数之比是( )
A . 9∶3∶4
B . 3∶1∶2
C . 2∶1∶3
D . 3∶2∶1
-
(1) 在反应A(g)+3B(g)=2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1 , 则以物质B表示此反应的化学反应速率为 mol·L-1·min-1。
-
(2) 在2 L的密闭容器中,充入2 mol N2和3 mol H2 , 在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的反应速率为。
-
(3) 将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1 , 则在2 s时,容器中有 mol A,此时C的物质的量浓度为。
反应2SO2+O2 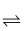 2SO3在密闭容器中进行。下列关于该反应的说法正确的是( )
2SO3在密闭容器中进行。下列关于该反应的说法正确的是( )
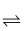 2SO3在密闭容器中进行。下列关于该反应的说法正确的是( )
2SO3在密闭容器中进行。下列关于该反应的说法正确的是( )
A . 增大压强能减慢反应速率
B . 升高温度能减慢反应速率
C . 使用恰当的催化剂能加快反应速率
D . 0.2molSO2与0.1mol O2充分反应生成0.2molSO3
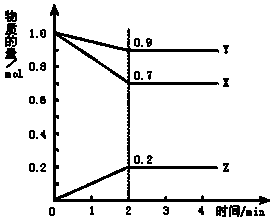
某温度时,在2L容器中X、Y、Z三种物质随时间的变化曲线如下图所示,由图中的数据分析,反应开始至2 min时用Z表示的平均反应速率为,用Y表示的平均反应速率为, 用X表示的平均反应速率为,该反应的化学方程式为。
反应4NH3+5O2 4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的化学速率v为( )
4NO+6H2O在5L的密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的化学速率v为( )
A . v(NH3)= 0.008mol/(L·s)
B . v(O2)= 0.01mol/(L·s)
C . v(NO)= 0.008mol/(L·s)
D . v(H2O)= 0.003mol/(L·s)
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,
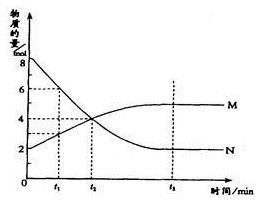
下列表述中正确的是()
A . 反应的化学方程式为2M  N
B . t2时,正逆反应速率相等达到平衡状态
C . t1时,N的浓度是M浓度的2倍
D . t3时,正反应速率大于逆反应速率
N
B . t2时,正逆反应速率相等达到平衡状态
C . t1时,N的浓度是M浓度的2倍
D . t3时,正反应速率大于逆反应速率
 N
B . t2时,正逆反应速率相等达到平衡状态
C . t1时,N的浓度是M浓度的2倍
D . t3时,正反应速率大于逆反应速率
N
B . t2时,正逆反应速率相等达到平衡状态
C . t1时,N的浓度是M浓度的2倍
D . t3时,正反应速率大于逆反应速率
一定温度下,把2.5molA和2.5molB混合盛入容积为2L的密闭容器里,发生如下反应:3A(g)+B(s)  xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1 , 同时生成1molD,下列叙述中错误的是( )
xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1 , 同时生成1molD,下列叙述中错误的是( )
 xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1 , 同时生成1molD,下列叙述中错误的是( )
xC(g)+2D(g),经5s反应达平衡,在此5s内C的平均反应速率为0.2mol·L-1·s-1 , 同时生成1molD,下列叙述中错误的是( )
A . 反应达到平衡状态时A的转化率为60%
B . x=4
C . 若混合气体的密度不再变化,则该可逆反应达到化学平衡状态
D . 反应达到平衡状态时,相同条件下容器内气体的压强与起始时压强比为6∶5
-
(1) I:已知:反应aA(g)+bB(g)
 cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在 2 L 的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。 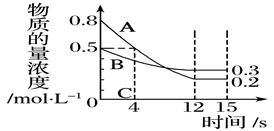
经测定前4 s内v(C)=0.05 mol·L-1·s-1 , 则该反应的化学方程式为
-
(2) 若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1; 乙:v(B)=0.12 mol·L-1·s-1; 丙:v(C)=9.6 mol·L-1·min-1 , 则甲、乙、丙三个容器中反应速率由快到慢的顺序为(用甲、乙、丙表示)。
-
(3) Ⅱ: 某学生为了探究锌与盐酸反应过程中的速率变化,他在100 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气(气体体积已折合成标准状况),实验记录如表(累计值):
时间/min
1
2
3
4
5
6
氢气体积/mL
50
120
224
392
472
502
哪一时间段反应速率最大(填0~1、1~2、2~3、3~4、4~5、5~6 min,下同),原因是
-
(4) 如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,他在盐酸中分别加入等体积的下列溶液,你认为可行的是__________(填字母)A . CH3COONa B . NaNO3溶液 C . KCl溶液 D . Na2CO3溶液
-
(5) Ⅲ:下列说法可以证明H2(g)+I2(g)
 2HI(g)已达平衡状态的是______________________
A . 单位时间内生成n mol H2的同时,生成n mol HI B . 一个H—H键断裂的同时有两个H—I键断裂 C . 温度和体积一定时,混合气体颜色不再变化 D . 反应速率v(H2)=v(I2)=
2HI(g)已达平衡状态的是______________________
A . 单位时间内生成n mol H2的同时,生成n mol HI B . 一个H—H键断裂的同时有两个H—I键断裂 C . 温度和体积一定时,混合气体颜色不再变化 D . 反应速率v(H2)=v(I2)= v(HI)
E . 温度和体积一定时,容器内压强不再变化
F . 温度和体积一定时,混合气体的密度不再变化
v(HI)
E . 温度和体积一定时,容器内压强不再变化
F . 温度和体积一定时,混合气体的密度不再变化
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是( )
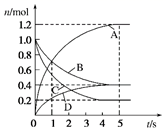
A . 该反应的化学方程式为6A+2D  3B+4C
B . 反应进行到1s时,v(A)=v(B)
C . 反应进行到5s时,B的平均反应速率为0.12mol/(L·s)
D . 反应从1s到4s时,C的反应速率逐渐减小
3B+4C
B . 反应进行到1s时,v(A)=v(B)
C . 反应进行到5s时,B的平均反应速率为0.12mol/(L·s)
D . 反应从1s到4s时,C的反应速率逐渐减小
 3B+4C
B . 反应进行到1s时,v(A)=v(B)
C . 反应进行到5s时,B的平均反应速率为0.12mol/(L·s)
D . 反应从1s到4s时,C的反应速率逐渐减小
3B+4C
B . 反应进行到1s时,v(A)=v(B)
C . 反应进行到5s时,B的平均反应速率为0.12mol/(L·s)
D . 反应从1s到4s时,C的反应速率逐渐减小
一定条件下,某密闭容器内发生反应 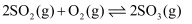 ,经一段时间后,SO3的浓度增加了0.4mol·L-1 , 在这段时间内用O2 表示的平均反应速率为0.04mol·L-1·s-1 , 则这段时间为( )
,经一段时间后,SO3的浓度增加了0.4mol·L-1 , 在这段时间内用O2 表示的平均反应速率为0.04mol·L-1·s-1 , 则这段时间为( )
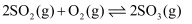 ,经一段时间后,SO3的浓度增加了0.4mol·L-1 , 在这段时间内用O2 表示的平均反应速率为0.04mol·L-1·s-1 , 则这段时间为( )
,经一段时间后,SO3的浓度增加了0.4mol·L-1 , 在这段时间内用O2 表示的平均反应速率为0.04mol·L-1·s-1 , 则这段时间为( )
A . 2.5s
B . 5 s
C . 7.5 s
D . 10 s
最近更新
- 木星是太阳系中体积最大的行星,人们对它充满无限遐想。为了解木星的形成、进化和结构等,在最新航天科技的支持下,美国预计于2
- 下列说法正确的是( )A.酸性氧化物在常温下均呈气态B.元素的非金属性强,其单质的活泼性也一定强C.非金属元素间相
- The first textbooks _____for teaching English as a foreign l
- 阅读下图,判断下面正确的说法是A.a河水力资源丰富 B.b河航运
- 将带开关的电灯、接冰箱的三孔插座,正确地接入图11中的电路中。
- “学生罢课半月,政府不惟不理,且对待日益严厉。乃商界罢市不及一日,而北京被捕之学生释;工商界罢工不及五日,而曹、章、陆去
- 提取下面一段话的主要信息,写出三个关键词语。 南航发文通知,从2010年5月1日(出票日期)起,调整中国境内始发的中国内
- BEIJING (AP) — Sandstorms whipping across China shrouded(遮蔽)
- 第①段中加点词“一跳一跳”写出霞光什么特点?
- ( ) A. B. C. D.
- Lucy _____ an “n” in“anniversary” in the exam, so she wasn’
- 我们之所以要毫不动摇地坚持和完善人民代表大会制度,发挥其优势和功能,是因为() A.人民代表大会制度直接体现了我国人民民
- 下列关于长江环境问题的叙述,正确的是 ( ) A.上中游湖泊面积缩小,森林和草地植被遭破坏,自然生态环
- 铁路是国家交通运输的命脉,承担着大量的运输任务,随着科技的不断进步,动车组相继投入运行,高速铁路也在不断修建。据此回答下
- Why do parents have such a difficult time tocommunicate open
- 有关神经系统的叙述,错误的是 () A.脊髓、脑干属于中枢神经系统 B.位于大脑皮层的呼吸中枢是维持生命的必要中枢 C.
- 开展道德模范评选表彰活动( ) ①是发展先进文化的重要内容 ②紧紧抓住了文化建设的灵魂③发挥了强有力的
- 句型转换;根据括号内的要求完成句子。 1.Brazil willwin the next World Cup.(就画线部
- 下列关于蛋白质的叙述中,正确的是 A.蛋白质溶液里加饱和(NH4)2SO4溶液可提纯蛋白质 B.天然蛋白质分子中既含,又
- (本小题满分14分)设为数列{an}的前项的积,且. (1)求数列{an}的通项公式; (2)若,求使成立的最小正整数.



