化学反应速率和化学计量数的关系 知识点题库
在2L密闭容器中发生反应N2+3H2⇋2NH3 , 经一段时间后NH3 的物质的量增加了2.4mol,这段时间内用氢气表示的反应速率为0.6mol/(L•s),则这段时间为( )
A . 6 s
B . 4 s
C . 3 s
D . 2 s
在四个不同的容器中,在不同条件下进行反应:N2+3H2⇌2NH3 根据在相同时间内测定的结果判断,生成氨气的速率最快的是( )
A . υ(H2)=0.2mol•L﹣1•s﹣1
B . υ(N2)=0.4mol•L﹣1•min﹣1
C . υ(NH3)=0.3mol•L﹣1•s﹣1
D . υ(H2)=0.6mol•L﹣1•min﹣1
反应4A(s)+3B(g)⇌2C(g)+D(g),经2min B的浓度减少0.6mol•L﹣1 . 对此反应速率的正确表示是( )
A . 用A表示的反应速率是0.8 mol•L﹣1•s﹣1
B . 分别用B,C,D表示反应的速率,其比值是3:2:1
C . 在2 min末时的反应速率,用反应物B来表示是0.3 mol•L﹣1•min﹣1
D . 在这2 min内用B和C表示的反应速率的值都是相同的
在2A(g)+B(g)=3C(g)+4D(g)反应中,表示该反应速率最快的数据是( )
A . v(A)=0.9 mol/(L•s)
B . v(B)=0.5 mol/(L•s)
C . v(C)=1.4 mol/(L•s)
D . v(D)=1.8 mol/(L•s)
将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)⇌xC(g)+2D(g),经5min后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,C的平均反应速率为0.1mol/(L•min).求:
-
(1) 此时A的浓度c(A)=mol/L,反应开始前容器中的A,B的物质的量:n(A)=n(B)=mol;
-
(2) B的平均反应速率v(B)=mol/(L•min);
-
(3) x的值为.
可逆反应A(g)+ 4B(g) 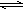 C(g)+ D(g),在四种不同情况下的反应速率如下,其中表示反应进行得最快的是( )
C(g)+ D(g),在四种不同情况下的反应速率如下,其中表示反应进行得最快的是( )
A . vA=0.15mol/(L·min)
B . vB=0.6 mol/(L·min)
C . vC=0.4 mol/(L·min)
D . vD=0.005 mol/(L·s)
游离态碳在自然界存在形式有多种,在工业上有着重要用途。请回答下列问题:
-
(1) 我国四大发明之一的黑火药由木炭与硫黄、硝酸钾按一定比例混合而成。黑火药爆炸时生成硫化钾、氮气和二氧化碳。其爆炸的化学方程式为。
-
(2) 高级碳粉可由烃类高温分解而制得,已知几个反应的热化学方程式:
C(s)+O2(g)=CO2(g) △H1= -393.5 kJ•mol-1
2H2(g)+O2(g)=2H2O(1) △H2= -571.6 kJ•mol-1
CH4(g)+2O2(g)-=CO2(g)+ 2H2O(1) △H3= -890.3 kJ•mol-1
则由天然气生产高级碳粉的热化学方程式为。
-
(3) 活性炭可以用来净化气体和液体。
①用活性炭还原氮氧化物,可防止空气污染。向1L闭容器加入一定量的活性炭和NO,某温度下发生反应C(s)+2NO(g)
 N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:
N2(g)+CO2(g),测得不同时间内各物质的物质的量如下表:物质的量/mol
时间/min
NO
N2
CO2
0
0.200
0
0
10
0.116
0.042
0.042
20
0.080
0.060
0.060
30
0.080
0.060
0.060
此温度下,该反应的平衡常数K=(保留两位小数)。10-20min内,NO的平均反应速率为;若30min后升高温度,达到新平衡时,容器中c(NO)∶c(N2) ∶c(CO2)=2∶1∶1,则该反应的ΔH0(填“>”、“<”或“=”)。
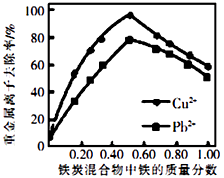
②活性炭和铁屑混合可用于处理水中污染物。在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示。当混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+ , 其原因是;当混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是。
在可逆反应:2A(g)+3B(g)  xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
 xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
A . 2min末时A和B的浓度之比为5:3
B . x=1
C . 2min末时B的浓度为1.5mol/L
D . 2min末时A的消耗浓度为0.5mol/L
下列四个数据是在不同条件下测出的2A+B=3C+4D反应速率,表示该反应速率最快的数据是( )
A . v(A)=0.5 mol·L-1·s-1
B . v(B)=0.3 mol·L-1·s-1
C . v(C)=0.8 mol·L-1·s-1
D . v(D)=1.0 mol·L-1·s-1
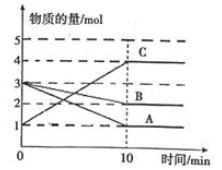
将一定量的A,B,C三种物质(都是气体)放入固定体积为1L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如下图所示。请回答下列问题:

-
(1) 反应的化学方程式用A、B、C可表示为。
-
(2) 用A表示在0~10min内的反应速率。
-
(3) 在该条件达到反应的限度时反应物B的转化率为。(计算结果用百分数表示,并保留1位小数)
-
(4) 开始时容器中的压强与平衡时的压强之比为。
反应4CO(g)+2NO2(g)  N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol·L-1 , N2的浓度为0,2 min后测得N2的浓度为0.6 mol·L-1 , 则此段时间内,下列反应速率表示正确的是( )
N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol·L-1 , N2的浓度为0,2 min后测得N2的浓度为0.6 mol·L-1 , 则此段时间内,下列反应速率表示正确的是( )
 N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol·L-1 , N2的浓度为0,2 min后测得N2的浓度为0.6 mol·L-1 , 则此段时间内,下列反应速率表示正确的是( )
N2(g)+4CO2(g)开始进行时,CO的浓度为4 mol·L-1 , N2的浓度为0,2 min后测得N2的浓度为0.6 mol·L-1 , 则此段时间内,下列反应速率表示正确的是( )
A . v(CO)=1.2 mol·L-1·s-1
B . v(NO2)=0.3 mol·L-1·min-1
C . v(N2)=0.6 mol·L-1·min-1
D . v(CO2)=1.2 mol·L-1·min-1
某温度下,在密闭容器中浓度都为1.0 mol·L-1的两种气体X2和Y2 , 反应生成气体Z。10 min后,测得X2、Z的浓度分别为0.4 mol·L-1、0.6 mol·L-1。该反应的化学方程式可能为( )
A . X2+2Y2  2XY2
B . 3X2+Y2
2XY2
B . 3X2+Y2  2X3Y
C . 2X2+Y2
2X3Y
C . 2X2+Y2  2X2Y
D . X2+3Y2
2X2Y
D . X2+3Y2  2XY3
2XY3
 2XY2
B . 3X2+Y2
2XY2
B . 3X2+Y2  2X3Y
C . 2X2+Y2
2X3Y
C . 2X2+Y2  2X2Y
D . X2+3Y2
2X2Y
D . X2+3Y2  2XY3
2XY3
在四个不同的容器中,在不同的条件下进行合成氨的反应,根据下列在相同时间内测定的结果判断,化学反应速率最快的是( )
A . v(H2)=0.2 mol·L-1·min-1
B . v(H2)=0.04 mol·L-1·s-1
C . v(N2)=0.01 mol·L-1·s-1
D . v(N2)=0.2 mol·L-1·min-1
某温度下,在2 L恒容密闭容器中投入一定量的A、B,发生反应:3A(g)+bB(g)  cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是( )
cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是( )
 cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是( )
cC(g)+2D(s),12 s时生成C的物质的量为0.8 mol(反应进程如图所示)。下列说法中正确的是( ) 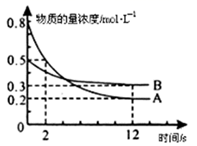
A . 图中两曲线相交时,A的消耗速率等于A的生成速率
B . 0-2 s,D的平均反应速率为0.1 mol·L-1·s-1
C . 化学计量系数之比b:c=1:4
D . 12 s时,A的转化率为75%
反应A(g)+3B(g)=2C(g)+2D(g)在四种不同情况下的反应速率分别为①v(A)=0.15mol∙L-1∙s-1 ②v(B)=0.6mol∙L-1∙s-1 ③v(C)=0.5mol∙L-1∙s-1 ④v(D)=0.45mol∙L-1∙s-1。下列表示该反应进行由快到慢的顺序正确的是( )
A . ②③④①
B . ④③②①
C . ③④②①
D . ②④③①
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此段时间内,该反应的速率 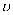 可表示为( )
可表示为( )
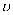 可表示为( )
可表示为( )
A . 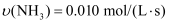 B .
B . 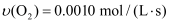 C .
C . 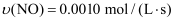 D .
D . 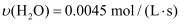
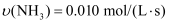 B .
B . 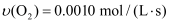 C .
C . 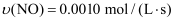 D .
D . 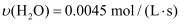
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列叙述中正确的是( )
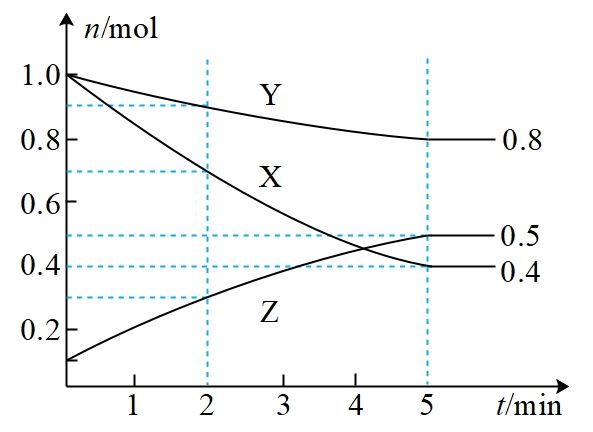
A . 5min后该反应停止进行
B . 5min时Y的体积分数约为47%
C . 该反应的化学方程式可表示为: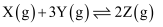 D . 前2min内,用Z表示该反应的化学反应速率为
D . 前2min内,用Z表示该反应的化学反应速率为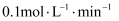
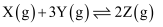 D . 前2min内,用Z表示该反应的化学反应速率为
D . 前2min内,用Z表示该反应的化学反应速率为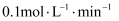
已知X(g)、Y(g)在适当条件下可反应生成化合物 , 反应过程中用X表示的正反应速率
, 反应过程中用X表示的正反应速率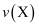 与时间的关系如图所示,下列有关说法错误的是( )。
与时间的关系如图所示,下列有关说法错误的是( )。
 , 反应过程中用X表示的正反应速率
, 反应过程中用X表示的正反应速率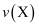 与时间的关系如图所示,下列有关说法错误的是( )。
与时间的关系如图所示,下列有关说法错误的是( )。
A . X与Y的反应是可逆反应,且在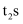 时达到平衡状态
B .
时达到平衡状态
B . 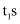 时,
时, 的生成速率小于其消耗速率
C .
的生成速率小于其消耗速率
C .  时间段内,
时间段内, 保持不变
D . 若某时间段内
保持不变
D . 若某时间段内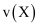 消耗
消耗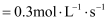 , 则该时间段内
, 则该时间段内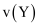 消耗
消耗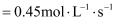
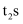 时达到平衡状态
B .
时达到平衡状态
B . 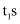 时,
时, 的生成速率小于其消耗速率
C .
的生成速率小于其消耗速率
C .  时间段内,
时间段内, 保持不变
D . 若某时间段内
保持不变
D . 若某时间段内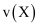 消耗
消耗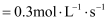 , 则该时间段内
, 则该时间段内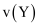 消耗
消耗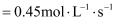
将气体X、Y置于容积为2L的密闭容器中,发生如下反应: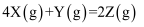 。反应进行到4s末,测得X为 0.5 mol,Y为 0.4 mol,Z为 0.2 mol。则用反应物X浓度的减少来表示该反应速率为( )
。反应进行到4s末,测得X为 0.5 mol,Y为 0.4 mol,Z为 0.2 mol。则用反应物X浓度的减少来表示该反应速率为( )
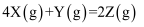 。反应进行到4s末,测得X为 0.5 mol,Y为 0.4 mol,Z为 0.2 mol。则用反应物X浓度的减少来表示该反应速率为( )
。反应进行到4s末,测得X为 0.5 mol,Y为 0.4 mol,Z为 0.2 mol。则用反应物X浓度的减少来表示该反应速率为( )
A . 0.025 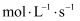 B . 0.0125
B . 0.0125 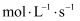 C . 0.05
C . 0.05 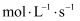 D . 0.1
D . 0.1 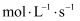
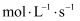 B . 0.0125
B . 0.0125 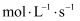 C . 0.05
C . 0.05 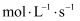 D . 0.1
D . 0.1 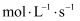
对于化学反应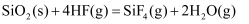 , 下列反应速率关系正确的是( )
, 下列反应速率关系正确的是( )
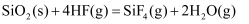 , 下列反应速率关系正确的是( )
, 下列反应速率关系正确的是( )
A . 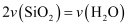 B .
B . 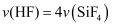 C .
C . 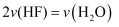 D .
D . 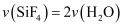
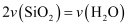 B .
B . 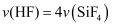 C .
C . 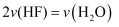 D .
D . 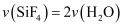
最近更新
- 将直尺和直角三角板按如图方式摆放,已知∠1=30°,则∠2的大小是() A. 30° B. 45° C. 60° D.
- ......
- 观察下图,可知当时实行的地方行政管理制度是A.分封制、郡县制
- A fish needs water and without water it will die ______. A.
- 下列动物及其气体交换部位搭配合理的是 ①蚯蚓—体壁 ②鲫鱼—鳃 ③家鸽—肺和气囊 ④青蛙—鳃和皮肤 ⑤家兔—肺 A
- 糖尿病在现代社会中的发病率越来越高。世界卫生组织将糖尿病列为三大疑难病之一并把每年的11月14日定为“世界糖尿病日”。下
- 一直流电压表,量程为1 V,内阻为1 000Ω,现将一阻值为5000~7000Ω之间的固定电阻R1与此电压表串联,以扩
- 如图所示的电路中,电源电动势E=10 V,内阻r=0.5 Ω,电动机的电阻R0=1.0 Ω,电阻R1=1.5 Ω.电动机
- 读我国某地的地形剖面图,回答问题。 图中山脉②是我国下列哪一组重要的地理分界线( ) A.第二
- 如图所示不同温度和压强下在一定容积的密闭容器中,对可逆反应4L(g) 2M(g)+N(g) △H>0,平衡状态时(
- Many people agree that there has never been a more splendid
- 请根据下图所示的四个装置,判断下列说法不正确的是()A.①可验证光合作用产生氧气 B.②可验证光合作用需要二氧化碳 C.
- 李欣经常偏食,结果他的上皮组织发生了角质化,皮肤粗糙,而且还出现皮下血管出血。这是由于他偏食,造成体内缺乏(
- Lucyis ________ at Chinese than Dick, but _________ at Math
- 孟德尔做了如下图所示的杂交实验,以下描述正确的是()A.所结豆荚细胞的基因型由植株A与植株B决定 B.所结豆荚细胞的基因
- 一定温度下,反应2 SO2 + O2 2SO3,达到平衡时,n(SO2):n(O2):n(SO3)=2:3:4。缩小体积
- 姓名是人的符号,中国人的姓总是位于名字之前,而不像西方那样,位于名字之后。中国人重视姓氏的现象体现了 A.男尊女卑
- 下列各句中,没有语病的一句是(3分)( ) A.扶贫工作组的同志经常到农村了解情况,他们的足迹踏遍了大江南北。 B. 因
- 设数列的前项和为,且满足,. (1)求数列的通项公式; (2)设,求数列的前项和.
- 已知定点P(-2,0)和直线l:(1+3λ)x+(1+2λ)y=2+5λ(λ∈R),则点P到直线l的距离的最大值为()



