晶格能的应用 知识点题库
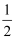 Cl2(g)―→NaCl(s) ΔH1
C . Na(s)―→Na(g) ΔH2
D . Na(g)-e-―→Na+(g) ΔH3
Cl2(g)―→NaCl(s) ΔH1
C . Na(s)―→Na(g) ΔH2
D . Na(g)-e-―→Na+(g) ΔH3
化学键 | Si﹣O | Si﹣Cl | H﹣H | H﹣Cl | Si﹣Si | Si﹣C |
键能/kJ•mol﹣1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
-
(1) 比较下列两组物质的熔点高低(填“>”或“<”)SiC Si;SiCl4 SiO2
-
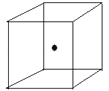
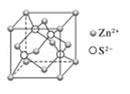
(2) 如图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子.
-
(3) 工业上用高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)
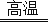 Si(s)+4HCl(g)该反应的反应热△H= kJ/mol.
Si(s)+4HCl(g)该反应的反应热△H= kJ/mol.
物质 | NaF | MgF2 | AlF3 | MgO | CaO | SrO | BaO |
| 923 | 2 957 | 5 492 | 3 791 | 3 401 | E | 1 918 |
由此表中数据不能得出的结论是( )
-
(1) 下列说法中正确的是_________。A . 半径:O2->Na+> Mg2+ B . 含氧酸的酸性:Cl>S>P C . 简单氢化物的稳定性:N>O>F D . 熔点:金刚石>碳化硅>硅单质
-
(2) C、N、O的电负性由大到小的顺序为。Na、Mg、Al的第一电离能由大到小的顺序为。
-
(3) 乙酸分子中σ键与π键的数目比为。HCOOCH3是乙酸的一种同分异构体,但沸点却比乙酸低得多,原因是。
-
(4) 已知AlCl3在178℃升华,熔融时生成二聚体Al2Cl6(结构式如下)。
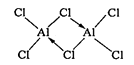
电解法制铝的原料是熔融的Al2O3而不是AlCl3 , 原因是;电解法制镁的原料是熔融的MgCl2而不用MgO,原因是。
 Cl2(g)=NaCl(s); △H2
C . Na+(l)+Cl-(l)=NaCl(s); △H3
D . Na(g)+
Cl2(g)=NaCl(s); △H2
C . Na+(l)+Cl-(l)=NaCl(s); △H3
D . Na(g)+  Cl2(g)=NaCl(s); △H4
Cl2(g)=NaCl(s); △H4
①具有规则几何外形的固体一定是晶体
②NaCl晶体中与每个Na+距离相等且最近的Na+共有12个
③非极性分子中一定含有非极性键
④晶格能由大到小: NaF> NaCl> NaBr>NaI
⑤含有共价键的晶体一定具有高的熔、沸点及硬度
⑥s-s σ键与s-p σ键的电子云形状相同
⑦含有π键的化合物与只含σ键的化合物的化学性质不同
⑧中心原子采取sp3杂化的分子,其立体构形不一定是正四面体
-
(1) 元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。A . 404.4 B . 553.5 C . 589.2 D . 670.8 E . 766.5
-
(2) 基态K原子中,核外电子占据的最高能层的符号是,占据该能层电子的电子云轮廓图形状为。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是。
-
(3) X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为,中心原子的杂化形式为。
-
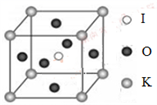
(4) KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为nm,与K紧邻的O个数为。
-
(5) 在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于位置,O处于位置。
 .
.
-
(1) Fe3+价层电子的轨道表达式(电子排布图)为。
-
(2) 硅能形成多种化合物(如SiH4、Si2H4等),SiH4的中心原子的杂化轨道类型为,其分子的立体构型为,键角为;Si2H4分子中含有的σ键和π键的数目之比为。
-
(3) Mg、Al的第一电离能:MgAl(填“>”或“<”)。
-
(4) Ca和Fe属于同一周期,且核外最外层电子构型相同,但金属Ca的熔点、沸点等都比金属Fe低,原因是。
-
(5) Ag晶体的堆积方式为面心立方最密堆积(如图所示),晶胞中Ag原子的配位数为;设Ag原子半径为rcm,阿伏加德罗常数的值用NA表示,则Ag晶体的密度为 g·cm-3(写出表达式)。

-
(1) 金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为 ;基态 Mn原子核外有种运动状态不同的电子,M层的电子云有种不同的伸展方向。
-
(2) 第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是
-
(3) NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒(写出一种),K3[Co(NO2)6]中存在的作用力有a.σ键 b.π键 c.配位键 d.离子键 e.范德华力
-
(4) 锰的一种配合物的化学式为 Mn(BH4)2(THF)3 , BH4-的空间构型为
-
(5) FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。

可知,O原子的第一电子亲和能为 kJ•mol-1 , FeO晶格能为kJ•mol-1。
-
(6) 铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为,已知该晶体的密度为ρg•cm-3 , NA是阿伏加德罗常数的值,则晶胞参数为pm
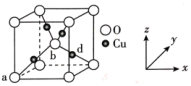
(列出计算式即可)
-
(1) 现有铜锌元素的4种微粒,①锌:[Ar]3d104s2;②锌:[Ar]3d104s1;③铜:[Ar]3d104s1;④铜:[Ar]3d10。失去一个电子需要的最低能量由大到小的顺序是(填字母)。
A ④②①③ B ④②③① C ①②④③ D ①④③②
-
(2) 砷化镉(Cd3As2)是一种验证三维量子霍尔效应的材料。
①砷与卤素可形成多种卤化物,AsBr3、AsCl3、AsF3的熔点由低到高的顺序为。砷酸的酸性弱于硒酸,从分子结构的角度解释原因。
②Cd2+与NH3形成配离子[Cd(NH3)4]2+中,配体的空间构型为,画出配离子的结构式(不考虑立体构型)。
-
(3) 铬(Cr)、钼(Mo)、钨(W)位于同一副族相邻周期,且原子序数依次增大。
①基态铬原子、钼原子的核外电子排布特点相同,则基态钼原子的价层电子排布图为。
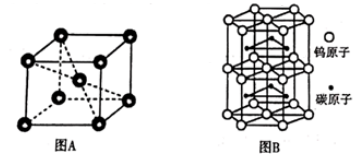
②铬的晶胞结构如图A所示,它的堆积模型为,在该晶胞中铬原子的配位数为。
③钨和碳能形成耐高温、耐磨材料碳化钨,其晶胞结构如图B所示,则碳化钨的化学式为,六棱柱的底边长为a cm,高为b cm,设阿伏加德罗常数的值为NA , 则碳化钨晶体的密度是g·cm-3(列出计算表达式)。
-
(1) 基态Co2+的价电子轨道表示式为。
-
(2) Co2+与CN-结合形成配合物[Co(CN)6]4- , 其中与Co2+结合的C原子的杂化方式是。
-
(3) NH3分子与Co2+结合成配合物[Co(NH3)6]2+ , 与游离的氨分子相比,其键角∠HNH(填“较大”,“较小”或“相同”),解释原因。
-
(4) Li2O熔点为1570℃,CoO的熔点为1935℃,解释后者熔点更高的主要原因是。
-
(5) 图(a)所示石墨晶体按ABAB方式堆积而成,图(b)为石墨的六方晶胞。
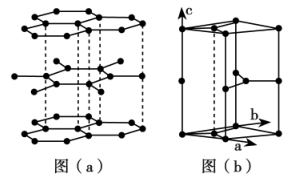
每个晶胞中的碳原子个数为,在下图中画出晶胞沿c轴的投影(用“●”标出碳原子位置即可)。
-
(1) 钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Fe的基态原子价电子排布式为。
②Ti的基态原子共有种不同能级的电子。
-
(2) 制备CrO2Cl2的反应为K2Cr2O7+3CCl4=2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由小到大的顺序是(用元素符号表示)。
②CCl4和COCl2分子中所有原子均满足8电子构型,CCl4和COCl2分子中σ键的个数比为,COCl2分子的中心原子的杂化方式为。
-
(3) NiO、FeO的晶体结构均与氯化钠的晶体结构相同,从微观角度解释NiO的熔点高于FeO的原因为。
-
(4) Ni和La的合金是目前使用广泛的储氢材料,具有大容量、高寿命、耐低温等特点,在日本和中国已实现了产业化。该合金的晶胞结构如图所示。
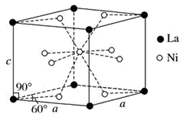
①该晶体的化学式为。
②已知该晶胞的摩尔质量为Mg·mol-1 , 密度为dg·cm-3.设NA为阿伏加德罗常数的值,则该晶胞的体积是cm3(用含M、d、NA的代数式表示)。
③该晶体的内部具有空隙,且每个晶胞的空隙中储存6个氢原子比较稳定。已知:a=500pm,c=400pm;标准状况下氢气的密度为9×10-5g·cm-3;储氢能力=
 。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为。(NA可近似取6×1023 ,
。若忽略吸氢前后晶胞的体积变化,则该储氢材料的储氢能力为。(NA可近似取6×1023 , 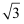 =1.7)
=1.7)
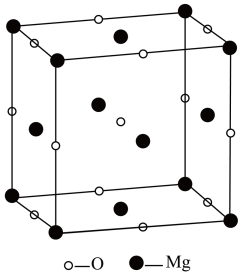
 距离相等且最近的
距离相等且最近的 共有8个
C . 一个晶胞中含有4个MgO
D . 晶体的熔点:CaO>MgO
共有8个
C . 一个晶胞中含有4个MgO
D . 晶体的熔点:CaO>MgO
- 氧化亚铁粉末和铝粉配成铝热剂,分成两等份。一份在高温下恰好完全反应后,在与盐酸反应;另一份直接放入足量的烧碱溶液中充分反
- You’re sitting on the trainhome and the person opposite you
- 马丁路德、加尔文和亨利八世宗教改革的共同影响包括 ①确定了“教随国定”的原则 ②建立了以国王为首脑的教会③否定了罗马教
- 下列有关平衡常数的说法正确的是( )A.已知 ,则对应的化学反应可以表示为:2CO2( g) + 6H2(g) C
- 与人体内环境及稳态有关的叙述,正确的是() A.肝细胞的直接内环境是组织液和淋巴 B.内环境中多余的H+主要从肺和皮肤排
- 我们应这样看待哲学的产生 ①与人类同时产生的 ②产生于人的主观情绪 ③产生于人的实践活动 ④产生于人们认识世
- A、B、C三种固体物质的溶解度曲线如图所示,下列说法正确的是()。A. t1 ℃时,三种物质的溶解度由大到小的顺序是A>
- 已知X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),则W、X不可能是选项
- 在过去300年里,经济现代化如潮水,一浪高过一浪。下表均摘自《2005中国现代化报告》,概述了经济现代化的六次浪潮。阅读
- 丙氨酸的R基为―CH3,谷氨酸的R基为―C3H5O2,它们缩合后形成的二肽分子中,C、H、O的原子比例为
- 读某岛屿示意图,完成29—30题29.有关该岛的说法正确的是
- 清代,徽剧与汉剧相互融合,兼收昆曲、秦腔以及其他民间曲调的唱腔、剧目和表演方式而形成的新剧种是 A、傩戏 B
- 近年来,我国人民在社会主义精神文明创建活动中,创造了丰富多彩的形式。下列属于精神文明创建活动的是: ①以“讲文明树
- 某同学用如图所示的装置及药品进行酸性强弱比较的实验,下列说法不正确的是()A. ①和②中发生的反应均为复分解反应 B.
- 研究表明,土壤中有一种细菌叫圆褐固氮菌,它能在代谢的过程中分泌某种物质,可以促进植物生根。为研究“圆褐固氮菌对某种植物枝
- 曹刿论战 《左传》 ①十年春,齐师伐我。公将战。曹刿请见。其乡人曰:“肉食者谋之,又何间焉?”刿曰:“肉食者鄙,未能远谋
- _____ with a big family ,the man worked hard day and night.
- 下图是在显微镜下观察到的某细胞内的某些结构,下列判断正确的是 A.这些结构是在光学显微镜下观察到的植物细胞结构 B.以上
- 已知函数f(x)=ax2+2(a+1)x+2,当-1≤a≤0时,恒有f(x)>0成立,试求x的取值范围.
- 下列电离方程式书写正确的是( ) A. NaHSO4 =Na++HSO4- B. H2SO32H+



