氢键的存在对物质性质的影响 知识点题库
-
(1) Mn3+基态核外电子排布式为。
-
(2) NO3-中氮原子轨道的杂化类型是。
-
(3) 与HNO2互为等电子体的一种阴离子的化学式为。
-
(4) 配合物[Mn(CH3OH)6]2+中提供孤对电子的原子是。
-
(5) CH3COOH能与H2O任意比混溶的原因,除它们都是极性分子外还有。
-
(6) 镁铝合金经过高温淬火获得一种储钠材料,其晶胞为立方结构(如图所示),图中原子位于顶点或面心。该晶体中每个铝原子周围距离最近的镁原子数目为。
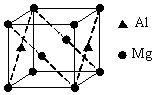
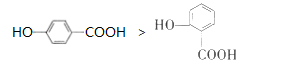 B . 晶格能的大小: Al2O3>MgCl2>NaCl
C . 共价键的键长: F-F>C-Cl>C-S>Si-O
D . 硬度由大到小:金刚石>氮化硅>晶体硅
B . 晶格能的大小: Al2O3>MgCl2>NaCl
C . 共价键的键长: F-F>C-Cl>C-S>Si-O
D . 硬度由大到小:金刚石>氮化硅>晶体硅
-
(1) N、P位于同一主族,NH3、PH3分子结构如下图所示:

①NH3和PH3中,N、P原子杂化方式相同,但H-N-H间的夹角比H-P-H间的大,其主要原因是。
②NH3比PH3易液化,其主要原因是。
-
(2) 基态氟原子核外电子的运动状态有种,有种不同能量的原子轨道。
-
(3) N与F可形成化合物N2F2 , 下列有关N2F2的说法正确的是(填字母)。
a.分子中氮原子的杂化轨道类型为sp2
b.其结构式为F-N≡N一F
c.1mol N2F2含有的σ键的数目为4NA
-
(1) H、B、N中,原子半径最大的是。根据对角线规则,B的一些化学性质与元素的相似。
-
(2) NH3BH3分子中,N—B化学键称为键,其电子对由提供。氨硼烷在催化剂作用下水解释放氢气:3NH3BH3+6H2O=3NH3+
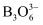 +9H2 ,
+9H2 , 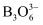 的结构如图所示:
的结构如图所示:
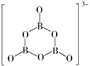
在该反应中,B原子的杂化轨道类型由变为。
-
(3) NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电负性大小顺序是。与NH3BH3原子总数相等的等电子体是(写分子式),其熔点比NH3BH3(填“高”或“低”),原因是在NH3BH3分子之间,存在,也称“双氢键”。
-
(4) 研究发现,氦硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
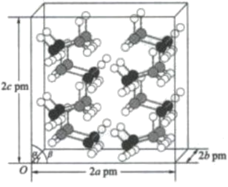
氨硼烷晶体的密度ρ=g·cm−3(列出计算式,设NA为阿伏加德罗常数的值)。
-
(1) Fe2+基态核外电子排布式为,PO43-的空间构型为(用文字描述)。
-
(2) NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是(填元素符号)。
-
(3) 1 mol
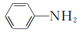 含有的σ键数目为,苯胺的沸点高于甲苯的主要原因是。
含有的σ键数目为,苯胺的沸点高于甲苯的主要原因是。
-
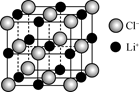
(4) 一个LiCl晶胞(如图)中,Li+数目为。
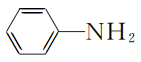 )制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
)制备的磷酸亚铁锂(LiFePO4)可用作电池的正极材料。
-
(1) Fe2+基态核外电子排布式为。
-
(2) N、P、O三种元素的电负性由大到小的顺序为。
-
(3) CO32-中心原子轨道的杂化类型为;与CO32-互为等电子体的一种分子为(填化学式)。
-
(4) 1 mol苯胺分子中含有σ键的数目为;苯胺与甲苯的相对分子质量相近,但苯胺的沸点高于甲苯,其原因是。
-
(1) 苯胺(
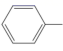 NH2)沸点高于甲苯(
NH2)沸点高于甲苯(  CH3)的主要原因是。
CH3)的主要原因是。
-
(2) KSCN是离子化合物,各原子均满足8电子稳定结构。写出KSCN的电子式。
-
(3) 已知NH2OH在水溶液中呈弱碱性的原理与NH3在水溶液中相似,请用电离方程式表示其原因。
①离子化合物中只存在离子键,共价化合物中只存在共价键②活泼非金属元素与活泼金属元素只能形成离子键③非金属元素间只能形成共价化合物④所有物质中均存在化学键⑤HF比HCl、HBr、HI更稳定,是因为HF分子间存在氢键
 ;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物
;D和氢原子可形成4核10电子分子,该分子可使湿润的红色石器试纸变蓝:A、C同周期,B和C同主族;A与B可形成两种离子化合物  、
、 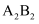 ,氢原子与B可形成两种共价化合物
,氢原子与B可形成两种共价化合物  、
、 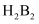 。试回答下列问题:
。试回答下列问题:
-
(1) C元素的元素符号为;写出A的电子排布式。
-
(2) 写出D元素形成的
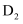 分子的结构式,其中
分子的结构式,其中  键与
键与  键的数目比为。
键的数目比为。
-
(3) B、D元素的第一电离能大小关系为:BD(填“<”或“>”)。
-
(4)
 对应的水化物的碱性比
对应的水化物的碱性比 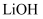 (填“强”或“弱”);写出
(填“强”或“弱”);写出 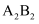 的电子式。
的电子式。
-
(5) 化合物
 、
、  它们结构与组成相似,热稳定性更强的是(填化学式),
它们结构与组成相似,热稳定性更强的是(填化学式),  的沸点比
的沸点比  高得多的原因是。
高得多的原因是。
-
(6) 下列选项能作为C元素和氧元素非金属性强弱比较的依据的是。
a.C的氧化物对应的水化物的酸性弱于盐酸
b.C元素的电负性小于氯的电负性
c.化学反应:
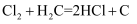
-
(7) B和C可以形成化合物
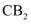 ,
, 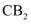 分子中空间结构为(填“V型”成“直线型”)。中心原子C采用杂化。
分子中空间结构为(填“V型”成“直线型”)。中心原子C采用杂化。
-
(8) 元素B和铜原子形成的化合物
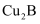 晶体结构可能是(填字母)。
晶体结构可能是(填字母)。 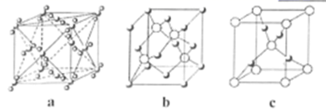
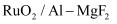 , 可应用于氟化工行业中的氯循环(如图)。
, 可应用于氟化工行业中的氯循环(如图)。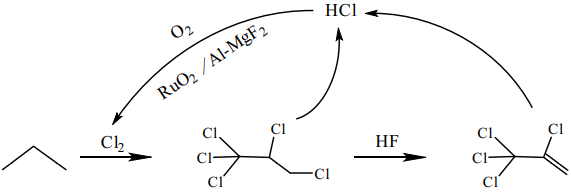
-
(1) Ru的价电子排布式为
 , 该元素位于第周期族。
, 该元素位于第周期族。
-
(2) 上述转化过程中涉及的有机反应类型有。
-
(3) 可通过液化分离出HCl中大多数的HF,从结构角度解释两者沸点差异的原因。
-
(4)
 、
、 、
、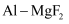 的晶体结构如图(
的晶体结构如图( 和
和 中实线部分为晶胞)
中实线部分为晶胞)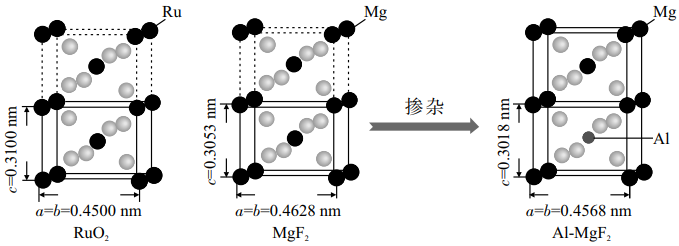
①
 晶胞中有个Ru,O在晶胞的位置为。
晶胞中有个Ru,O在晶胞的位置为。②已知
 与载体晶体结构(堆积方式、晶胞参数)越相似,催化效果越好。
与载体晶体结构(堆积方式、晶胞参数)越相似,催化效果越好。 载体中掺杂
载体中掺杂 的原因是。
的原因是。
 的熔、沸点比第VA族其他元素氢化物的高
B . 小分子的醇可以和水以任意比互溶
C . 冰的密度比液态水的密度小
D . 水分子高温下很稳定
的熔、沸点比第VA族其他元素氢化物的高
B . 小分子的醇可以和水以任意比互溶
C . 冰的密度比液态水的密度小
D . 水分子高温下很稳定
-
(1) 邻氨基吡啶的铜配合物在有机不对称合成中起催化诱导效应,其结构简式如下图所示。
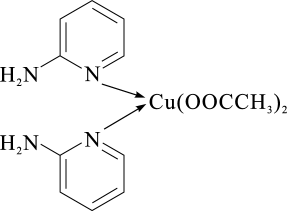
①在元素周期表中铜位于区(填“s”、“p”、“d”或“ds”)。C、N、O三种元素的电负性由大到小的顺序为。
②邻氨基吡啶的铜配合物中,Cu2+的配位数是,N原子的杂化类型有。
-
(2) 化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。
①1体积水可溶解约1体积CO2 , 1体积水可溶解约700体积NH3 , NH3极易溶于水的原因是,反应时,向饱和NaCl溶液中先通入。
②NaHCO3分解得Na2CO3 ,
 空间结构为。
空间结构为。 -
(3) 碳原子构成的单质具有多种同素异形体,也对应着有多种不同晶体类型。
①下图为石墨和石墨烯的结构示意图。石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体。下列关于石墨与石墨烯的说法正确的是。
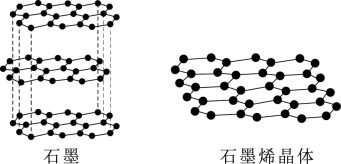
A.从石墨中剥离石墨烯需要破坏化学键
B.石墨中的碳原子采取sp3杂化
C.石墨属于混合型晶体,层与层之间存在分子间作用力
D.石墨烯中平均每个六元碳环含有2个碳原子
②利用皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管可以合成T-碳,T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)取代,如图所示(其中图(a)、(b)为T-碳的晶胞和俯视图,图(c)为金刚石晶胞)。
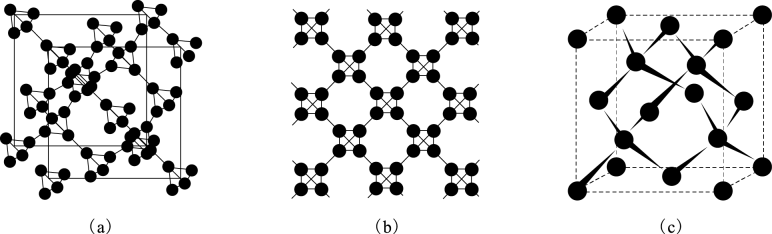
一个T-碳晶胞中含有个碳原子,T-碳的密度非常小为金刚石的一半,则T-碳晶胞的边长和金刚石晶胞的边长之比为。
- 马克思主义中国化的三大理论成果是 ①思想 ②理论 ③党的基本路线 ④“三个代表”的重要思想 A、①
- 编写一个程序,要求输入两个正数a和b的值,输出ab和ba的值.
- 第四部分 写作(共三节,满分35分) 第一节 单词拼写(把完整的单词写在答题卡上) 71. Every body kn
- 下图表示细胞内遗传信息传递的某个阶段,其中①②③分别表示相应的结构或物质,Asn、Ser、Cly为三种氨基酸,分别是天冬
- 光在透明物质或中传播,声音的传播需要 。
- 在泡菜腌制过程中亚硝酸盐含量变化曲线如图所示,正确的是() A. B. C. D.
- 下列关于人类遗传病的说法,正确的是 A.单基因遗传病是受1个基因控制的遗传病 B.镰刀型细胞贫血症的人与正常人相比,有关
- 日常生活中发生的下列变化都属于化学变化的一组是() A.玻璃杯被摔碎,米饭变馊 B.酒精挥发,湿衣服晾干 C.蜡烛燃
- 已知P为⊙O内一点,OP=1,如果⊙O的半径是2,那么过P点的最短弦长是 ( ) A.1
- 一切陆生生物的“立足点”是A、大气圈 B、水圈 C、岩石圈 D、生物圈
- 木工师傅做完房门后,为防止变形钉上两条斜拉的木条这样做的根据是
- 物体在光滑斜面顶端由静止开始匀加速下滑,最初4s内经过的位移为S1,最后4s内经过的位移为S2,且S2-S1=8m,S1
- 下面四幅地形剖面图中,能正确表示湖南省沿28°N线地形起伏的是
- 地球同步卫星每天绕地球运转一周,月球这颗地球的天然卫星27天 绕地 球运转一周,则月球绕地球运转的轨道半径是同步卫星轨
- 维新运动期间,宣扬维新思想的学会、学堂在全国各地纷纷兴起。其中,创办于湖南长沙的是( ) A.保国会
- 某同学在家中找到一种白色粉末,到学校实验室进行实验,实验过程与现象如下,对此粉末成分判断正确的是( ) A、该粉末
- 图4中甲图为非洲和欧洲大陆从赤道向两极,以及山地从山麓向山顶自然带的地域分异示意图,乙图为亚欧大陆从沿海向内陆以及山地由
- 3.依次填入下面一段文字横线处的语句,衔接最恰当的一组是( ) 一个民族如果没有自己的科技,可能会亡国;但是,一
- 下列词语中加点字的读音完全正确的一组是( ) A.贮备(chù) 一幢(zhuàn
- CH2===CHCH2OH可能发生的反应类型有:①加成反应 ②氧化反应 ③取代反应 ④中和反应() A.只有①③



