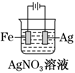
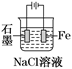
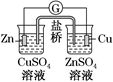
铜的电解精炼 知识点题库
下列有关说法中正确的是( )
A . 自来水厂可用明矾对水进行消毒杀菌
B . 氯碱工业中,NaOH是在阴极室中产生的
C . 电解法精炼铜时,粗铜接电源的负极
D . 实验室盛放Na2CO3、Na2SiO3等溶液的试剂瓶应用玻璃塞
下列关于工业生产说法不正确的是( )
A . 电解精炼铜时,用粗铜做阴极,纯铜做阳极
B . 在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率
C . 在炼铁工业,需要的原料有铁矿石、焦炭、空气、石灰石等
D . 在侯氏制碱工业中,向饱和氯化钠溶液中先通氨气,后通二氧化碳
下列说法中正确的是( )
A . 电解精炼铜时,纯铜作为阳极,粗铜作为阴极
B . 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
C . 氯碱工业中阳离子交换膜的主要作用是:防止阳极产生的氯气和阴极产生的氢气及氢氧化钠反应
D . 工业合成氨通常采用500℃的高温主要是为了提高氮气的转化率
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是( )
A . 粗铜精炼时,与电源正极相连的是纯铜,阳极反应式为Cu﹣2e﹣═Cu2+
B . 氢氧燃料电池的负极反应式:O2+2H2O+4e﹣═4OH﹣
C . 用惰性电极电解饱和食盐水时,阳极的电极反应式为2Cl﹣﹣2e﹣═Cl2↑
D . 钢铁发生电化学腐蚀的正极反应式:Fe﹣2e﹣═Fe2+
下列描述中,不符合生产实际的是( )
A . 电解法精炼粗铜,用纯铜作阴极
B . 在镀件上电镀锌,用锌作阳极
C . 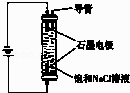 用如图装置生产家用消毒液(NaClO)
D .
用如图装置生产家用消毒液(NaClO)
D . 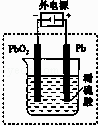 用如图装置为铅蓄电池充电
用如图装置为铅蓄电池充电
 用如图装置生产家用消毒液(NaClO)
D .
用如图装置生产家用消毒液(NaClO)
D .  用如图装置为铅蓄电池充电
用如图装置为铅蓄电池充电
下列说法正确的是( )
A . 工业上电解氯化镁溶液可以制备金属镁
B . 生物炼铜就是利用植物对铜离子的吸收达到富集铜的目的
C . 工业上用廉价的焦炭还原铁矿石得到铁
D . 工业上利用氢气在氯气中燃烧生成氯化氢,再将氯化氢溶于水制得盐酸
下列有关电化学装置完全正确的是( )
| A | B | C | D |
| | | | |
| 铜的精炼 | 铁上镀银 | 防止Fe被腐蚀 | 构成铜锌原电池 |
A . A
B . B
C . C
D . D
下列化学用语书写正确的是( )
A . 次氯酸的电离方程式:HClO=H++ClO-
B . 硫化钠水解的离子方程式:S2-+2H2O  H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)
H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)  Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
 H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)
H2S+2OH-
C . 电解精炼铜的阴极反应式:Cu-2e-=Cu2+
D . 碳酸钙的溶解平衡:CaCO3(s)  Ca2+(aq)+CO32-(aq)
Ca2+(aq)+CO32-(aq)
下列说法中正确的是( )
A . 在船体上镶嵌锌块,可以减缓船体被海水腐蚀的速率
B . 粗铜精炼时,电镀液中的c(Cu2+)保持不变
C . 纯银在空气中久置变黑发生的是电化学腐蚀
D . 阴极电保护法是将被保护的金属与外加电源的正极相连
关于下列装置的说法正确的是( )
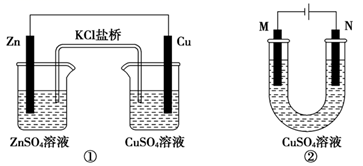
A . 装置①将电能转变为化学能
B . 装置①中盐桥内的 K+移向 CuSO4 溶液
C . 若装置②用于铁棒镀铜,则 N 极为铁棒
D . 若装置②用于电解精炼铜,溶液中的 Cu2+浓度保持不变
下列有关工业生产的叙述正确的是( )
A . 合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B . 从海水中可以得到NaCl,工业冶炼金属钠可以通过电解NaCl饱和溶液获得
C . 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
D . 电解饱和食盐水制烧碱,采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室
如图所示,某学生设计一个甲醚燃料电池并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。
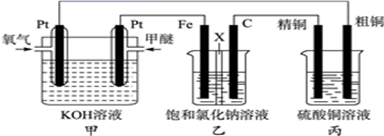
根据要求回答相关问题:(甲醚的化学式:CH3OCH3)
-
(1) 通入氧气的电极为(填“正极”或“负极”),写出负极的电极反应式。
-
(2) 铁电极为(填“阳极”或“阴极”),石墨电极(C)的电极反应式为。
-
(3) 如果粗铜中含有锌、银等杂质,反应一段时间,硫酸铜溶液浓度将 (填“增大”“减小”或“不变”)。
-
(4) 若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为;丙装置中阴极析出铜的质量为。
关于下列各装置图的叙述中,错误的是( )
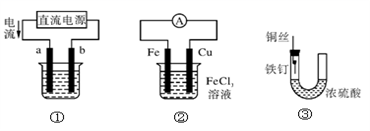
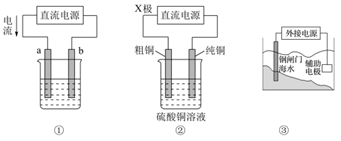
A . 用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B . 用装置①进行电镀,镀件接在b极上
C . 装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
D . 装置③中的铁钉几乎没被腐蚀
下列关于铜电极的叙述中错误的是( )
A . 锌铜原电池中铜是正极
B . 在镀件上镀铜时可用金属铜作阳极
C . 用电解法精炼粗铜时粗铜作阳极
D . 用电解法精炼粗铜时纯铜作阳极
铜的氧化物及其盐有重要的用途。制泡铜发生如下反应:2Cu2S+3O2=2Cu2O+2SO2 , 2Cu2O+Cu2S=6Cu+SO2↑,将泡铜熔炼后再电解精炼制精铜。关于铜及铜的制备说法正确的是( )
A . 铜元素在元素周期表的d区,基态原子核外电子排布式为[Ar]3d104s1
B . 制泡铜过程中,制取6molCu共转移18mol电子
C . 电解精炼粗铜时,阴极减小的质量等于阳极增加的质量
D . 精炼后的电解液中存在:Cu2+、Zn2+、  、Fe2+、Ag+
、Fe2+、Ag+
 、Fe2+、Ag+
、Fe2+、Ag+
设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A . 14 g聚丙烯中含C-H键总数目为NA
B . 氢氧燃料电池正极消耗22. 4 L(标准状况)气体时,电路中通过的电子数目为2NA
C . 2.3gNa与氧气完全反应,反应中转移的电子数介于0.1NA到0. 2NA之间
D . 电解精炼铜时,若阳极质量减少64 g,则阴极得到电子的数目为2NA
关于下列各装置图的叙述错误的( )
A . 图①装置可实现铁上镀铜,则a极为铜,b极为铁
B . 图②装置可实现粗铜的精炼,则X极为正极
C . 图①装置可用于氯碱工业,则电极总反应式为:2Cl-+2H2O  H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
 H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
H2↑+Cl2↑+2OH-
D . 图③装置中钢闸门应与外接电源的负极相连以实现牺牲阳极的阴极保护法
NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 1L浓度为0.100mol/L的Na2CO3溶液中,阴离子总数为0.100NA
B . 常温下,pH=9的CH3COONa溶液中,水电离出的OH-数为10-5 NA
C . 电解精炼铜时,电路中通过的电子数为NA , 阳极有32g Cu转化为Cu2+
D . 4MnO  +5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO  +5HCHO]完全反应转移的电子数为20 NA
+5HCHO]完全反应转移的电子数为20 NA
 +5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO
+5HCHO+12H+=4Mn2++5CO2↑+11H2O,1mol [4MnO  +5HCHO]完全反应转移的电子数为20 NA
+5HCHO]完全反应转移的电子数为20 NA
下列关于电化学的说法正确的是( )
A . 钢板上的铁铆钉处在潮湿的空气中直接发生反应: 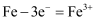 ,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
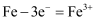 ,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
,发生吸氧腐蚀
B . 电解精炼铜时,阳极为粗铜,阴极为精铜,电解过程中电解质溶液不需要更换
C . 在铁制器皿上镀锌,铁制器皿作阴极,锌片作阳极
D . 二次电池充电时,电池上标有“+”的电极应与外接电源的负极相连
辉铜矿(主要成分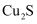 )可以用于制铜,化学反应方程式为
)可以用于制铜,化学反应方程式为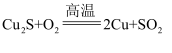 , 制得的粗铜(含
, 制得的粗铜(含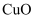 等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
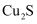 )可以用于制铜,化学反应方程式为
)可以用于制铜,化学反应方程式为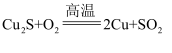 , 制得的粗铜(含
, 制得的粗铜(含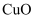 等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
等杂质)可通过电解法进行精炼,下列相关说法正确的是( )
A . 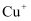 转化为基态
转化为基态 , 得到的电子填充在
, 得到的电子填充在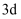 轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的
轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的 晶胞中,黑球表示的是
晶胞中,黑球表示的是
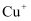 转化为基态
转化为基态 , 得到的电子填充在
, 得到的电子填充在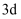 轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的
轨道上
B . S元素的电负性大于O元素的电负性
C . 电解精炼铜时,粗铜应与电源的负极相连
D . 如图所示的 晶胞中,黑球表示的是
晶胞中,黑球表示的是
最近更新
- 萘环上的碳原子编号如Ⅰ式,根据系统命名法,Ⅱ式可称为2硝基萘,则化合物Ⅲ的名称应是A.2,6二甲基萘 B.2
- 中考链接阅读下列文字,回答文后问题。 雨 中 李瑛 一朵云, 拧下一阵雨, 匆匆地掠过车篷; 汽车兵, 从窗
- 在充满 的日子里 先将题目补写完整,然后作文,文体不限,字数不少于800字。
- 已知实数、,则“”是“”的 ( ) A.充分不必要条件 B.必要不充分条件
- 全部在南半球的大洲是( ) A、亚洲 B、南极洲 C、非洲 D、
- 1929-1933年美、德、英、法、日等国的工业生产分别下降情况:美国 德国 英国 法国 日本 46.2% 40.6%
- 6.宋代开国宰相赵普总结其辅佐宋太祖赵匡胤治理天下的经验时说:“半部论语治天下。”孔子思想成为中国古代统治阶级治国的正统
- 我们的故乡重庆是一个山清水秀、人杰地灵,文化底蕴浓重的地方,在这里,大师功成名就,学问发扬光大。请问宋代哪一门学问的研究
- 根据提示将下列句子译成英语。(共5小题 每小题2分 计10分) 101. 他们正在谈论举行一个晚会来为穷地区的孩子募集钱
- 山居秋暝 王 维 空山新雨后,天气晚来秋。 明月松间照,清泉石上流。 竹喧归浣女,莲动下渔舟。 随意春芳歇,王孙自可留。
- 日常生活中我们常观察到以下现象:①菜刀表面常产生棕黄色的斑点 ②新鲜萝卜放入泡菜坛中,几天后萝卜变酸了 ③水果腐烂后
- 将3.48 g Fe3O4 完全溶解在 100 mL 1.00 mol·L-1的 H2SO4(aq)中,然后加入 K2C
- — that he managed to get the information? —Oh,a fri
- 为得到函数的图象,只需将函数的图像( ) A.向左平移个单位长度 B.向右平移个单位长度 C.向左平
- 下列语段中加点的词语,使用恰当的一项是 ( ) 来自广西的“飞人”劳义在广州亚运会
- 13. —Do you have ________ difficulty working out the problem
- —_______ to the sun, the flowers will become dry soon. —What
- 2012年,全国普通高校毕业生规模达到680万人,高校毕业生就业形势依然严峻,众 多大学生都要“抢”工作。一个“抢”字主
- Along the river banks of the Amazon and the Orinoco there li
- 已知磷酸分子中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可跟D2O进行氢交换