甲烷的取代反应 知识点题库
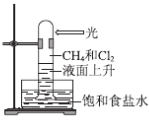
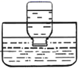
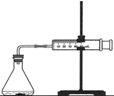
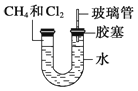
如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解度可以忽略.将封闭有甲烷和氯气混合气体的装置放置在有光亮的地方,让混合气体缓慢地反应一段时间.
-
(1) 假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:
-
(2) 若题目中甲烷与氯气的体积之比为1:1,则得到的产物为 (填字母编号).
A.CH3Cl HCl B.CCl4 HCl
C.CH3Cl CH2Cl2 D.CH3Cl CH2Cl2 CHCl3 CCl4 HCl
-
(3) 经过几个小时的反应后,U形管右端的水柱变化是 (填字母编号).
A.升高 B.降低 C.不变 D.无法确定
-
(4) 若水中含有Na2SiO3 , 则在U形管左端会观察到
-
(5) 右端玻璃管的作用是
已知碳化铝(Al4C3)与水反应生成氢氧化铝和甲烷.为了探究甲烷性质,某同学设计如下两组实验方案;甲方案探究甲烷与氧化剂反应(如图1所示);乙方案探究甲烷与氯气反应的条件(如图2所示)

甲实验现象:溴水无颜色变化,澄清石灰水变浑浊,无水硫酸铜变蓝色.乙实验操作过程:通过排饱和食盐水的方法收集两瓶甲烷与氯气(体积比为1:4)混合气体(Ⅰ、Ⅱ),Ⅱ瓶用预先准备好的黑色纸套套上,I瓶放在光亮处(不要放在日光直射的地方,以免引起爆炸).按图2安装好装置,并加紧弹簧夹a和b.
-
(1) 写出碳化铝与硫酸反应的化学方程式
-
(2) 实验甲中浓硫酸的作用是 ,集气瓶中收集到的气体能否直接排入空气中? (填“能”或“否”).
-
(3) 下列对实验甲有关现象与结论的叙述都正确的是
A.酸性高锰酸钾溶液不褪色,结论是通常条件下,甲烷不能与强氧化剂反应
B.硬质试管里黑色粉末无颜色变化,结论是甲烷不与氧化铜反应
C.硬质试管里黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳
D.甲烷不能与溴水反应,推知甲烷不能与卤素单质反应
-
(4) 写出硬质试管里可能发生的化学方程式
-
(5) 过一段时间,打开图2的a、b弹簧夹,Ⅰ、Ⅱ中观察到现象是
-
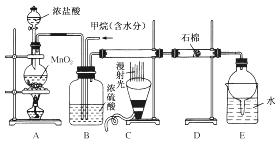
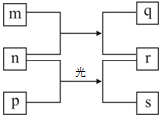
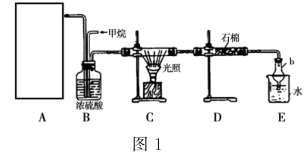
(1) B装置有三种功能:①控制气流速度;②均匀混合气体;③。
-
(2) 设V(Cl2)/V(CH4)=x , 若理论上欲获得最多的氯化氢,则x的值应为。
-
(3) D装置的石棉中均匀混有KI粉末,其作用是。
-
(4) E装置的作用是(填编号)。
A.收集气体 B.吸收氯气
C.防止倒吸 D.吸收氯化氢
-
(5) E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为。该装置存在的缺陷是没有进行尾气处理,其尾气的主要成分为(填编号)。
A.CH4 B.CH3Cl
C.CH2Cl2 D.CHCl3
E.CCl4
-
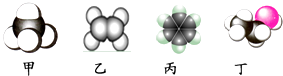
(1) Y形成的简单阴离子结构示意图为。
-
(2) n的电子式为。
-
(3) 请列举q的一种用途。
-
(4) W、X、Y原子半径的由大到小的顺序为(用元素符号表示)。
-
(5) 写出n、p第一步反应的化学方程式。
| A | B | C | D |
| | | | |
| 甲烷发生了取代反应 | 乙烯发生了加成反应 | 乙醛发生还原反应 | 有不饱和烃生成 |
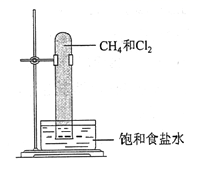
光照下反应一段时间后,下列装置示意图中能符合题意反映实验现象的是( )
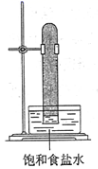 B .
B . 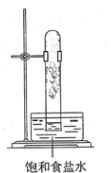 C .
C . 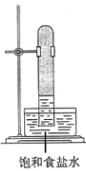 D .
D . 
| | | | |
| A.将绿豆大小的金属钠投入蒸馏水中,钠块熔成小球,浮于水面,迅速游 动,溶液变红 | B.将甲烷与氯气1∶1混合,在光照条件下反应,黄绿色褪去,水面上升,充满集气瓶 | C.将5g碳酸钙投入20mL1mol·L-1盐酸,针筒活塞向右移动的速率先逐渐增大,然后减小 | D.将铜片与浓硫酸混合加热,品红溶液变红,试管内出现蓝色固体和 少量黑色物质 |
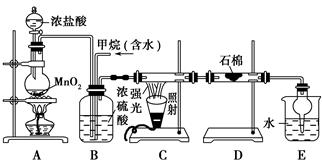
根据设计要求回答:
-
(1) B装置有三种功能:①控制气流速度;②均匀混合气体;③。
-
(2) D装置的石棉中均匀混有KI粉末,其作用是。
-
(3) E装置的作用是________________________(填编号)。A . 收集气体 B . 吸收氯气 C . 防止倒吸 D . 吸收氯化氢
-
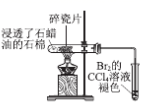
(4) 在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式。
-
(5) E装置除生成盐酸外,还含有有机物,从E中分离出有机物的最佳方法为。
-
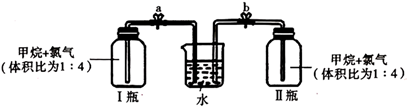
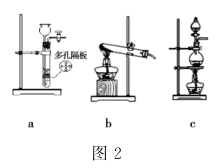
(1) (甲方案)探究甲烷与氯气反应的条件,如图所示。Ⅰ瓶放在光亮处,Ⅱ瓶用预先准备好的黑色纸套套上,并夹紧弹簧夹a和b。
一段时间后,打开弹簧夹a、b,观察到有水倒吸入Ⅰ瓶中,但水并不能充满Ⅰ瓶。除了上述现象外,该实验中还可能观察到的现象有______________(填字母)。
A . Ⅰ瓶中气体颜色变浅 B . Ⅰ瓶中出现白雾 C . Ⅰ瓶内壁出现油状物质 D . Ⅱ瓶中与Ⅰ瓶现象相同 -
(2) (乙方案)探究甲烷与氧化剂反应,如图所示。已知碳化铝(
 )与水反应生成氢氧化铝和甲烷。
)与水反应生成氢氧化铝和甲烷。 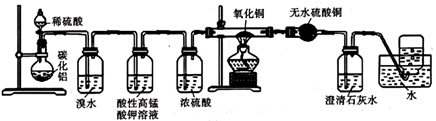
实验现象:溴水不褪色,无水硫酸铜变蓝色,澄清石灰水变浑浊。
回答下列问题:
碳化铝与稀硫酸反应的化学方程式为。
-
(3) 加入药品前,应先进行的一步操作是。
-
(4) 下列对实验中的有关现象与结论叙述都正确的是_____________(填字母)。A . 甲烷不能与溴水反应,推知甲烷不能与卤素单质反应 B . 酸性高锰酸钾溶液不褪色,结论是通常条件下甲烷不能与强氧化剂反应 C . 硬质玻璃管中黑色粉末无颜色变化,结论是甲烷不与氧化铜反应 D . 硬质玻璃管中黑色粉末变红色,推断氧化铜与甲烷反应只生成水和二氧化碳
-
(5) 经测定,甲烷与氧化铜反应时每消耗1mol甲烷转移电子7mol,写出实验时硬质玻璃管中发生反应的化学方程式。
-
(6) 浓硫酸的作用是,集气瓶中排水法收集到的气体(填“能”或“不能”)直接排入空气中。
-
(1) A是氯气发生装置,该实验中A部分的装置是图2中的(填字母)。
-
(2) B装置有三种功能:①控制气流速度;②;③。
-
(3) D装置中的石棉上吸附着潮湿的KI,其作用是。
-
(4) E装置中除了有盐酸生成外,还含有有机物,从E中分离出盐酸的最佳方法是。
-
(5) 该装置的缺陷是没有进行尾气处理,其尾气的主要成分是_______(填序号)。A . CH4 B . CH3Cl C . CH2Cl2 D . CHCl3 E . CCl4
-
(6) 将1molCH4与Cl2发生取代反应,充分反应后生成四种有机产物,其中CH3Cl、CH2Cl2 , CHCl3的物质的量依次为amol、bmol、cmol,则参加反应的Cl2的物质的量为mol。
|
物质 |
溶解性 |
熔点(℃) |
沸点(℃) |
|
甲苯 |
极微溶于水,能与乙醇、乙醚等混溶 |
-94.9 |
110 |
|
氯化苄 |
微溶于水,易溶于苯、甲苯等有机溶剂 |
-39 |
178.8 |
|
二氯化苄 |
不溶于水,溶于乙醇、乙醚 |
-16 |
205 |
|
三氯化苄 |
不溶于水,溶于乙醇、乙醚和苯 |
-7 |
220 |
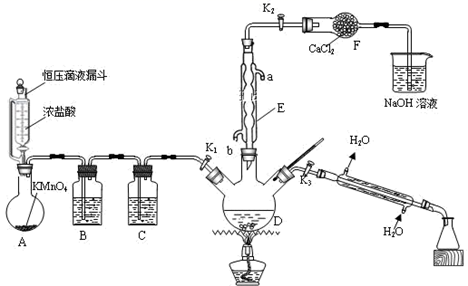
回答下列问题:
-
(1) 装置A中,发生的离子反应方程式为:。装置F的作用是。
-
(2) 已知甲苯和氯化苄均是无色透明液体,请用一个简单的方法,鉴别甲苯和氯化苄:。
-
(3) 装置D中,发生的反应为:,该反应类型是。
-
(4) 实验结束时,为了得到纯净的氯化苄,简述其操作:。
-
(5) 检测氯化苄样品的纯度:
①称取13.00 g样品于烧杯中,加入50.00 mL 4 mol•L-1 NaOH水溶液,水浴加热1小时,冷却后加入35.00mL40% HNO3 , 再将全部溶液转移到容量瓶中配成100 mL溶液。取20.00 mL溶液于试管中,加入足量的AgNO3溶液,充分振荡,过滤、洗涤、干燥,称量固体质量为2.87g,则该样品的纯度为%(结果保留小数点后1位)。
②实际测量中,由于样品中混入二氯化苄、三氯化苄等杂质,会使结果。(偏高、偏低、无影响)
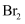 , 分液时先从分液漏斗下口放出有机层,再从上口倒出水层
B . 因为乙烯具有还原性,所以乙烯通入溴水中能使溴水褪色
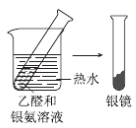
C . 做完银镜反应后的试管可用热的稀硝酸清洗,回收后的硝酸银溶液可再利用
D . 充满
, 分液时先从分液漏斗下口放出有机层,再从上口倒出水层
B . 因为乙烯具有还原性,所以乙烯通入溴水中能使溴水褪色
C . 做完银镜反应后的试管可用热的稀硝酸清洗,回收后的硝酸银溶液可再利用
D . 充满 和
和 的试管倒置在饱和食盐水溶液之上,光照充分反应后,液体会充满试管
的试管倒置在饱和食盐水溶液之上,光照充分反应后,液体会充满试管
选项 | 实验 | 结论 |
A | 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 | 生成的一氯甲烷具有酸性 |
B | 向淀粉溶液中加少量稀硫酸,加热4~5min。冷却后向其中加入新制Cu(OH)2悬浊液,加热至沸腾,无砖红色沉淀 | 淀粉没有发生水解 |
C | 乙烯能使酸性高锰酸钾溶液褪色 | 可以用酸性高锰酸钾溶液除去乙烷中的乙烯,并得到于燥纯净的乙烷 |
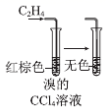
D | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 发生加成反应,产物无色、可溶于四氯化碳 |
- 太祖时,郭进①为西山巡检,有告其阴通河东刘继元②,将有异志者,太祖大怒,以其诬害忠臣,命缚其人予进,使自处置。进得而不杀
- 光滑水平面上有一边长为的正方形区域处在场强为的匀强电场中,电场方向与正方形一边平行。一质量为、带电量为的小球由某一边的中
- 下列物质中,在核糖体内合成的是( ) ①性激素 ②K+的载体 ③淀粉 ④唾液淀粉酶 ⑤纤维素 A、①②
- 已知向量=(m,2),向量=(2,﹣3),若|+|=|﹣|,则实数m的值是() A.﹣2 B.3 C. D
- 已知A、B两点对应的复数分别为3-2i和4+3i,试判断A、B两点是否在圆|z-(1-i)|=5上.
- (1)300 ℃时,将2 mol A和2mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2
- Debbie will have fun looking for the Easter eggs.A.enjoyB.di
- Ihave two friends who love backpacking. They spent a lot of
- 1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质, 但还有一些问题尚未解决,下列事实中它不能
- 《汉书》记载:“秦遂并兼四海,以为周制微弱,终为周制所丧……”为此秦朝开创了:A. 三公九卿制 B.皇帝制度
- 圆台的一个底面周长是另一个底面周长的3倍,轴截面的面积等于392,母线与轴的夹角为45°,求这个圆台的高、母线长和底面半
- 改革开放的30年是中国特色社会主义理论体系形成与发展的30年。中国特色社会主义理论体系是马克思主义中国化的最新成果,是党
- What’s with you? A.wrong B.thewrong
- He isquiet and shy. He likes to hide(隐藏) his eyes behind his
- 阅读下面文言文 顾亭林①居家恒服布衣, 俯身者无寸缕之丝,当著《音学五书》时,《诗本音》卷二稿再为鼠啮,再为誊录,略无愠
- 下列各原子或离子的电子排布式错误的是 ( ) A
- 如图,点E在正方形ABCD内,满足∠AEB=90°,AE=6,BE=8,则阴影部分的面积是() A.48 B.60
- 用下列方法测定空气中污染物的含量:将一定体积的空气通入吸收剂,并测定其电导的变化(导体的电阻愈大,它的电导愈小)。如测定
- 在家鼠的遗传实验中,一黑色家鼠与白色家鼠杂交,F1均为黑色。F1个体间随机交配得F2,F2中黑色∶浅灰色∶白色=12∶3
- 若点B(,0)在以点A(1,0)为圆心,以2为半径的圆内, 则的取值范围为A.B.C.D.或