反应热和焓变 知识点题库
 O2(g)═H2O(g);△H=a kJ/mol
O2(g)═H2O(g);△H=a kJ/mol 2)2H2(g)+O2(g)═2H2O(g);△H=b kJ/mol
3)H2(g)+  O2(g)═H2O(l);△H=c kJ/mol
O2(g)═H2O(l);△H=c kJ/mol
4)2H2 (g)+O2(g)═2H2O(l);△H=d kJ/mol
下列关系式中正确的是( )
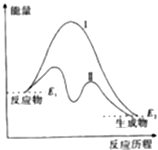
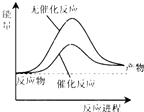
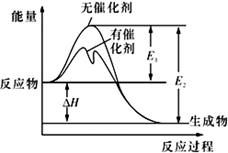
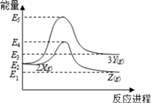
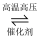 N2+3H2的能量变化
C . 该反应不需要加热就能发生
D . 该反应的△H=E2﹣E1
N2+3H2的能量变化
C . 该反应不需要加热就能发生
D . 该反应的△H=E2﹣E1
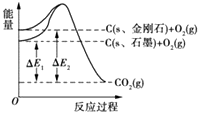
 2NH3(g) △H=-92kJ/mol,相关数据如下:
2NH3(g) △H=-92kJ/mol,相关数据如下:H2(g) | N2(g) | NH3(g) | |
1mol分子中的化学键形成时要释放出的能量/kJ | 436 | 946 | a |
一定条件下,在体积为1L的密闭容器中加入1 mol N2和3 mol H2充分反应,放出热量Q1kJ ,下列说法正确的是( )
 B . a的数值为391
C . Q1的数值为92
D . 相同条件下,反应物若为2molN2和6molH2 , 放出热量Q2>2Q1
B . a的数值为391
C . Q1的数值为92
D . 相同条件下,反应物若为2molN2和6molH2 , 放出热量Q2>2Q1
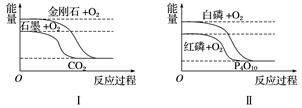
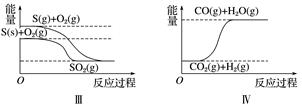
据此判断下列说法中正确的是( )
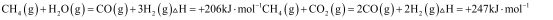
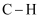 键的键能约为
键的键能约为 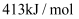 ,
, 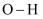 键的键能约为
键的键能约为 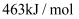 ,
, 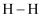 键的键能约为
键的键能约为 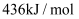 ,则
,则  中
中 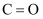 键的键能约为( )
键的键能约为( )
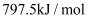 B .
B . 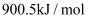 C .
C . 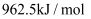 D .
D . 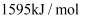
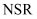 (
(  的储存和还原在不同时段交替进行)技术时有效降低稀燃柴油和汽油发动机尾气中
的储存和还原在不同时段交替进行)技术时有效降低稀燃柴油和汽油发动机尾气中  的排放,其工作原理如图。
的排放,其工作原理如图。 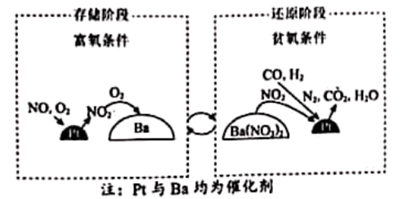
-
(1) 已知:

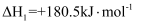
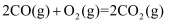
则
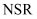 技术工作原理的热化学方程式:
技术工作原理的热化学方程式: 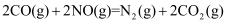
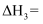 。
。 -
(2) ①存储阶段:
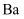 存储
存储  后转化为
后转化为 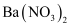 的化学方程式是。
的化学方程式是。 ②还原阶段:
 从
从 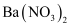 中释放,然后在
中释放,然后在 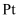 的表面被
的表面被  、
、  还原为
还原为  。若参加反应的
。若参加反应的 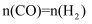 ,则反应的
,则反应的  。
。 -
(3) 某实验小组模拟
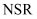 系统中的一个存储、还原过程,让尾气通过
系统中的一个存储、还原过程,让尾气通过 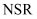 反应器,测得过程中出口
反应器,测得过程中出口  浓度变化如图。
浓度变化如图。 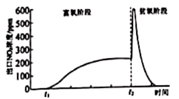
①
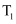 时刻前,
时刻前,  的浓度接近0,原因是。
的浓度接近0,原因是。②
 时刻,切换至贫氧条件。
时刻,切换至贫氧条件。  的浓度急剧上升又快速下降的原因是。
的浓度急剧上升又快速下降的原因是。
 主席在第75届联合国大会提出我国要实现2030年前碳达峰、2060年前碳中和的目标。因此CO2的捕集、利用与封存成为科学家研究的重要课题。
主席在第75届联合国大会提出我国要实现2030年前碳达峰、2060年前碳中和的目标。因此CO2的捕集、利用与封存成为科学家研究的重要课题。
-
(1) I.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:CO2(g)+CH4(g)
 2CO(g)+2H2(g) ∆H
2CO(g)+2H2(g) ∆H 一定压强下,由最稳定单质生成1mol化合物的焓变为该物质的摩尔生成焓。已知CO2(g)、CH4(g)、CO(g)的摩尔生成焓分别为-395kJ·mol-1、-74.9kJ·mol-1、-110.4kJ·mol-1.则上述反应的∆H=kJ·mol-1。
-
(2) 此反应的活化能Ea(正)Ea(逆)(填“>”、“=”或“<”),利于反应自发进行的条件是(填“高温”或“低温”)。
-
(3) 一定温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数Kp=(kPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
-
(4) II.CO2和H2合成甲烷也是CO2资源化利用的重要方法。对于反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ∆H=-165kJ·mol-1 , 催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示。
CH4(g)+2H2O(g) ∆H=-165kJ·mol-1 , 催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示。 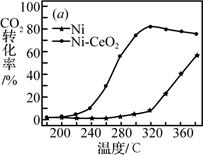
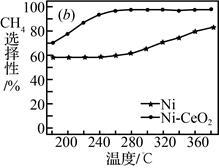
高于320℃后,以Ni-CeO2为催化剂,CO2转化率略有下降,而以Ni为催化剂,CO2转化率却仍在上升,其原因是。
-
(5) 对比上述两种催化剂的催化性能,工业上应选择的催化剂是,使用的合适温度为。
-
(6) III.以铅蓄电池为电源可将CO2转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。
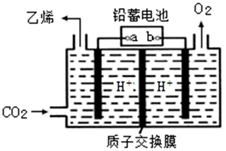
阴极上的电极反应式为;每生成0.5mol乙烯,理论上需消耗铅蓄电池中mol硫酸。
-
(1) 由氢气和氧气反应生成1mol水蒸气放热242kJ,写出该反应的热化学方程式:。
已知断裂1molH2、1molO2的化学键分别需要消耗436kJ、496kJ的能量,则断裂1molH-O所需的能量为kJ。
-
(2) 已知:①CH4(g)+H2O(g)
 CO(g)+3H2(g)△H1=+205.9kJ•mol-1
CO(g)+3H2(g)△H1=+205.9kJ•mol-1 ②CO(g)+H2O(g)
 CO2(g)+H2(g)△H2=-41.2kJ•mol-1
CO2(g)+H2(g)△H2=-41.2kJ•mol-1则反应③:CH4(g)+CO2(g)
 2CO(g)+2H2(g)△H3=kJ•mol-1。
2CO(g)+2H2(g)△H3=kJ•mol-1。写出反应③的平衡常数表达式K=。
-
(3) 若将反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,则该电池正极的电极反应式为:。
-
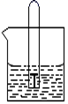
(4) 如图所示,水槽中试管内有一枚铁钉,放置数天后观察,发现试管内液面上升,铁钉表面出现铁锈。该铁钉发生的电化学腐蚀类型为腐蚀,其正极电极反应式为。
-
(1) 用Cl2生产某些含氯有机物时会产生副产物HCl,利用下列反应可实现氯的循环利用:

已知:a.上述反应中,4 mol HCl被氧化,放出115.6 kJ的热量;
b.

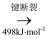

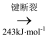
①H2O的电子式为。
②断开1 mol
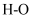 键与断开1 mol
键与断开1 mol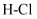 键所需能量相差约为kJ,H2O中
键所需能量相差约为kJ,H2O中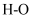 键比HCl中
键比HCl中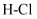 键(填“强”或“弱”)。
键(填“强”或“弱”)。 -
(2) 我国“神舟”系列飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。飞船在光照区运行时,太阳能电池帆板将能转化为能,除供给飞船使用外,多余部分用镉镍蓄电池储存起来。
-
(3) 科学家已研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:
 。制得的氢气可用于燃料电池。
。制得的氢气可用于燃料电池。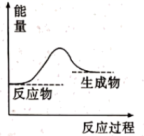
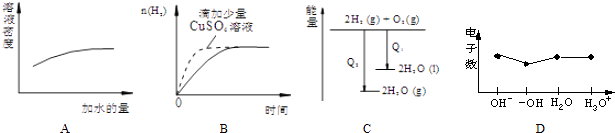
①太阳光分解海水过程中的能量变化如图所示,则该反应属于(填“放热”或“吸热”)反应。反应过程
②某种氢氧燃料电池可用20% KOH溶液作电解质,正极反应式为
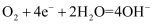 , 则电池的负极反应式为。供电过程中,当消耗氢气11.2L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移电子的物质的量为mol。
, 则电池的负极反应式为。供电过程中,当消耗氢气11.2L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移电子的物质的量为mol。
-
(1) 实验测得,
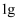 氢气燃烧生成液态水时放出
氢气燃烧生成液态水时放出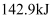 热量,则氢气燃烧的热化学方程式为。
热量,则氢气燃烧的热化学方程式为。
-
(2) 已知:
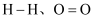 和
和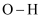 键的键能分别为
键的键能分别为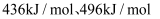 和
和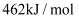 ,
, 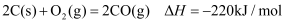 , 则:
, 则: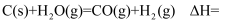
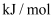
-
(3) 某化学家根据“原子经济”的思想,设计了如下制备
 的反应步骤:
的反应步骤:
①
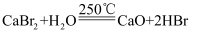
②
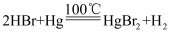
③

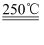 +
+ ④
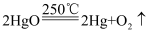
请根据“原子经济”的思想完成上述步骤③的化学方程式:;根据“绿色化学”的思想评估该方法制
 的主要缺点:。
的主要缺点:。 -
(4) 在固态金属氧化物电解池中,高温电解
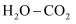 混合气体是制备
混合气体是制备 和
和 的一种新能源利用方式,基本原理如图所示。
的一种新能源利用方式,基本原理如图所示。
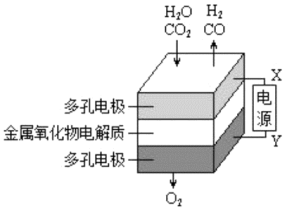
①X是电源的极。
②阴极的反应式有:
 和。
和。③阴、阳两极产生的气体的物质的量之比为。
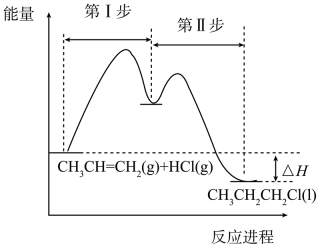
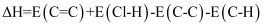 (E表示键能)
D . 1—氯丙烷同分异构体的结构简式为
(E表示键能)
D . 1—氯丙烷同分异构体的结构简式为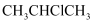
- 美国细胞生物学家威尔逊(E. B.Wilson)曾经说过:“每一个生物科学问题的答案都必须在细胞中寻找”。他作出这一结论
- 古代诗歌阅读(16分) 鹧鸪天 苏轼 林断山明竹隐墙,乱蝉衰草小池塘。翻空白鸟时时见,照水红蕖细细香。 村舍外,
- 有关A、B两河段的叙述。错误的是 A.A河段主要表现为侵蚀作用
- (06全国卷Ⅰ)下列关于动物细胞培养的叙述,正确的是 A.培养中的人效应T细胞能产生单克隆抗体 B.培养中的
- 阅读下列材料 以下材料反映了工业革命在一些方面的影响 材料一 根据1801年首次普查,该郡(英国的约克郡)只有15个城
- 下列物质属于芳香烃,但不是苯的同系物的是()
- 读冬季某区域等压线图,据此回答下列各小题.图中等压线数值排列正确的是 A.P3>P2>P1
- 下列各项中,加点字注音全错的一项是()A.躯壳qiào 香菌jùn 酵jiào母 鞠jū躬尽瘁B.独角jué戏 累léi
- 潮湿的氯气、新制的氯水、次氯酸钠溶液、漂白粉溶液均能使有色布条褪色,这是由于它们含有或能生成( ) A.氯气
- -- I’ll find someone to send this letter to the general hims
- 关于下列各图的说法错误的是( ) A.图甲中4是植物根尖吸收水分、无机盐的主要部位 B.图乙中
- 下列生物中,全部属于生产者的一组是( ) A.海带、梨树、酵母菌 B. 蘑菇、水绵、洋葱 C.马
- 10.如图(a),圆形线圈P静止在水平桌面上,其正上方悬挂一相同的线圈Q、P和Q其轴,Q中通有变化电流,电流随时间变化的
- 下列实验装置或操作与微粒的大小无直接关系的是 ( )
- 梁启超曾称誉美国是“世界共和政体之祖国”,他认为“彼美国者,有两重之政府……各省政府之发生,远在联邦政府以前。虽联邦政府
- ________ did the United States launch the war against Iraq?
- 赫拉克利特有一句名言:“世界是包括一切的整体,它不是由任何神或被任何人创造的,它过去、现在和将来都是按规律燃烧着、按规律
- 下图所反映的历史事件发生在( )A.英国资产阶级革命期间 B.法国大革
- 在香港回归时,英国王储查尔斯代表英国参加了香港政府权力交接仪式。这说明( )A.英国王室仍然行使外交权力
- 下面设想符合能量守恒定律的是( )A.利用永久磁体间的作用力造一台永远转动的机械B.做成一条船利用河水的能量逆水航



