化学能与热能的相互转化 知识点题库
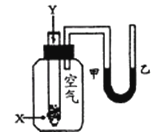
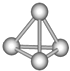
某学生用如图所示装置对化学反应:2X+Y═2Z 进行能量变化情况的研究.当往试管中加入试剂Y时,看到U型管中液面甲处上升,乙处下降.关于该反应的下列叙述:①该反应为放热反应 ②生成物的总能量比反应物的总能量高 ③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来.其中正确的是( )
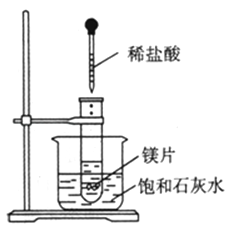
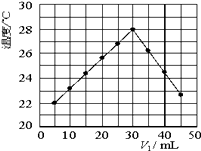
如图所示,把试管放入盛25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5mL盐酸于试管中.
试完成下列问题(提示:氢氧化钙的溶解度随温度升高而降低)
(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式
(4)由实验推知,MgCl2溶液和H2的总能量 (填“大于”“小于”或“等于”)镁片的盐酸的总能量.
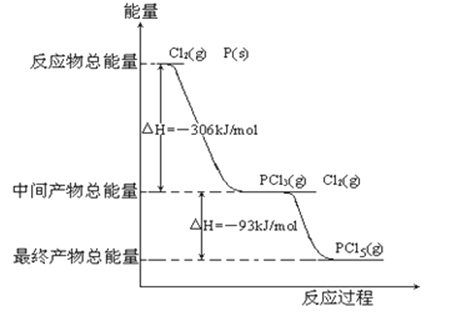
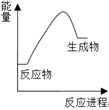
红磷 P(s)和 Cl2(g)发生反应生成 PCl3(g)和 PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成 1 mol 产物的数据).
根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式是
(2)PCl5分解成 PCl3和Cl2的热化学方程式是
(3)P和Cl2分两步反应生成1molPCl5的△H3= P和Cl2一步反应生成1molPCl5的△H4 △H3(填“大于”、“小于”或“等于”).
(4)PCl5 与足量水充分反应,最终生成两种酸,已知反应前后各元素化合价不变,其化学方程式是
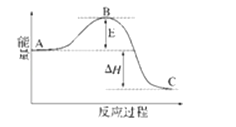
2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3的△H=﹣99kJ•mol﹣1 . 请回答下列问题:
-
(1) 图中A、C分别表示 、 ,E的大小对该反应的反应热有无影响? .该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? ,理由是
-
(2) 图中△H=kJ•mol﹣1
-
(3) V2O5的催化循环机理可能为:V2O5氧化SO2时,自身被还原为四价钒化合物;四价钒化合物再被氧气氧化.写出该催化循环机理的化学方程式
-
(4) 已知单质硫的燃烧热为296kJ•mol﹣1 , 计算由S(s)生成3mol SO3(g)的△H (要求计算过程).
化学键 | Si -O | Si –Cl | H-H | H- Cl | Si -Si | Si -Si |
E(kJ/mol) | 460 | 360 | 436 | 431 | 176 | 347 |
工业上高纯硅可通过下列反制取:SiCl4(g) +2H2(g)= Si(g) +4HCl(g),(已知 1mol晶体Si中2molSi -Si键),该反应产生的热量为( )
 C . 铝热反应是放热反应
D . 吸热反应均需要加热才能发生
C . 铝热反应是放热反应
D . 吸热反应均需要加热才能发生
 B . 蒸发浓缩
B . 蒸发浓缩 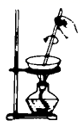 C . 指针发生了偏转
C . 指针发生了偏转 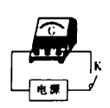 D . 太阳能集热器
D . 太阳能集热器 
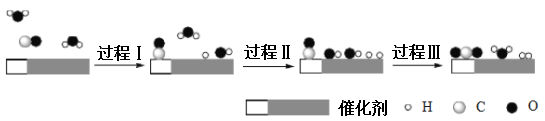
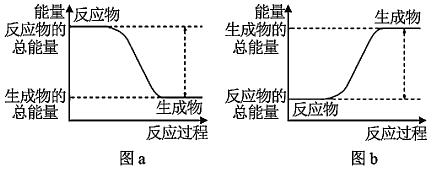
下列说法正确的是( )
- 下图表示当今世界汽车产业转移的一种趋势,读图,回答19~20题。19.甲、乙、丙三地汽车产业向丁地转移的主要原因
- 如图,某工程队要挖一个横断面为矩形ABCD的坑,挖出的土只能沿道路AP、BP运到P处,已知PA=100 m,PB=150
- 合成氨反应为N2+3H22NH3,今有A、B、C、D四个容器,每个容器中有两种操作,两种操作分别达到平衡后,操作1中N2
- 《一千零一夜》中有这样一段文字:有一群鸽子,其中有一部分在树上欢歌,另一部分在地上觅食,树上一只鸽子对地上觅食的鸽子说:
- “跑步热”的兴起,使一些城市的马拉松比赛吸引了众多的爱好者,赛事组织者常常面临报名者众多而参赛名额有限的困难。在解决参赛
- 蚯蚓生活在什么环境中( )A.清澈、缓流、富含有机质的江河中 B.浑浊、急流、富含有机质的江河中C.潮湿
- 图甲是“探究冰的熔化特点”的实验装置,实验中冰的温度随吸热时间变化的图像如图乙所示. (1)将装有适量碎冰的烧杯直接放置
- ∠α的补角为125°,∠β的余角为37°,则α、β的大小关系为α___β.
- 我国长江中下游地区初夏的“梅雨”天气,是由准静止锋造成的。
- 一元二次方程x2﹣2x+m=0有实数根,则m的取值范围在数轴上表示正确的是() A. B. C.
- 已知复数对应的点都在直线上,则 .
- 按照程序框图如图执行,第3个输出的数是 A. 6 B. 5
- 短文填空 A.wrote to B. got C. present D.hoped E. went
- Husband and wife by Arrangement Some Japanese still get m
- 乌克兰是世界三大黑土分布区之一,黑土面积约占全国的三分之二,其北部地区与美国中部平原、中国东北地区并称为世界三大
- 皖南事变的发生,说明 A.国民党消极抗日、积极 B.国民党由抗日转向 C.抗日战争开始进入相持阶段
- 如图所示,在第Ⅰ象限内有垂直纸面向里的匀强磁场,一对正、负电子分别以相同速率沿与x轴成30°角的方向从原点射入磁场,则正
- 有四种化合物W、X、Y、Z,它们都是由短周期元素A、B、C、D、E中的两种元素组成的。已知: (a)A、B、C、D、E五
- 已知正四棱柱ABCD—A1B1C1D1的底面边长为a,侧棱长为2a,则点B1到截面A1BC1的距离为( )A.
- 若A={x} B={x },全集U=R,则A=



