含有氢键的物质 知识点题库
(1)关于H2O:①分子内的O﹣H键,②分子间的范德华力,③分子间氢键,从强到弱顺序为 (填序号),在冰晶体中每个水分子周围有 个紧邻的水分子.
(2)金属钠在三维空间里原子堆积方式为 堆积.
(3)CO32﹣离子中心原子上的孤电子对数为 ,VSEPR模型名称为 .
(4)工业上合成氨的反应方程式为 .
 =.若加水稀释,则CH3COOH⇌CH3COO﹣+H+向右移动,a增大,Ka不变
C . 甲烷的标准燃烧热为﹣890.3 kJ•mol﹣1 , 则甲烷燃烧的热化学方程式可表示为:CH3 (g)+2O2(g)﹣CO2(g)+2H2O(l)△H=﹣890.3 kJ•mol﹣1
D . 500℃、30 MPa下,将0.5 mol N和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)
=.若加水稀释,则CH3COOH⇌CH3COO﹣+H+向右移动,a增大,Ka不变
C . 甲烷的标准燃烧热为﹣890.3 kJ•mol﹣1 , 则甲烷燃烧的热化学方程式可表示为:CH3 (g)+2O2(g)﹣CO2(g)+2H2O(l)△H=﹣890.3 kJ•mol﹣1
D . 500℃、30 MPa下,将0.5 mol N和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) 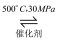 2NH3(g)△H=﹣38.6kJ•mol﹣1
2NH3(g)△H=﹣38.6kJ•mol﹣1
物质及其编号 | 分子式 | 沸点/℃ | 水溶性 | |
① | 甘油 | C3H8O3 | 259 | |
② | 1.2-丙二醉 | C3H8O2 | 188 | 与水以任意比混溶 |
③ | 乙醇 | C2H6O | 197.3 | |
④ | 丙烷 | C3H8 | -42.1 | 难溶于水 |
-
(1) 基态Fe2+的核外电子排布式为。结合电子排布式分析Fe3+比Co3+氧化性弱的原因:。
-
(2) BNCP可用于激光起爆器等,BNCP可由N2H4、HClO4、CTCN、NaNT共反应制备。
①ClO4-的空间构型为。
②CTCN的化学式为
 ,与Co3+形成配位键的原子是。(已知CO32−的结构式为
,与Co3+形成配位键的原子是。(已知CO32−的结构式为 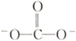 )
)③
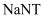 可以
可以 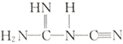 (双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为,
(双聚氰胺为原料制备。双聚氰胺中碳原子杂化轨道类型为, 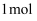
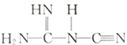 中含有σ键的物质的量为。
中含有σ键的物质的量为。④
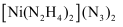 是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为。
是一种富氮含能材料。配体N2H4能与水混溶,除因为它们都是极性分子外,还因为。 -
(3) 一种新型的功能材料的晶胞结构如图所示,Mn在面心和顶点,它的化学式可表示为。
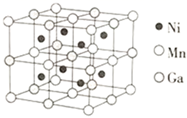
-
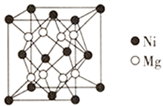
(4) 镍镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。若该晶体储氢时,H2分子在晶胞的体心和棱的中心位置,距离最近的两个H2分子之间的距离为anm。则镍镁晶体未储氢时的密度为(列出计算表达式,NA表示阿伏加德罗常数的数值) g∙cm-3。
①H2O的熔沸点比同主族其他元素氢化物的熔沸点高
②小分子的醇、羧酸可以和水以任意比互溶
③AsH3的熔沸点高于PH3
④水分子高温下也很稳定
⑤邻羟基苯甲酸的熔沸点比对羟基苯甲酸的低
-
(1) 单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经济可行的途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。Ni与CO在60~80℃时反应生成 Ni(CO)4气体,在 Ni(CO)4分子中与Ni形成配位键的原子是 ,Ni(CO)4晶体类型是 。
-
(2) 非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用Cs2CO3、XO2(X=Si、Ge)和H3BO3首次合成了组成为CsXB3O7的非线性光学晶体。回答下列问题:
①SiO2、GeO2具有类似的晶体结构,其中熔点较高的是,原因是。
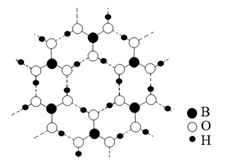
②正硼酸(H3BO3)是一种片层状结构的白色晶体,如图为硼酸晶体的片层结构,层内的H3BO3分子之间通过氢键相连图中“虚线”表示氢键)其中硼的杂化方式为sp2 , H3BO3在热水中比冷水中溶解度显著增大的主要原因是。
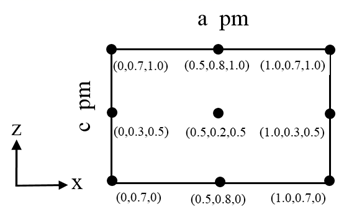
③以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为a pm、b pm、c pm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为 。CsSiB3O7的摩尔质量为M g·mol-1 , 设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为g·cm-3(用代数式表示)。
①离子键与共价键的本质都是静电作用 ②任何物质中都存在化学键 ③氢键是极弱的化学键 ④离子键就是阴、阳离子之间的静电吸引力 ⑤活泼金属与活泼非金属化合时能形成离子键 ⑥任何共价键中,成键原子成键后均满足稳定结构 ⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电 ⑧两种非金属元素形成的化合物不可能含有离子键 ⑨化学键断裂,一定发生化学变化
- 成人体内氨的最主要代谢去路是 A.合成尿素 B.合成非必需氨基酸 C.合成必需氨基酸 D.合成NH随尿排出
- 作函数y=tanx·cosx的图象.
- 电热安全压力锅彻底解决了压力锅的安全问题,解除了普通压力锅困扰消费者多年的安全隐患;省时省电(比普通电饭锅节电30%以上
- 宋朝有一条规矩,“官员不入酒肆”,一旦发现官员在酒店吃喝,不管公款私款,即刻遭到御史弹劾,重则罢官免职,轻则纪律处分。另
- 配制一定物质的量浓度的溶液,造成浓度偏高的操作是: ( ) A. 洗涤后的容量瓶未干燥
- 1. 从这本书中,我知道这个地方有许多的改变。 From the book, I learnt that great _
- 已知△ABC∽△DEF,且相似比为1:2,则△ABC与△DEF的面积比为() A.1:4B.4:1C.1:2D.2:1
- 起重机把重量为1000N的重物匀速提高4m,不计空气阻力,求: (1)钢绳的拉力做多少功? (2)重力做多少功? (3)
- 锻炼身体的方式有多种,游泳是效果较好的一种。在下列相关判断中,正确的是 A.游泳时,神经调节起作用,其他调节不起作用 B
- 如图为一原电池装置,其中X、Y为两电极。对此装置的下列说法中正确的是A.若两电极都是金属,则它们的活动性顺序为:X>
- The doctor said jokingly that his own infection of the viru
- 下列哪项不是健康的生活方式 ( ) A.按时作息,坚持体育锻炼B.不吸烟、不饮酒,营养配餐好C.青少年有些或多或少的心
- --- is it today? --- It's Monday.
- 果蝇是常用的遗传学材料。现有①-④四个果蝇品系(都是纯种),其中品系①的性状均为显性,品系②-④均只有一种性状是隐 性,
- (6分)下图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,B是可溶性碳酸盐,Q、
- 有学者在分析某一重大事件的发动时说:“此举若成功,王权的扩张就会被阻止,而‘自由’又不需要再呼唤一个克伦威尔。”该历史事
- 阅读两则与“赏荷”有关的文言文,完成10—13题。(17分) [甲]水陆草木之花,可爱者甚蕃。晋陶渊明独爱菊。自李唐来
- 完成句子,根据括号内的汉语和句末括号内的英语单词提示完成句子。 1. —How long does it take yo
- 2009年夏末,台风“莫拉克”过后,我国南方部分省市大面积干旱,出现了人畜饮水困难的现象。下列有关水的作用错误的是()
- 下列所示的四种现象中,可用光的直线传播原理解释的是 ( )A.镜中花 B.水中桥



