分子间作用力 知识点题库
下列各组物质气化或熔化时,所克服的粒子间的作用力属于同种类型的是( )
A . 二氧化硅和生石灰的熔化
B . 氯化钠和铁的熔化
C . 碘和干冰的升华
D . 氯化铵受热气化和苯的气化
下列物质中存在分子间作用力的是( )
A . 氯化钠
B . 干冰
C . 金刚石
D . 铁
下列比较中错误的是( )
A . 沸点:CH4>GeH4>SiH4
B . 溶解性:NH3>SO2>Cl2
C . 结合质子的能力:CO32﹣>C6H50﹣>HC03﹣
D . 分散系中分散质粒子的大小:Fe(OH)3浊液>Fe(OH)3胶体>FeCl3溶液
下列情况中分子间相距最近的是( )
A . 0℃的水
B . 3℃的水蒸汽
C . 4℃的水
D . 100℃的沸水
下列物质发生变化时,所克服的粒子间作用力属于同种类型的是( )
A . 酒精和水分别受热变为气体
B . 干冰和氯化铵分别受热变为气体
C . 二氧化硅和铁分别受热融化
D . 食盐和葡萄糖分别溶解在水中
在单质的晶体中一定不存在( )
A . 离子键
B . 分子间作用力
C . 共价键
D . 金属离子与自由电子间的作用
将下列晶体熔化:过氧化钠、二氧化硫、氯化铵、二氧化硅,需要克服的微粒间的相互作用①共价键 ②离子键 ③分子间作用力,符合题意的顺序是( )
A . ①②②③
B . ②①②③
C . ②③②①
D . ②③①③
下列说法不正确的是( )
A . Mg2+和S2-的最外电子层都形成了8个电子的稳定结构
B . 石英和金刚石都是原子间通过共价键结合形成的原子晶体
C . 浓硫酸和H2O混合时放出热量与微粒之间的作用力有关
D . H2O2易分解是因为H2O2分子间作用力弱
下列说法中正确的是 ( )
A . 氢键是一种较弱的化学键
B . NH3的稳定性很强,是因为其分子间能形成氢键
C . 常温下Cl2、Br2、I2状态由气态到固态变化的主要原因是分子间作用力在逐渐增大
D . 最外层能达到稳定结构的微粒只是稀有气体的原子
下列有关化学键、氢键和范德华力的叙述中,不正确的是 ( )
A . 金属键是金属离子与“电子气”之间的较强作用,金属键无方向性和饱和性
B . 共价键是原子之间通过共用电子对形成的相互作用,共价键有方向性和饱和性
C . 范德华力是分子间存在的一种作用力,分子的极性越大,范德华力越大
D . 氢键不是化学键而是分子间的一种作用力,所以氢键只存在于分子与分子之间
下列关于微粒间作用力与晶体的说法不正确的是( )
A . 某物质呈固体时不导电,熔融状态下能导电,则该物质一定是离子晶体
B . H2O和CCl4的晶体类型相同,且每个原子的最外层都达到8电子稳定结构
C . F2、Cl2、Br2、I2的沸点逐渐升高,是因为分子间作用力逐渐增大
D . 干冰溶于水中,既有分子间作用力的破坏,也有共价键的破坏
近年来,德国研究人员利用O2、N2、CH4、NH3、H2O和HCN这6种远古地球上存在的简单物质,再使用硫醇和铁盐等物质模拟当时环境,成功制得核酸的4种基本模块。下列说法正确的是( )
A . O2的沸点比N2的低
B . NH3分子呈三角锥形
C . 配离子[Fe(H2O)6]3+中H与中心原子配位
D . 元素C、N、O、S的第一电离能依次增大
下列说法正确的是( )
A . Na2O2和NaOH所含化学键类型完全相同
B . NH3比PH3稳定是因为NH3分子间存在氢键
C . CO2溶于水和干冰升华都只有分子间作用力改变
D . NaHSO4溶于水电离的过程既破坏离子键又破坏共价键
下列关于范德华力与氢键的叙述中正确的是( )
A . 任何物质中都存在范德华力,而氢键只存在于含有 N、O、F 的物质中
B . 范德华力比氢键的作用还要弱
C . 范德华力与氢键共同决定物质的物理性质
D . 范德华力与氢键的强弱都只与相对分子质量有关
下列物质在变化过程中,只需克服分子间作用力的是( )
A . 食盐熔化
B . 干冰升华
C . 氯化铵受热,固体消失
D . 氯化氢溶于水
下列各组物质发生变化时,所克服的微粒间作用力属于同种类型的是( )
A . 二氧化硅和生石灰的熔化
B . 加热氯化铵和水
C . 碘和干冰的升华
D . 氯化钠和硫的汽化
由解放军总装备部军事医学研究所研制的小分子团水,解决了医务人员工作时的如厕难题。新型小分子团水,具有饮用量少、渗透力强、生物利用度高、在人体内储留时间长、排放量少的特点。一次饮用125mL小分子团水,可维持人体6小时正常需水量。下列关于小分子团水的说法正确的是( )
A . 水分子的化学性质改变
B . 水分子中氧氢键长缩短
C . 小分子团水是一种新化合物
D . 水分子间结构、物理性质改变
 和
和  都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示: 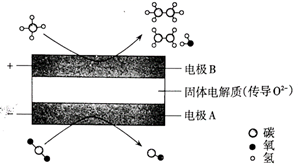
-
(1) C、N、O三种元素的第一电离能由大到小的顺序是(填元素符号)。
-
(2) 下列有关乙烷(
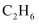 )和乙烯(
)和乙烯( 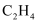 )的描述正确的是___________(填字母)。
A . 分子中均含有
)的描述正确的是___________(填字母)。
A . 分子中均含有 键和
键和  键
B . 分子中的所有原子均处于同一平面上
C . 分子中的碳碳键键长:乙烯>乙烷
D . 乙烯中碳原子的杂化轨道类型为
键
B . 分子中的所有原子均处于同一平面上
C . 分子中的碳碳键键长:乙烯>乙烷
D . 乙烯中碳原子的杂化轨道类型为 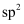
-
(3) 已知相同条件下生成乙烯和乙烷的体积比为2:1,消耗
 和
和  的体积比为6:5,则生成的CO和
的体积比为6:5,则生成的CO和  的物质的量之比为。
的物质的量之比为。
-
(4) ①已知碳和硅的有关化学键键能如下所示:
化学键
C-C
C-H
Si-Si
Si-H
键能/(
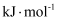 )
)356
413
226
318
简要分析乙烷的稳定性大于
 的原因:。
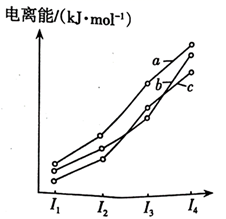
的原因:。②如图表示碳、硅和磷三种元素的四级电离能变化趋势,其中表示硅的曲线是(填字母),判断的依据是。
-
(5) ①通常情况下,与乙烯的沸点(-103.7℃)相比,氯乙烯(
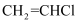 )的沸点更高(-13.9℃),其原因是。
)的沸点更高(-13.9℃),其原因是。 ②在乙烯中碳碳双键的键长为134pm,而在氯乙烯中碳碳双键的键长为138pm,请解释原因:。
下列事实能用键能大小解释的是( )
A . 常温常压下,氟单质呈气态,碘单质呈固态
B . 氮气的化学性质比氧气稳定
C . 氦气一般很难发生化学反应
D . 盐酸易挥发,而硫酸难挥发
下列说法正确的是( )
A . 分子间作用力越大,分子越稳定
B . 分子间作用力越大,物质的熔、沸点越高
C . 相对分子质量越大,其分子间作用力越小
D . 分子间只存在范德华力
最近更新
- the occasional visit, what else does Alan do f
- 阅读下面一段文言文,完成1—4题。 周维城传 清·张惠言 嘉庆元年,余游富阳,知县恽候请余修县志,未及属稿
- 在远距离输电时,输送的电功率为P,输电电压为U,所用导线电阻率为ρ,横截面积为S,总长度为L,输电线损失的电功率为P′,
- 下图为某一区域M、N两物种的资源利用曲线,叙述不正确的是A.该曲线表明M、N之间为竞争关系 B.b越大表明该生物适应环境
- 如果采用分层抽样,从个体数为N的总体中,抽取一个容量为n的样本,那么每个个体被抽到的概率等于( )A.
- —I think math is more useful than P.E.—I don't______you.They
- 按粒子的半径从小到大顺序排列的是() A.Cl、S、P
- 在△ABC中,若,则( ) A. B. C. D.
- 如图所示,有一带负电的粒子,自A点沿电场线运动到B点,在此过程中该带电粒子 ( ) A、所受的电场
- 商纣王的“炮烙之刑”是属于 (
- 由两种气态烃组成的混合气体,其平均组成为C2H3,因此混合气体的成分和体积之比可能是()A.C2H2和C2H4,体积比为
- 方程(x2-4)2+=0表示的图形是( )A.两条直线 B.两个点 C.四
- 据报道,我国登记的个体工商户为2 423万户,私营企业202.86万户,从业人员达7 474万人,注册资金21 648亿
- 下列关于浓硫酸的叙述正确的是( )
- 下列各句中,没有语病的一句是 ( )
- It took me a long time before I was able to fully appreciate
- Will you ________ playing basketball? A.join us in B.j
- 铁制品在通常情况下很易生锈,制造时往往在铁制品表面电镀一层铜起防锈作用。下列说法正确的是( )A.镀铜铁制品不可
- 下列图形中,正确画出AC边上的高的是( ).
- 如图所示,弹簧测力计挂一铁块A,烧杯中盛有稀硫酸溶液B,此时发生反应的化学方程式为



