用电子式表示简单的离子化合物和共价化合物的形成 知识点题库
近年来研制的NH3气体可用作氟化氢一氟化氚高能化学激光器的氟源,也可作为火箭推进剂,NF3可用NH3与氟气制取,化学方程式为:4NH3+3F2=NF3+3NH4F,下列说法不正确的是( )
A . NF3的形成过程用电子式可表示为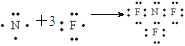 B . NF3的氧化性大于F2
C . NF3分子空间构型为三角锥形
D . NH4F中既有离子键又有极性共价键
B . NF3的氧化性大于F2
C . NF3分子空间构型为三角锥形
D . NH4F中既有离子键又有极性共价键
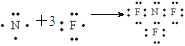 B . NF3的氧化性大于F2
C . NF3分子空间构型为三角锥形
D . NH4F中既有离子键又有极性共价键
B . NF3的氧化性大于F2
C . NF3分子空间构型为三角锥形
D . NH4F中既有离子键又有极性共价键
下列有关化学用语表示错误的是( )
A . 原子核内有10个中子的氧离子: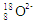 B . 鸟粪石中2种阳离子的电子式分别为
B . 鸟粪石中2种阳离子的电子式分别为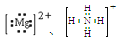 C . 氧与氟形成的化合物OF2中,氧元素的化合价为+2价
D . 在Mg18O晶体中,阴离子结构示意图可表示为
C . 氧与氟形成的化合物OF2中,氧元素的化合价为+2价
D . 在Mg18O晶体中,阴离子结构示意图可表示为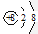
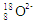 B . 鸟粪石中2种阳离子的电子式分别为
B . 鸟粪石中2种阳离子的电子式分别为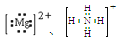 C . 氧与氟形成的化合物OF2中,氧元素的化合价为+2价
D . 在Mg18O晶体中,阴离子结构示意图可表示为
C . 氧与氟形成的化合物OF2中,氧元素的化合价为+2价
D . 在Mg18O晶体中,阴离子结构示意图可表示为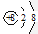
(1)写出铝粉与氧化铁粉在高温下反应的化学方程式,并用双线桥表示下列反应中电子转移方向和数目:
(2)过氧化钠的电子式为 ,它是由Na+与 (填写离子符号)构成的.
下列关于化学键和化合物的说法中正确的是( )
A . 化学键的形成一定伴随着电子的得失
B . 金属元素和非金属元素形成的化合物一定是离子化合物
C . 非金属元素组成的化合物一定是共价化合物
D . 含有阴离子的化合物中一定含有阳离子
下列化学用语对事实的表述错误的是( )
A . 氢氧化钠溶液与二氧化硅反应:SiO2+2OH-=SiO32-+H2O
B . 常温时,0.1mol·L-1氨水的pH=11.1:NH3·H2O  NH4++OH-
C . 由Na和Cl形成离子键的过程:
NH4++OH-
C . 由Na和Cl形成离子键的过程:  D . 大理石与醋酸反应CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑
D . 大理石与醋酸反应CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑
 NH4++OH-
C . 由Na和Cl形成离子键的过程:
NH4++OH-
C . 由Na和Cl形成离子键的过程:  D . 大理石与醋酸反应CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑
D . 大理石与醋酸反应CO32-+2CH3COOH=2CH3COO-+H2O+CO2↑
下列有关化学用语的表示方法中正确的是( )
A . 次氯酸的电子式: 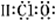 B . M2+离子核外有a个电子,b个中子,M原子符号为
B . M2+离子核外有a个电子,b个中子,M原子符号为 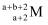 C . 用电子式表示MgCl2的形成过程为:
C . 用电子式表示MgCl2的形成过程为: 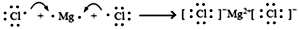 D . Na+的结构示意图:
D . Na+的结构示意图: 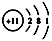
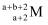 C . 用电子式表示MgCl2的形成过程为:
C . 用电子式表示MgCl2的形成过程为:
下列化学用语正确的是( )
A . 用电子式表示氯化氢分子的形成过程: 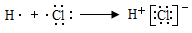 B . HClO的结构式:H—Cl—O
C . 比例模型
B . HClO的结构式:H—Cl—O
C . 比例模型  可以表示甲烷分子,也可以表示四氯化碳分子
D . H2O的电子式:
可以表示甲烷分子,也可以表示四氯化碳分子
D . H2O的电子式: 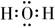
下表是元素周期表的一部分,请用化学符号回答有关问题:
|
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||||||
| 1 | ① | |||||||||||||
| 2 | ② | ③ | ④ | ⑤ | ||||||||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
-
(1) 表中化学性质最不活泼的元素,其原子结构示意图为 。
-
(2) ②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是,最高价氧化物的水化物中酸性最强的是 。
-
(3) 第三周期元素形成的简单离子中半径最小的微粒是,写出该元素的单质分别与⑥、⑩最高价氧化物的水化物反应的离子方程式、 。
-
(4) 元素③的氢化物的电子式是;该氢化物与元素⑩的氢化物发生反应的化学方程式。
-
(5) 用电子式分别写出元素⑩与元素②、⑥形成化合物过程 、。
一种高品质的磷矿石——鸟粪石的化学式为MgNH4PO4 , 下列关于该物质的结构和性质的推测中不合理的是( )
A . 鸟粪石既属于镁盐又属于磷酸盐
B . 鸟粪石既能和强酸反应又能和强碱反应
C . 鸟粪石中既含有离子键又含有共价键
D . 鸟粪石中两种阳离子的电子式分别为 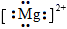 、
、 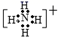
A、B、C、D是四种短周期元素,E是过渡元素,A、B、C同周期,C、D同主族,A原子M层电子数是L层的一半,B是同周期第一电离能最小的元素,C在同周期中未成对电子数最多,E的外围电子排布式为3d64s2。回答下列问题:
-
(1) 写出下列元素的名称:A B C D
-
(2) 上述五种元素中最高价氧化物对应水化物酸性最强的是(用化学式表示,下同),碱性最强的是 。
-
(3) D所在周期第一电离能最小的元素是,电负性最大的元素是。(填元素符号)
-
(4) D的氢化物比C的氢化物的沸点(填“高”或“低”),原因是 。
-
(5) E元素原子的核电荷数是,E元素在周期表的位置是 ,E元素处于周期表分区中的区。
-
(6) 画出D的核外电子排布图,E的外围电子排布图。
-
(7) 用电子式表示B的硫化物的形成过程:。
-
(1) 下列物质N2、H2O、Na2O2、 CaCl2、KOH、NaF中,既含有离子键,又含有共价键的物质是,属于共价化合物的是。
-
(2) 用电子式表示CaCl2的形成过程:。
-
(3) 氮化钠(Na3N)是科学家制备的一种重要化合物,它与水作用产生NH3。请写出NH3的电子式是。
-
(4) Na3N与盐酸反应生成两种盐,反应的化学方程式为。
下列化学用语中正确的是( )
A . HCl的形成过程: 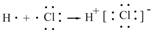 B . Na2S的电子式:
B . Na2S的电子式: 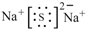 C . N2的结构式:︰N≡N︰
D . Cl–结构示意图:
C . N2的结构式:︰N≡N︰
D . Cl–结构示意图: 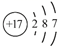
下表为元素周期表的一部分,请回答有关问题:
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
|
1 |
① |
|||||||
|
2 |
② |
③ |
④ |
|||||
|
3 |
⑤ |
⑥ |
⑦ |
⑧ |
||||
|
4 |
⑨ |
⑩ |
-
(1) 已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为。
-
(2) 由元素②和④形成的三核分子的结构式为。
-
(3) 用电子式表示元素⑤和⑦的原子形成的化合物(该化合物含有三个原子核)的形成过程。
-
(4) 由上述元素④和⑤构成的淡黄色固体,该化合物所含的化学键类型为(填“离子键”、“极性键”或“非极性键”), ④和⑦的氢化物稳定性较强的是、沸点较高的是(填化学式)⑧和⑩的氢化物还原性较强的是(填化学式)。
-
(5) 元素⑦、⑧、⑨的离子半径由大到小的顺序是(用离子符号表示);元素⑨的最高价氧化物的水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为。
-
(6) 铍和⑥二者的单质、化合物均具有相似的化学性质,写出BeCl2溶液与Na2BeO2的水溶液混合的化学方程式。
-
(7) 假设元素⑧的对应元素符号为X,若在一定条件下,X单质能够与硫反应生成一种用途广泛的硫化剂S2X2。该硫化剂S2X2与足量水反应有淡黄色沉淀生成,同时生成能够使品红溶液褪色的无色气体,则该反应的化学方程式是(元素X请用具体元素符号表示)。
-
(1) I.按要求回答下列问题:
某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是。
-
(2) 写出下列物质的电子式:Mg(OH)2,NH3,Na2O2。
-
(3) 用电子式表示下列化合物的形成过程:Na2S;CO2。
-
(4) Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
①
⑥
⑦
②
④
⑤
⑧
③
⑩
⑨
②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是(填化学式)。
-
(5) 10种元素中,简单离子半径最大的是填离子符号)。
-
(6) 元素⑦的简单氢化物与过量的元素⑧的单质反应的化学方程式为。
-
(7) 元素⑩的原子序数为,其单质与水在高温下反应的化学方程式为。
-
(8) 元素①⑦⑧形成的常见化合物的化学式,含有化学键类型、。
下列有关化学用语正确的是( )
A . 次氯酸电子式: 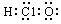 B . 乙醇的分子式:C2H5OH
C . 用电子式表示氯化氢分子的形成过程:
B . 乙醇的分子式:C2H5OH
C . 用电子式表示氯化氢分子的形成过程: 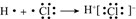 D . CS2分子比例模型:
D . CS2分子比例模型: 
已知 X、Y、Z、W、Q 为五种原子序数依次增大的短周期主族元素,常温下 X 能与氢元素形成两种常见的液态化合物,W 的原子序数是 X 的两倍;Z 的离子半径在同周期简单离子中最小,Y 的最高价氧化物对应的水化物和 Z 的最高价氧化物对应的水化物能发生反应。
请回答:
-
(1) Q 在元素周期表中的位置: 。
-
(2) Y的最高价氧化物的水化物中存在的化学键类型: 。
-
(3) X的简单氢化物比 W 的简单氢化物熔沸点高的原因: 。
-
(4) Z与Q两者的最高价氧化物对应的水化物反应的离子方程式: 。
-
(5) Y的氢化物可由单质化合而成,请用电子式表示该氢化物形成过程: 。
偏二甲肼(C2H8O2)是长征系列火箭的动力燃料之一,其制备方法为:C2H6O2+2Zn+4HCl=2ZnCl2+H2O+C2H8O2 , 下列说法错误的是( )
A . N原子的结构示意图为:  B . H2O的比例模型:
B . H2O的比例模型:  C . 12C与14C互为同位素
D . HCl的形成过程为:
C . 12C与14C互为同位素
D . HCl的形成过程为: 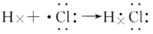
 B . H2O的比例模型:
B . H2O的比例模型:
下列化学用语正确的是( )
A . 中子数为18的氯原子: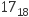 Cl
B . CO2分子的电子式:
Cl
B . CO2分子的电子式: C . 顺-2-丁烯的结构简式:
C . 顺-2-丁烯的结构简式: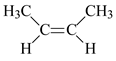 D . 铝离子的结构示意图:
D . 铝离子的结构示意图:
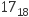 Cl
B . CO2分子的电子式:
Cl
B . CO2分子的电子式: C . 顺-2-丁烯的结构简式:
C . 顺-2-丁烯的结构简式: D . 铝离子的结构示意图:
D . 铝离子的结构示意图:
现有A、B、C、D、E五种短周期主族元素,原子序数依次增大。已知A、D同主族,常温下A、B组成的气态化合物能使湿润的红色石蕊试纸变蓝,C是地壳中含量最高的元素,A、B、C、D四种元素的最外层电子数之和与E的原子序数等。下列说法中错误的是( )
A . 最简单氢化物的稳定性:C>B
B . A,B,C三种元素只能形成共价化合物
C . A,C,D形成的化合物的电子式为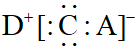 D . 常温下,E在B的最高价氧化物对应水化物的浓溶液中会钝化
D . 常温下,E在B的最高价氧化物对应水化物的浓溶液中会钝化
如表为元素周期表的一部分,请回答有关问题
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
-
(1) 已知元素⑩的一种核素,其中中子数为45,用原子符号表示该核素为。
-
(2) 由元素③形成的单质分子的结构式为,用电子式表示⑤和⑧两元素形成化合物的过程。
-
(3) 由上述元素构成的淡黄色固体化合物的电子式,该化合物所含的化学键类型(填“离子键”、“极性键”或“非极性键”)。
-
(4) 元素⑦、⑧、⑨其离子半径由大到小的顺序是(用离子符号),元素⑤的最高价氧化物的水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为。
-
(5) 下列事实不能说明元素⑧的非金属性比元素⑦的非金属性强的是____。A.元素⑧的单质与⑦的氢化物的水溶液反应,溶液变浑浊A . 元素⑧的单质能将Fe氧化成三价铁,而元素⑦的单质只能将铁氧化成二价铁 B . ⑦和⑧两元素的简单氢化物受热分解,后者的分解温度高 C . 元素⑧的氢化物的水溶液的酸性比元素⑦的氢化物水溶液的酸性强
最近更新
- 补写出下列名句名篇中的空缺部分。 (1) , ,
- 历史学家钱穆指出“在此制度下,人民优秀分子均有参政之机会,新陈代谢,决无政治上之特权阶级”。他所指的这一制度是 A.世官
- 2019年8月28日,浙江省金华市婺城区城东街道青春路社区的会议室里正在举行第一届“你好,邻居”
- 《说文解字》解释说:“宗,尊祖庙也。”也就是说,宗法的“宗”的本义是宗庙。这说明宗法制以什么为纽带A.财产
- 函数的性质通常指函数的定义域、值域、周期性、单调性、奇偶性等,请选择适当的探究顺序,研究函数f(x)= +的性质,并在此
- 由铜、锌和稀盐酸组成的原电池中,铜是________极,发生________反应,电极反应式是________;锌是__
- 下列说法正确的是 A.许多元素能自发地放出射线,使人们开始认识到原子是有复杂结构的 B.工业部门可以使用放射线
- 某器官炎症,导致细胞内淀粉酶过多地进入血液,该器官是 A.肝脏 B.胃 C.胰腺
- 某养老院护工刘女士说:“孙老太太有儿有女,却没人照看其生活,自从被送进养老院,就再也没人交过护理费了。&rd
- 17.下列各句中加点成语的使用,全都正确的一项是(3分) ①从历史上看,人类社会每一个新时代的开启,似乎都与技术变革息息
- 如下图所示,是使用游标卡尺和螺旋测微器分别测量两个工件时的情况.图中游标卡尺的读数为________mm,螺旋测微器的读
- PART THREE: READING COMPREHENSIONDirections: Read the follow
- Welcome to your future life! You get up in the mornin
- 直接参与体内细胞与外界环境之间气体交换的系统是 A.循环系统和消化系统 B.消化系统和呼吸系统
- 我国首台自主设计研发的载人深潜器“蛟龙号”在2012年6月27日进行了7 000 m级海试,最大下潜深度达7 062 m
- 6﹣(+3)﹣(﹣7)+(﹣2);
- 已知a、b、c是三条不重合的直线,α、β、γ是三个不重合的平面.下列命题中正确的是( )①a∥c,b∥ca∥b;②
- 僧肇说:“旋岚偃岳而常静,江河竞注而不流,野马飘鼓而不动,日月历天而不周。复何怪哉?”下列观点中与其错误相近的是(
- 阅读下面文言文,回答9—13题。 ①子曰:“学而时习之,不亦说(yuè)乎?有朋自远方来,不亦乐乎?人不知而不愠(yùn
- 小明家安装自来水管时,将一根水管截成长短不同的两段,则这两段水管 ( )A.质量相等B.密度相等C.重力相等D.



