共价键的形成及共价键的主要类型 知识点题库
在下列变化过程中,既有离子键被破坏又有共价键被破坏的是( )
A . 将SO2通入水中
B . 火碱溶于水
C . 将HCl通入水中
D . 硫酸氢钠溶于水
下列物质中,只含共价键的化合物是( )
A . N2
B . CO2
C . MgO
D . NaOH
下列叙述正确的是( )
A . 离子键只存在于金属阳离子与酸根阴离子之间
B . 两种非金属元素形成AB型化合物,它一定含共价键
C . 物质中化学键破坏了,一定发生化学变化
D . 化学键类型一定由元素类别决定
下列物质中属于共价化合物的是( )
A . HNO3
B . NaHSO4
C . Na2O2
D . I2
下列物质中,既含共价键又含离子键的是( )
A . KCl
B . H2O
C . Na2O2
D . CO2
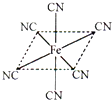
铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成黄血盐,其配离子结构如图;已知CN﹣与N2结构相似,1molCN﹣中π键数目为.
下列物质属于共价化合物的是( )
A . NH4Cl
B . MgO
C . H2O
D . CaCl2
关于乙醇分子的说法正确的是( )
A . 分子中共含有8个极性键
B . 分子中不含非极性键
C . 分子中只含σ键
D . 分子中含有1个π键
A、B、C、D是原子序数依次递增的前四周期元素,A元素的正化合价与负化合价的代数和为零;B元素原子的价电子结构为nsnnpn;C元素基态原子s能级的电子总数比p能级的电子总数多1;D元素原子的M能层全满,最外层只有一个电子。请回答:
-
(1) A 元素的单质为A2 , 不能形成A3或A4 , 这体现了共价键的性;B元素单质的一种空间网状结构的晶体熔点>3550℃,该单质的晶体类型属于;基态D原子共有种不同运动状态的电子。
-
(2) A与C形成的最简单分子的中心原子杂化方式是,该分子与D2+、H2O以2:1:2的配比结合形成的配离子是(填化学式),此配离子中的两种配体的不同之处为(填标号)。
①中心原子的价层电子对数 ②中心原子的孤电子对的对数 ③中心原子的化学键类型 ④VSEPR模型
-
(3) 1molBC—中含有的π键数目为;写出与BC-互为等电子体的分子和离子各一种、。
-
(4) D2+的硫酸盐晶体的熔点比D2+的硝酸盐晶体的熔点高,其原 因是。
-
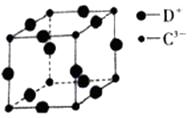
(5) D3C 具有良好的电学和光学性能,其晶体的晶胞结构如图所示,D+和C3—半径分别为apm、bpm,D+和C3—都是紧密接触的刚性小球,则C3—的配位数为,晶体的密度为g·cm-3。
下列属于共价化合物的是( )
A . NH4NO3
B . CH4
C . CaCl2
D . C60
下列物质中属于共价化合物的是( )
A . HCl
B . Na2CO3
C . NaCl
D . N2
H2O分子中每个O原子结合2个H原子的根本原因是( )
A . 共价键的方向性
B . 共价键的键长
C . 共价键的键角
D . 共价键的饱和性
下列过程中,共价键被破坏的是( )
A . 碘升华
B . 溴蒸气被木炭吸附
C . 水结为冰
D . 氯化氢气体溶于水
三氯化氮(NCl3)是一种淡黄色的油状液体,其分子空间构型与NH3相似。则下面对于NCl3的描述正确的是 ( )
A . 是由极性键形成的非极性分子
B . 它的挥发性比PBr3要小
C . 它还能再以配位键与H+结合
D . Cl-N-Cl的键角是120°
下列各组物质中所含化学键均只有共价键的是( )
A . NaCl和K2O2
B . HCl和H2O
C . HNO3与NH4NO3
D . K2SO4与SO3
下列物质的构成微粒中,不含共价键的是( )
A . MgCl2
B . Cl2
C . HCl
D . NaOH
下列说法正确的是( )
A . 反应H2+Cl2  2HCl,破坏了原有共价键又形成了新的共价键
B . NaOH熔化时,既破坏了离子键又破坏了共价键
C . 破坏化学键的过程,一定是化学变化过程
D . 35Cl和37Cl的相互转化属于化学变化
2HCl,破坏了原有共价键又形成了新的共价键
B . NaOH熔化时,既破坏了离子键又破坏了共价键
C . 破坏化学键的过程,一定是化学变化过程
D . 35Cl和37Cl的相互转化属于化学变化
 2HCl,破坏了原有共价键又形成了新的共价键
B . NaOH熔化时,既破坏了离子键又破坏了共价键
C . 破坏化学键的过程,一定是化学变化过程
D . 35Cl和37Cl的相互转化属于化学变化
2HCl,破坏了原有共价键又形成了新的共价键
B . NaOH熔化时,既破坏了离子键又破坏了共价键
C . 破坏化学键的过程,一定是化学变化过程
D . 35Cl和37Cl的相互转化属于化学变化
在乙烯分子中有5个σ键和1个π键,它们分别是( )
A . sp2杂化轨道形成σ键,未杂化的2p轨道形成π键
B . sp2杂化轨道形成π键,未杂化的2p轨道形成σ键
C . C-H之间是sp2杂化轨道形成σ键,C-C之间是未杂化的2p轨道形成π键
D . C-C之间是sp2杂化轨道形成σ键,C-H之间是未杂化的2p轨道形成π键
下列说法正确的有几句( )
①离子键与共价键的本质都是静电作用 ②任何物质中都存在化学键 ③氢键是极弱的化学键 ④离子键就是阴、阳离子之间的静电吸引力 ⑤活泼金属与活泼非金属化合时能形成离子键 ⑥任何共价键中,成键原子成键后均满足稳定结构 ⑦验证化合物是否为离子化合物的实验方法是可以看其熔化状态下能否导电 ⑧两种非金属元素形成的化合物不可能含有离子键 ⑨化学键断裂,一定发生化学变化
A . 1
B . 2
C . 3
D . 4
下列说法错误的是( )
A . 杂化轨道可用于形成 键和
键和 键
B . 若中心原子杂化方式相同,分子中孤电子对数越多,键角越小
C .
键
B . 若中心原子杂化方式相同,分子中孤电子对数越多,键角越小
C .  和
和 的
的 空间构型和分子空间构型均不一致
D . 价电子对互斥理论一般不适用于推测过渡金属化合物分子的空间构型
空间构型和分子空间构型均不一致
D . 价电子对互斥理论一般不适用于推测过渡金属化合物分子的空间构型
 键和
键和 键
B . 若中心原子杂化方式相同,分子中孤电子对数越多,键角越小
C .
键
B . 若中心原子杂化方式相同,分子中孤电子对数越多,键角越小
C .  和
和 的
的 空间构型和分子空间构型均不一致
D . 价电子对互斥理论一般不适用于推测过渡金属化合物分子的空间构型
空间构型和分子空间构型均不一致
D . 价电子对互斥理论一般不适用于推测过渡金属化合物分子的空间构型
最近更新
- 如图,在正方形ABCD中,边长为2的等边三角形AEF的顶点E、F分别在BC和CD上,下列结论:①CE=CF;②∠AEB=
- 设P为双曲线-y2=1上一动点,O为坐标原点,M为线段OP的中点,则点M的轨迹方程是________.
- 下图是水循环示意图,读图完成下列各题。(8分) (1)将图中未标明箭头的线段标出箭头,以表示完整的水循环过程。(1分)
- 地沟油,泛指在生活中存在的各类劣质油。由于地沟油中含有杂质及有毒物质,很多人猜想它的密度应该比正常食用油的密度要大,为了
- 用所给词的适当形式填空。work, close, look, have, teacher’s, pen, eat, Ch
- 某双链DNA分子中,作为模板链的部分碱基的排列顺序是: G-C-A-G-T-A-C-C-G-C-G-T-C-A-T.已知
- 某农场种植甲乙两种不同品种的水稻,6年中各年每亩的平均产量如下(单位Kg) 甲450 458 450 425
- (2013年5月武汉市模拟)如图所示是由地面同一点踢出的足球的三条飞行路径,三条路径的最高点是等高的。忽略空气对飞行的影
- 常温下,将1体积pH=2.5的盐酸与10体积NaOH溶液混合,两者恰好完全反应,则NaOH溶液的pH等于 A.11.5
- 做匀速直线运动的甲、乙两物体从某地同时同向出发,它们的路程随时间变化的图像如图6所示。则两物体运动较快的是
- 新鲜的叶类蔬菜表面常残留水溶性有机农药。现取同一新鲜蔬菜若干,浸入一定量纯水中,每隔一段时间,取出一小片菜叶,测定其细胞
- 子弹从枪膛里射出以后仍然向前飞行,这是由于( ) A.子弹受到一个向前的推力
- 甲参加一次英语口语考试,已知在被选的10道题中甲能答对其中6题,现从10道备选题中随机抽取3道进行测试,求甲答对试题数ξ
- 某研究性学习小组的同学利用下列装置探究植物的呼吸作用,请分析回答: (1)通过上图所示实验,可以得出的结论是______
- 谁也不曾料到,这是如此艰难的一年。2008,我们热切期待的阳光和欢笑,却不料被一路风暴阻隔。2月肆虐的雪灾,冻裂了中国大
- 选出含有三个错别字的一项:( )A、消费者向消协反应,一些商家以打折为诱饵,设下陷井,坑害百姓,商家的这种做法将遗害
- (6分)电场中某点的电场强度为E=6.0×105N/C,放在该点的点电荷受到电场力为F=3.0×10-4N,求该点电荷的
- 如图所示是一颗子弹以120米/秒的速度将纸牌击穿瞬间的情形,这一情形反映了力的作用效果.子弹对纸牌的力使纸牌发生了
- (12分)已知:①A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平;②2CH3CHO+O22CH3C
- 在斯巴达,虽然公民大会名义上是国家最高权力机关,但王位世袭,国王垄断了军事统帅权;长老会议员仅30人,且终身任职;监察官



