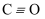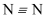共价键的形成及共价键的主要类型 知识点题库
由原子轨道相互重叠形成的σ键和π键总称价键轨道,是分子结构的价键理论中最基本的组成部分。关于该理论下列有关认识不正确的是( )
A . σ键不属于共价键,是另一种化学键
B . s-sσ键与s-pσ键的对称性相同
C . 分子中含有共价键,则至少含有一个σ键
D . 含有π键的化合物与只含σ键的化合物的化学性质不同
有下列物质:①Cl2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl ⑧CaCl2
-
(1) 属于离子化合物的是;
-
(2) 属于共价化合物的是;
-
(3) 含有离子键的物质是;
-
(4) 既含有共价键又含有离子键的物质是.(用序号填空)
CO2 分子中σ键与π键数目比为( )
A . 2:1
B . 1:2
C . 1:1
D . 1:3
下列物质中,既含有离子键又含有非极性共价键的是( )
A . HClO
B . Ba(OH)2
C . Na2O2
D . Ar
下列说法正确的是( )
A . N2、O2和Cl2分子中既含有σ键,又含有π键
B . PCl3分子中,中心原子采取sp3杂化方式
C . CS2、H2O、C2H2都是直线型分子
D . CH4、C6H6都是只含有极性键的非极性分子
下列各组物质中,所含化学键类型完全相同的是( )
A . HCl和MgCl2
B . H2O和CO2
C . NH4Cl和CCl4
D . HCl和NaOH
下列叙述中正确选项的个数是( )
①离子化合物一定含离子键,也可能含极性键或非极性键
②若晶体中有阳离子,则一定也含有阴离子
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
⑥熔融状态能导电的物质一定是离子化合物
⑦冰熔化时水分子中共价键发生断裂
A . 2个
B . 3个
C . 4个
D . 5个
下列说法中正确的是 



A .  、
、  、
、  中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
 、
、  、
、  中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
中,所有原子都满足最外层8电子的稳定结构
B . 在元素周期表中金属和非金属交界处可以找到半导体材料
C . 由非金属元素组成的化合物一定是共价化合物
D . 第ⅠA族元素和第ⅦA族元素的原子之间都能形成离子键
已知A原子只有一个未成对电子,M电子层比N电子层多11个电子,试回答下列问题:
-
(1) 该元素的基态原子有个能层充有电子;
-
(2) 写出A原子的电子排布式和元素符号;。
-
(3) 指出元素A在周期表中的位置。
-
(4) 指出元素A的最高化合价 。
-
(5) A的氢化物分子中共价键的类型可能有。
① s-pσ键 ② p-pσ键 ③ s-s σ键 ④ p-pπ键
-
(6) 写出与A同周期未成对电子数最多的元素原子的价层电子排布式。
下列说法中正确的是( )
A . 2px2表示2px能级有两个轨道
B . 在CS2分子中α键与π键的数目之比是2:1
C . 电子仅在激发态跃进到基态时才会产生原子光谱
D . 表示一个某原子在第三电子层上有10个电子可以写3s23p63d2
下列属于强电解质的共价化合物是( )
A . H2SO4
B . NaCl
C . CH3COOH
D . Mg3N2
下列关于非金属元素和金属元素特征的叙述不正确的是( )
①非金属元素可能有还原性,也可能有氧化性;②非金属元素只能形成共价化合物;③金属阳离子被还原不一定得到金属单质;④金属元素不可能存在于阴离子中;
⑤金属元素与非金属元素形成的化合物一定是离子化合物
A . ①③
B . ②③
C . ③④⑤
D . ②④⑤
下面两表分别列出了CO和N2 的某些性质及相关键能,有关说法错误的是( )
表一
| 分子 | 熔点/℃ | 沸点/℃ | 常温时在水中溶解度 |
| CO | -205.05 | -191.49 | 2.3mL |
| N2 | -210.00 | -195.81 | 1.6mL |
表二
| CO | C-O | C=O | |
| 键能(kJ /mol) | 357.7 | 798.9 | 1071.9 |
| N2 | N-N | N=N | |
| 键能(kJ /mol) | 193 | 418 | 946 |
A . CO与N2的价电子总数相等
B . 由表2可知,CO的活泼性不及N2
C . 由表1可知,CO的熔沸点高于N2 , 是因为CO分子间作用力大于N2
D . 由表2可知,σ键的稳定性不一定强于π键
下列物质属于共价化合物的是( )
A . NH4Cl
B . CO2
C . N2
D . NaCl
盐酸肼(N2H6Cl2)是一种化工原料,与NH4Cl类似,其溶液呈酸性。下列说法正确的是( )
A . N2H6Cl2属于共价化合物
B . N2H6Cl2中含有非极性共价键
C . N2H6Cl2中氮元素化合价为﹣3价
D . 盐酸肼在水中电离方程式为N2H6Cl2 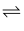
 +2Cl﹣
+2Cl﹣
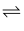
 +2Cl﹣
+2Cl﹣
下列含有非极性键的化合物是( )
A .  B .
B .  C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
下列叙述中正确的是 ( )
A . 含离子键的化合物一定是离子化合物
B . 含共价键的化合物一定是共价化合物
C . 全部由非金属元素形成的化合物一定是共价化合物
D . 在离子化合物中也可能含有金属键
下列说法不正确的是( )
A . HCl属于共价化合物,溶于水能电离出H+和Cl-
B . NaOH是离子化合物,该物质中只含有离子键
C . HI气体受热分解的过程中,破坏了极性共价键
D . Mg2+和S2-的最外电子层都形成了8个电子的稳定结构
已知短周期元素M、N、P、Q最高价氧化物对应水化物分别为X、Y、Z、W,M是短周期中原子半径最大的元素,常温下X、Z、W均可与Y反应,M、P、Q的原子序数及0.1mol/LX、Z、W溶液的pH如图所示。下列说法正确的是( )
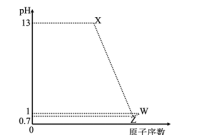
A . N原子的电子层数与最外层电子数相等
B . M的离子半径小于N的离子半径
C . P氢化物稳定性大于Q氢化物稳定性
D . X、W两物质含有的化学键类型相同
我国科学家成功合成了世界上首个五氮阴离子盐 (用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。从结构角度分析,R中两种阳离子不同之处为( )
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。从结构角度分析,R中两种阳离子不同之处为( )
 (用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。从结构角度分析,R中两种阳离子不同之处为( )
(用R代表),经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。从结构角度分析,R中两种阳离子不同之处为( )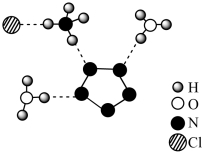
A . 电子总数
B . 中心原子的价层电子对数
C . 空间结构
D . 共价键类型
最近更新
- The discovery of new evidence led to __________. A. the thi
- 如下图所示,重球m用一条不可伸长的轻质细线拴住后悬于O点,重球置于一个斜面不光滑的斜劈M上,用水平力F向左推动斜劈M在光
- “龟兔赛跑”的故事可为家喻户晓,也是一个富有哲理的寓言故事,如图所示为“龟兔赛跑”中的乌龟和兔子在时间t0内的位移-时间
- 唐朝诗人皮日休曾说:“大运河北通诼郡之渔商,南运江都之转输,其为利也博哉。”由此可看出隋朝开凿大运河的意义是:(
- 在一个不透明的布袋中装有个白球,个黄球,它们除颜色不同外,其余均相同.若从中随机摸出一个球,它是黄球的概率是,则=
- 下列成语或古诗与图的哲学寓意相一致的是 A.当局者迷,旁观者清 B.种瓜得瓜,种豆得豆 C.蝉噪林逾静,鸟鸣山更幽 D.
- 下表是民国初年统计的国内若干个地区的农村消费情况统计数据,该数据反映出的主要结论是区域 情况 北部平均 安徽怀县 河北平
- 设为阿伏加德罗常数,下列说法中不正确的是( ) A.质子总数为5的重水()是0.5mol B.在标准状况下,11.2L甲
- 下列各组离子,能在指定溶液中共存的是①无色溶液中:K+、Cl-、Na+、HCO3-、OH-② 使pH试纸变深蓝色的4应中
- Under no circumstances, he was warned, _____ to give the pas
- “人间四月芳菲尽,山寺桃花始盛开。”造成这一差异的环境因素是() A.光 B.水
- Do I need to have any experience to take this course?
- 下列离子方程式书写正确的是A.少量烧碱滴入Ca(HCO3)2溶液中:Ca2+++OH-===CaCO3↓+H2OB.少量
- 下列有关氧气的叙述正确的是( ) A.铁丝燃烧,发出耀眼白光,生成黑色固体 B.氧气化学性质比较活泼,具有可燃性
- (28分)阅读材料,结合所学知识回答问题。 材料一 十六世纪前后西欧国家认为:谁控制了世界的海洋,谁就控制了世界贸易;
- (2019·广东清远期末)如图为某种单基因遗传病的遗传系谱图,其中Ⅱ3、Ⅱ7均携带致病基因。下列相关判断正确的是()A.
- 做唾液淀粉酶催化淀粉实验时,用口含一小口清水,然后将含过的清水加入淀粉溶液中,也会使淀粉消化,和用纯唾液的效果一样,这一
- 3的负倒数是A.B.—C.3D.—3
- 用NA表示阿伏加德罗常数的值。下列叙述中正确的是A.6g SiO2所含分子数为0.1NA,化学键总数为0.4NA B.将
- Chinese _________ in many countries today.Maybe you will tea