微粒半径大小的比较 知识点题库
下列各项内容,排列顺序正确是( )
①固体的热稳定性:Na2CO3>CaCO3>NaHCO3
②常见离子的还原性排序:S2﹣>I﹣>Fe2+
③微粒半径:K+>S2﹣>F﹣
④给出质子的能力:CH3COOH>C2H3OH>H2O
⑤氢化物的沸点:H2Se>H2S>H2O.
A . ①③
B . ②④
C . ①②
D . ③⑤
a、b、c、d为原子序数依次增大的短周期不同主族元素,其中只有一种为金属元素,四种元素的单质在通常情况下只有一种不是气体,b与d的最外层电子数之和为a与c最外层电子数之和的四倍。下列叙述错误的是( )
A . 原子半径:c>d>a
B . d的氧化物对应的水化物酸性均比b的强
C . a、b、d三种元素形成的化合物可能既含离子键又含共价键
D . 单质的熔点:c>b>a
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A . L2+与R2-的核外电子数相等
B . M与T形成的化合物既能与强酸反应又能与强碱反应
C . 氢化物的稳定性为H2T<H2R
D . 单质与浓度相等的稀盐酸反应的速率为Q>L
短周期主族元素X、Y、Z的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z的核电荷数比Y多4。下列说法正确的是( )
A . 原子半径的大小顺序:Z>Y>X
B . Y分别与Z、X形成的化合物中化学键类型相同
C . 单质Z能在X的最高价氧化物中燃烧
D . Y、X的简单气态氢化物的热稳定性:Y<X
短周期主族元素X、Y、Z、W的原子序数依次增大,其中Y、W处于同一主族,Y、Z的原子最外层电子数之和等于9,X的简单氢化物与W的单质组成的混合气体见光可生成W的氢化物和油状混合物。下列说法正确的是( )
A . 简单离子半径:Y<Z<W
B . Y的简单气态氢化物的热稳定性一定比W的强
C . W的氧化物对应的水化物的酸性一定比X的强
D . Y分别与X、Z形成的化合物,其所含化学键的类型相同
短周期主族元素X、Y、Z、W原子序数依次增大。 X的族序数是周期数的3倍,25 ℃时,0.1 mol·L-1Z的最高价氧化物对应的水化物溶液的pH为13,W的最外层有6个电子。下列说法正确的是( )
A . X的简单气态氢化物的热稳定性比W的弱
B . 原子半径:r(Z)>r(W)>r(X)>r(Y)
C . 元素Y、W的简单阴离子具有相同的电子层结构
D . Z分别与X、Y、W形成的化合物中均一定只含离子键
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构,则下列关于X、Y、Z、W四种元素的描述中,正确的是( )
A . 原子序数:Y>X>Z>W
B . 原子最外层电子数:Y>X>Z>W
C . 原子半径:X>Y>Z>W
D . 金属性:X<Y,还原性:W2->Z-
在通常条件下,下列各组物质的性质排列不正确的是( )
A . 还原性强弱:Cl-<Br-<I-
B . 酸性:CH3COOH>H2CO3>H2SiO3
C . 热稳定性:HF>H2O>NH3
D . 微粒半径大小:S>Na+>O2-
Q、X、Y和Z为短周期元素,它们在周期表中的位置如图所示,这4种元素的原子最外层电子数之和为22。下列说法正确的是( )
![]()
A . Y的原子半径比X的大
B . Q的最高价氧化物的水化物的酸性比Z的强
C . X、Y和氢3种元素形成的化合物中都只有共价键
D . Q的单质具有半导体的性质,Q与Z可形成化合物QZ4
下列微粒的半径比值大于1的是 ( )
A . Mg2+/Mg
B . K+/S2-
C . N/P
D . Cl-/Cl
图中是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
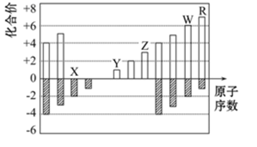
A . 原子半径:Z>Y>X
B . 气态氢化物稳定性:R<W
C . WX3和水反应生成的化合物是离子化合物
D . Y和Z两者最高价氧化物对应的水化物能相互反应
新型储氢材料是开发利用氢能的重要研究方向。
-
(1) 元素N 的价层电子排布式为3d2 4s2 ,其氯化物 NCl4 和LiBH4 反应可制得储氢材料N(BH4)3 。元素 N 在周期表中的位置为,该原子具有种不同运动状态的电子。 B 原子的轨道表示式为。
-
(2) 金属氢化物是具有良好发展前景的储氢材料。
① LiH 中,离子半径: Li+ (填“>”“=”或“<”) H- 。
②某储氢材料是短周期金属元素M 的氢化物。 M 的部分电离能(单位: kJ· mol-1 )如下表所示:
I1
I2
I3
I4
I5
738
1451
7733
10540
13630
M 的最高正价是价。
-
(3) AlF3 具有较高的熔点(1040℃),属于(填晶体类型)晶体;AlCl3 在 178℃时升华,写出 AlF3 、AlCl3晶体类型不同的原因(从原子结构与元素性质的角度作答)。
随原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如图所示。下列关于说法中错误的是( )
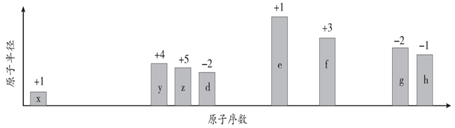
A . f在元素周期表的位置是第3周期ⅢA族。
B . d、e常见离子的半径大小:r(O2-)>r(Na+)
C . g、h的最高价氧化物对应的水化物的酸性强弱是:HClO4>H2SO4
D . x2d2的结构式: 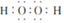
X、Y、Z、M、Q为五种短周期主族元素,原子序数依次增大。X是形成化合物种类最多的元素,Y元素最外层电子数是次外层电子数的3倍,Z是同周期中原子半径最大的元素,Q的最高正价与最低负价代数和为4,X、M同主族,M和Q同周期。下列说法错误的是( )
A . 最高价氧化物对应水化物的酸性:M<X<Q
B . 原子半径:Y<Q<Z
C . 最简单氢化物的稳定性:M<Y<Q
D . XY2与MY2中的化学键类型相同
短周期元素X。Y、Z、Q、W在元素周期表中的位置如表所示,其中Q的最低价氢化物摩尔质量为34g/mol,X的最低价氢化物不是电解质,则下列说法中正确的是( )
X | Y | |||
Z | Q | W |
A . 原子半径:X>Y>Z
B . Z是自然界中含量最多的元素
C . 氧化物对应水化物的酸性X<W
D . 最低价氢化物的稳定性:Q<Y
由同周期元素原子W、X、Y、Z构成的一种阴离子(如图),Y的最外层电子数等于X的核外电子总数,四种原子最外层电子数之和为20。下列说法正确的是( )
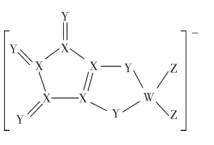
A . W、X、Y、Z第一电离能由大到小依次是:Z>Y>X>W
B . Y形成的简单离子的半径比Z形成的简单离子的半径小
C . W和X的最高价氧化物对应水化物的酸性:W>X
D . W、Z形成的化合物分子中各原子均满足8电子稳定结构
一种工业洗涤剂中间体的结构如图,其中X、Y、Z、Q、W原子序数依次增大且分属三个短周期。Y、Q元素的基态原子中均有两个未成对电子,下列说法正确的是( )
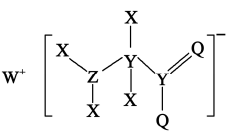
A . 电负性大小:Q>Z>Y>X
B . 简单离子半径:Q<Z<W
C . 简单氢化物的沸点:Y>Z>Q
D . 阴离子中各原子都满足8电子稳定结构
一种新型漂白剂(如图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是( )
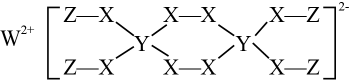
A . W单质在空气中点燃发出耀眼的白光
B . W、X对应的简单离子半径W>X
C . Y的单质高温下可与水反应放出氢气,体现Y的氧化性
D . 该漂白剂的漂白原理与 相同
相同
 相同
相同
四种短周期元素X、Y、Z和W在周期表中的位置如图所示。下列说法错误的是( )
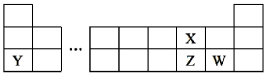
A . 原子半径(r):r(Y)>r(Z)>r(W)
B . W的氧化物的水化物一定是强酸
C . Y和W的最高化合价之和为8
D . 简单氢化物的热稳定性:X>Z
W、X、Y、Z 为原子序数依次增大的短周期元素,四种元素的核外电子总数满足X+Y=W+Z;化合物 XW3与WZ相遇会产生白烟。下列叙述正确的是( )
A . X的气态氢化物属于碱
B . Y的氧化物属于离子化合物
C . 原子半径:Z>Y>X>W
D . 非金属性:W> X>Y> Z
最近更新
- 阅读下面一首宋诗,然后回答问题。 夜半闻横管 南宋程俱 秋风夜搅浮云起,幽梦归来度寒水。 一声横笛静穿云,响振疏林叶空委
- For most Chinese young peoplein recent years, a house is wi
- When the oldman was alive, he ______ sit for hours at the d
- 下面是实验高中的四位同学的实验操作方法或结果,其中错误的一项是 A、甲基绿和毗罗红混合染色可以显示DNA和RNA在细
- 在一定条件下,1体积气体A2和3体积B2完全反应生成了2体积气体X(体积在相同条件下测定),则X的化学式是 A.AB
- 假定英语课上老师要求同桌之间交换修改作文,请你修改你同桌写的以下作文。文中共有10处语言错误,每句中最多有两处。错误
- 上课时,你听见老师的讲课声是由 传到耳朵中的,把手表压在枕头底下,晚上睡觉时能清晰地听见手表的嘀嗒声,
- 下列物质的鉴别方法不正确的是() A.用焰色反应鉴别NaCl、KCl和Na2SO4 B.用氢氧化钠溶液鉴别MgCl2溶液
- 但愿人长久, 。(苏轼《水调歌头》)
- A、B、C、D、E、F和G都是有机化合物,它们的关系如下图所示:(1)化合物C的分子式是C7H8O,C遇FeCl3溶液显
- 下列说法正确的是 A.凡能发生银镜反应的有机物一定是醛 B.在氧气中燃烧时只生成CO2和H2O的物质一定是烃 C.苯
- 生活中常要对一些物理量进行估测,以下估测最接近实际值的是A.小明的鞋长为58cmB.人从一楼步行到三楼的时间约16sC.
- 京津城际列车的开通是打破行政区划限制、合作共赢的典型案例,它将极大地拉近京津两地经济空间,使两地资源互补成为可能。这说明
- 为庆祝第14个世界读书日(4月23日),某英文报社对读者进行了调查活动。请根据以下提示,写一篇120词左右的英语短文,将
- You are fatter than _______. A. he B. his C. him D. he is t
- How much doesit cost to build the school library? Four
- 如图,将直角三角形ABO放入平面直角坐标系xoy中,直角顶点O与原点重合,点,为两动点,Rt⊿ABO能够绕点O 旋转,其
- 函数y=﹣x的图象与函数y=x+1的图象的交点在 A.第一象限 B.第二象限 C.第三象限
- 补写出下列名句名篇中的空缺部分。(任意选两小题)(4分) (1)请写出李白《梦游天姥吟留别》中表现诗作主旨的一句。
- 已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:(1)CuSO4 +Na2CO3 主要:Cu2+



