氮的固定 知识点题库
下列反应属于人工固氮的是( )
A . 分离液态空气制氮气
B . NO和O2生成NO2
C . 空气在雷电作用下所产生NO
D . 工业合成氨
下列过程中不属于氮的固定的是( )
A . 工业合成氨
B . 雷雨天,空气中的氮气转化为能被植物吸收的硝酸盐
C . 用氨气与硝酸制成“硝铵”化肥
D . 豆科作物的根瘤菌将空气中的氮转化为氨
不属于氮的固定的变化是( )
A . 氨催化氧化制硝酸
B . 由氮气和氢气合成氨气
C . 镁条在氮气中燃烧
D . 豆科植物的根瘤固氮
下列过程属于人工固氮的是( )
A . 合成氨
B . 闪电时N2转化为NO
C . 分离液态空气制氮气
D . 豆科作物根瘤菌将N2转化为NH3
下列变化不属于氮的固定的是( )
A . 工业合成氨
B . 雷雨闪电时,大气中产生了一氧化氮
C . 豆科作物的根瘤菌将空气中的氮转化为氨
D . 在一定条件下由氨气和二氧化碳合成尿素
“雷雨肥庄稼“的方程式是 .
氮气是制备含氮化合物的一种重要物质,而氮的化合物用途广泛.
(1)下面是利用氮气的一种途径

①步骤I中主要利用N2与液态空气中其它成分的 (填性质)不同.
②步骤II在自然界大气中发生反应的化学方程式为 .
③最新研究发现在碱性溶液中通过电解反应2N2+6H2O 4NH3+3O2实现氮的固定,阴极上发生的电极反应式为 .
4NH3+3O2实现氮的固定,阴极上发生的电极反应式为 .
(2)氨气可以用于侯氏制碱法,其流程如图所示:
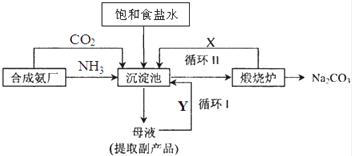
①循环Ⅰ、Ⅱ中循环利用的物质X是 ,Y是 .(填化学式)
②向沉淀池中通入气体时,需要先通入NH3 , 再通入CO2 , 其原因是 .
(3)尿素【CO(NH2)2】是氮的一种重要化合物,可用于除去酸性工业废水中的NO2﹣ , 生成的产物无污染,反应的离子方程式为 ;该反应生成6.72L(已折算为标准状况)混合气体时,消耗尿素的质量为 .
下列解释事实的方程式不正确的是( )
A . 铝热法炼铁:2Al+Fe2O3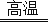 2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2
2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2 2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
 2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2
2Fe+Al2O3
B . 工业进行“氮的固定”:N2+3H2 2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
2NH3
C . 铅蓄电池充电时阴极反应:PbSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
D . 用铜和稀硝酸备硝酸铜:Cu+4H++2NO3﹣=Cu2++2NO2↑+2H2
下列过程不属于氮的固定的是( )
A . 工业合成氨
B . 工业上用氨催化氧化法制备硝酸
C . 闪电导致雷雨中含有硝酸
D . 豆科植物的根瘤菌制造含氮化合物
氮的固定是指( )
A . 植物从土壤中吸收氮肥
B . 大豆的根瘤菌将含氮的化合物转变为植物蛋白质
C . 将空气中的氮气转变为氮的化合物
D . 硝酸和氨气反应生成氮肥
将空气中氮气转化成氮的化合物的过程称为固氮.下列选项中能实现人工固氮的是( )
A . 闪电
B . 电解饱和食盐水车间
C . 根瘤菌
D . 合成氨车间
属于工业固氮的是( )
A . N2与O2反应生成NO
B . 由NH3转变成 NH4HCO3
C . N2与H2在一定条件下反应生成NH3
D . 豆科植物的根瘤吸收氮
下列关于自然界中氮循环(如图)的说法错误的是( )
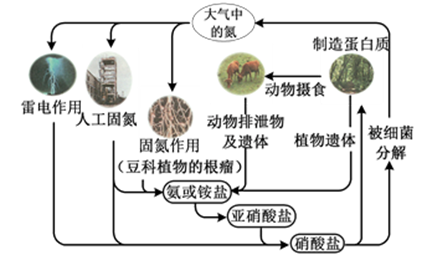
A . 雷电作用是氮元素被氧化
B . 豆科植物的根瘤固氮属于人工固氮
C . 含氮无机物和含氮有机物可相互转化
D . 碳、氢、氧三种元素也参与了氮循环
下列关于自然界中氮循环(如图)的说法不正确的是:( )
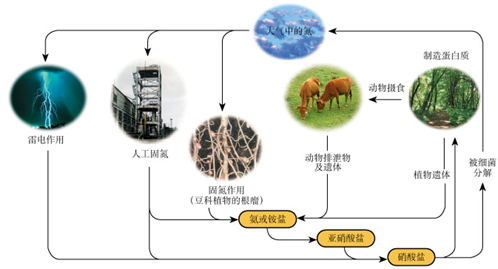
A . 氮元素均被氧化
B . 工业合成氨属于人工固氮
C . 含氮无机物和含氮有机物可相互转化
D . 碳、氢、氧三种元素也参与了氮循环
下列说法不正确的是( )
A . 工业合成氨是一种人工固氮方法
B . 侯氏制碱法应用了物质溶解度的差异
C . 播撒碘化银可实现人工降雨
D . 铁是人类最早使用的金属材料
合成氨是目前最有效工业固氮的方法,解决数亿人口生存问题。回答下列问题:
-
(1) 科学家研究利用铁触媒催化合成氨的反应历程如图所示,其中吸附在催化剂表面的物种用“ad”表示。
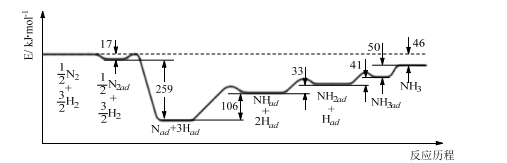
由图可知合成氨反应
 N2(g)+
N2(g)+ 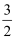 H2(g)
H2(g)  NH3(g)的∆H= kJ·mol-1。该历程中反应速率最慢的步骤的化学方程式为。
NH3(g)的∆H= kJ·mol-1。该历程中反应速率最慢的步骤的化学方程式为。 -
(2) 工业合成氨反应为:N2(g)+3H2(g)
 2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示:
2NH3(g),当进料体积比V(N2):V(H2)=1:3时平衡气体中NH3的物质的量分数随温度和压强变化的关系如图所示: 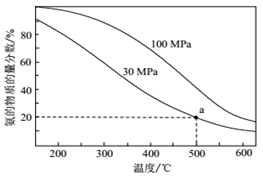
①500℃时,反应平衡常数Kp(30MPa) Kp(100MPa)。(填“<”、“=”、“>”)
②500℃、30MPa时,氢气的平衡转化率为(保留2位有效数字),Kp=(MPa)-2(列出计算式)。
-
(3) 科学家利用电解法在常温常压下实现合成氨,工作时阴极区的微观示意如图,其中电解液为溶解有三氟甲磺酸锂和乙醇的惰性有机溶剂。
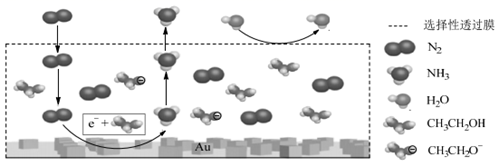
①阴极区生成NH3的电极方程式为。
②下列说法正确的是(填标号)。
A.三氟甲磺酸锂的作用是增强导电性
B.该装置用金(Au)作催化剂目的是降低N2的键能
C.选择性透过膜可允许N2和NH3通过,防止H2O进入装置
下列不属于固氮的是( )
A . 合成氨反应
B . 氮气与氧气在雷电作用下化合
C . 根瘤菌将氮气转化为氨基酸
D . 氨气制造铵态氮肥
下列过程不属于氮的固定的是( )
A . 雷电时生成氮的氧化物
B . 工业上用氢气与氮气合成氨
C . 植物的根从土壤中吸收铵根离子和硝酸盐
D . 豆科植物的根瘤把空气中的氮气转化为硝酸盐
下面能实现人工固氮的是( )
A | B | C | D |
|
|
|
|
闪电 | 电解饱和食盐水车间 | 根瘤 | 合成氨车间 |
A . A
B . B
C . C
D . D
下列反应中,不属于氮的固定的是( )
A . 由 制碳酸氢铵和尿素
B .
制碳酸氢铵和尿素
B .  和
和 在一定条件下合成
在一定条件下合成 C . 雷电时,空气中的
C . 雷电时,空气中的 与
与 反应生成
反应生成 D . 豆科植物把空气中的氮气转化为化合态的氮
D . 豆科植物把空气中的氮气转化为化合态的氮
 制碳酸氢铵和尿素
B .
制碳酸氢铵和尿素
B .  和
和 在一定条件下合成
在一定条件下合成 C . 雷电时,空气中的
C . 雷电时,空气中的 与
与 反应生成
反应生成 D . 豆科植物把空气中的氮气转化为化合态的氮
D . 豆科植物把空气中的氮气转化为化合态的氮
最近更新
- 在全球变暖的大背景下,低碳经济受到越来越多国家的关注。下图是生态系统碳循环的部分过程,其中甲、乙、丙表示生态系统中的三种
- NA代表阿伏加德罗常数,下列叙述正确的是A.1 mol Cl2在反应中得到电子数不一定为2NA B.1 mol O2在反
- 已知,则的大小关系为 A. B. C. D.
- 1978年安徽小岗村18家农户决定分田到户,揭开了中国农村家庭联产承包责任制的序幕。在经济体制改革的进程中,小岗村不断探
- Miss Zhang ________ her lesson with apoem ________ of last t
- 化学与生活密切相关。 (1)识别织物成分常用灼烧法。若灼烧时,闻到了 ,则该织物中含有羊毛。 (2)“钙强化营
- 仿照示例,任选两种物质,分别写出它们的一个性质和与之对应的用途:物质 性 质 用 途 例:氢气 可
- 如图所示的异形导线框,匀速穿过一匀强磁场区,导线框中的感应电流i随时间t变化的图象是(设导线框中电流沿abcdef为正方
- ﹣How was your trip in the mountains last weekend? ﹣Fantastic
- 若,则( )A.<< B. << C. <<
- 也是诗词大家。他在复《诗刊》主编臧克家的信中写道:“诗当然应以新诗为主体,旧诗可以写一些,但是不宜在青年中提倡,因为这
- 某种群中AA、Aa、aa的基因型频率如图,图中阴影部分表示繁殖成活率低的个体。则该种群经选择之后,下一代中三种基因型频率
- 下列所提到的历史现象或事件中,李贽应该会持反对意见的是 : A.花木兰替父从军 B.梁祝化蝶相随 C.商鞅变法
- 读森林与环境示意图,回答下列问题。(1)该图所示森林的环境效益有 、 、 、 。 (2)此
- 20世纪50年代中期,民族资本家荣毅仁说:“对于我,失去的是我个人的一些剥削所得……得到的却是一个人人富裕、繁荣强盛的社
- 如图所示是初中化学中的一些重要实验,请回答下列问题:实验一 实验二 实验三 (1
- 假定生产一件甲商品的社会必要劳动时间为2小时,价值为40元。如果生产者A生产该商品的个别劳动时间为1小时,那么,A在4小
- 保护生物多样性最为有效的措施是
- There is song in English that goes like this: “Sign,sign,
- 如图,在 中, ,点 D 是 AB 延长线上一点,过点 D 作 .若 ,则 的度数为( ) A . 25°B . 35°







