二氧化硫的性质 知识点题库
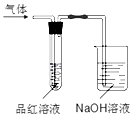
请回答下列问题:
-
(1) 若装置中通入一段时间的SO2 , 观察到试管中的品红溶液,然后再加热试管,溶液又呈现红色;
-
(2) 若装置中通入一段时间的氯气,观察到试管中的品红也褪色,生成的具有漂白性的物质是( 填化学式),然后再加热试管,溶液;
-
(3) 由以上两个实验可以说明SO2和Cl2的漂白原理 (填“相同”或“不相同”);
-
(4) 实验中NaOH溶液的作用是.
-
(1) 电解饱和食盐水:.
-
(2) 氢氧化钠溶液腐蚀磨砂玻璃塞:.
-
(3) 实验室用亚硫酸钠与浓硫酸反应制备二化硫:.
-
(4) 氢氧化铝溶于氢氧化钠溶液:.
-
(5) 氨在催化剂的作用下与氧气发生反应,生成一氧化氮.
|
选项 |
实验及现象 |
结论 |
|
A |
用玻璃棒蘸取某样品进行焰色反应时观察到黄色火焰 |
该样品含钠元素 |
|
B |
向NaHCO3溶液中加入过量盐酸振荡、静置、有气泡产生 |
证明非金属性:Cl>C |
|
C |
向酸化的KMnO4溶液通入SO2,向反应后的溶液中加入BaCl2产生白色沉淀 |
证明SO2被氧化为SO42- |
|
D |
将10mL 2mol/L的KI溶液与1 mL 1mol/LFeCl3溶液混合充分反应后滴加KSCN,溶液颜色变红 |
KI与FeCl3反应有可逆性 |
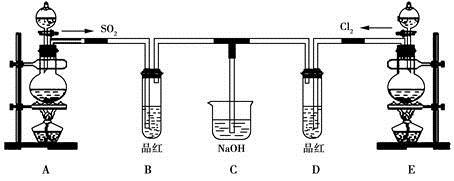
-
(1) 实验室用装置A制备SO2。某同学在实验时发现打开A的分液漏斗活塞后,漏斗中液体未流下,你认为原因可能是:;
-
(2) 实验室用装置E制备Cl2 , 其反应的化学化学方程式为:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O;若有6 mol的HCl参加反应,则转移的电子总数为;
MnCl2+Cl2↑+2H2O;若有6 mol的HCl参加反应,则转移的电子总数为;
-
(3) ①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:,D:。
②停止通气后,再给B、D两个试管分别加热,两个试管中的现象分别为B:,D:。
-
(4) 另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强。他们将制得的SO2和Cl2按1∶1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样。请你分析该现象的原因(用化学方程式表示)。
| 操作和现象 | 结论 | |
| A | 向NaCl溶液中先滴加少量AgNO3溶液,后滴加少量NaI溶液,先有白色沉淀,后变成黄色沉淀 | 说明Ksp(AgI)<Ksp (AgCl) |
| B | 将SO2通入酸性KMnO4溶液中,紫色褪去 | 说明SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 说明氧化性:Cu2+>Fe3+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
①用天然气代替煤炭做民用燃料 ②提高热能利用率 ③硫酸厂采用更好的催化剂使SO2氧化成SO3④使用CS2萃取煤炭中的硫 ⑤燃煤中加入石灰后再使用
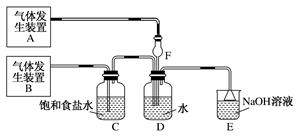
-
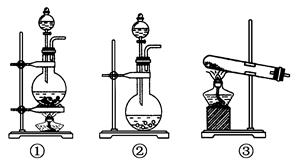
(1) 该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2 , 采用MnO2和浓盐酸(12 mol·L-1)为原料制取Cl2。在此实验中,F仪器的作用是;发生装置B应选择以下三种装置中的(填序号)。
-
(2) D装置中主要反应的离子方程式为。
-
(3) 为验证通入D装置中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
①氯化铁溶液②氯化亚铁溶液 ③硫氰化钾溶液④酸性高锰酸钾溶液若Cl2过量,取适量D中溶液滴加至盛有 (选填一个序号)试剂的试管内,再加入(选填一个序号)试剂。发生的现象是。若SO2过量,取适量D中溶液滴加至盛有(选填一个序 号)试剂的试管内,发生的现象是。
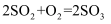 B . 此工艺的优点之一是物质能循环利用
C . 由以上流程可推知氧化性:
B . 此工艺的优点之一是物质能循环利用
C . 由以上流程可推知氧化性:  D . 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
D . 可用酸性高锰酸钾溶液检验溶液C中是否含有Fe3+
 分别通入下列四种溶液,根据实验现象所得结论正确的是( )
分别通入下列四种溶液,根据实验现象所得结论正确的是( )
|
选项 |
溶液 |
现象 |
结论 |
|
A |
溴水 |
溴水褪色 |
|
|
B |
|
出现淡黄色浑浊 |
|
|
C |
|
无明显变化 |
|
|
D |
|
无明显变化 |
|
溶液 | 现象 | 结论 | |
A | 含HCl、BaCl2的FeCl3溶液 | 产生白色沉淀 | SO2有还原性 |
B | H2S溶液 | 产生黄色沉淀 | SO2有氧化性 |
C | 酸性KMnO4溶液 | 紫色溶液褪色 | SO2有漂白性 |
D | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
-
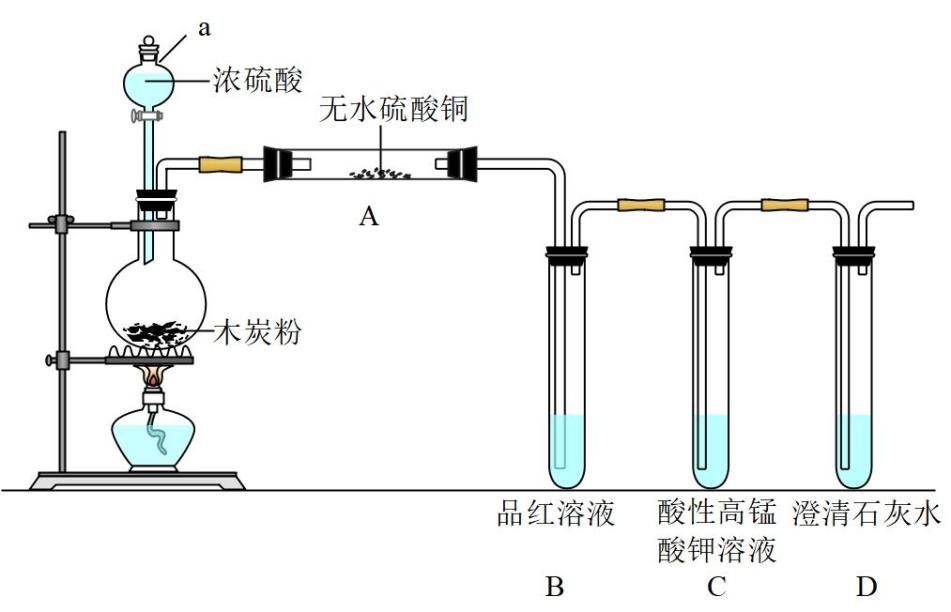
(1) 写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式。
-
(2) 仪器a的名称是。
-
(3) 装置A中出现现象,证明气体产物中有
 。
。
-
(4) C装置作用是。
- 加热氯酸钾与二氧化锰的混合物15.5 g,待反应完全后,冷却,称量得到10 g固体剩余物质,则制得的氧气为_______
- 下列说法不正确的是( )A.空间中,一组对边平行且相等的四边形是一定是平行四边形;B.同一平面的两条垂线一定共面
- 实验中可能会出现一些异常现象,下列对异常现象的分析不合理的是 A. 细铁丝在氧气中燃烧时集气瓶底炸裂———集气瓶底部未放
- 李同学是长沙市某校高二学生,在暑期学校组织的综合实践活动中,他积极响应学校的号召,准备以“参与基层民主管理”为目的参加实
- 2010年3月28日,吉利汽车以18亿美元成功收购福特旗下沃尔沃轿车100%的股权。这项交易对于飞速增长的中国汽车行业具
- 对于以下四幅图的描述中说法正确的是: 甲 乙 丙
- 下列过程中,需要吸收能量的是()A. H+H=H2 B. H+Cl=HCl C. I2→I+I D. S+O2=SO2
- 按要求把下面的句子扩写成一段话。 这个冬季,天气异常寒冷。 要求:①正面描写与侧面描写相结合。②至少运用两种不同
- 如图所示的电路中,电源电压保持不变,R为定值电阻,当开关闭合时,标有“6V 3W”的小灯泡L恰好正常发光;若保持R不变
- I seldom focus on classes, ______assigneda seat by the teac
- 2011年3月16日,《中华人民共和国国民经济和社会发展第十二个五年规划纲要》正式公布。“十二五”规划强调实现“两个同步
- 《西游记》中唐僧取经的故事家喻户晓,你知道唐僧的原型是谁吗?( )a.僧一行 b.鉴真
- --Whatdid he say in_______ of his stupid behavior? --He admi
- 已知则 ▲ .
- 甲乙两人下棋,甲获胜的概率为40%,甲不输的概率为90%,则甲乙下成和棋的概率为() A.60%
- 江苏省栟茶高级中学2010届高三高考模拟测试1(历史).doc 孙中山指出:“此一省欲起事,彼一省亦欲起事,不相联络,
- 阅读下面的文字,完成下题。 徐乾清:清水徐徐洒乾坤 2010年1月9日上午11点15分,我国著名水利专家、中国工程院院士
- 已知函数,则 的值是 .
- .理论是马克思主义与中国革命和建设实践相结合的理论成果,该成果( ) A.是中国第三代领导集体智慧的结晶B.丰
- 根据下面材料,按要求回答问题。(6分) 某县教育局丁局长在欢迎著名的语文特级教师x x x的大会上致辞说:“x老师是现代
 溶液
溶液 溶液
溶液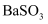 能溶于水
能溶于水 溶液
溶液


