硅和二氧化硅 知识点题库
下列说法正确的是( )
A . SiO2能和水发生化合反应生成硅酸
B . SiO2是酸性氧化物,它不溶于任何酸
C . SiO2的俗名叫水玻璃,不溶于水
D . SiO2又叫水晶,能溶于NaOH溶液中
近年来,有科学家提出硅是“21世纪的能源”、“未来的石油”的观点.假如硅作为一种普遍使用的新型能源被开发利用,其有利因素的下列说法中你认为不妥当的是( )
A . 硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料
B . 硅的来源丰富,易于开采,且可再生
C . 硅燃料放出的热量大,且燃料产物对环境污染较低,容易有效控制
D . 寻找高效催化剂,使二氧化硅分解产生硅的同时释放能量,是硅能源大规模开发利用的一项关键技术
下列有关物质用途或性质的叙述中正确的是( )
A . SiC俗称金刚砂,可用作砂纸、砂轮的磨料
B . 金属铝熔点高,所以我们可以用铝制器皿煮饭
C . 硅酸钠俗称水玻璃,可用作黏合剂和木材防火剂
D . 二氧化硫有毒,严禁将其添加到任何食品和饮料中
(14分)水泥是重要的建筑材料.水泥熟料的主要成分为CaO、SiO2 , 并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:
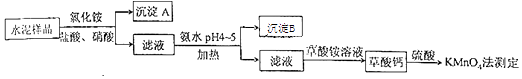
回答下列问题:
-
(1) 在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸.加入硝酸的目的是,还可使用代替硝酸.
-
(2) 沉淀A的主要成分是,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为.
-
(3) 加氨水过程中加热的目的是.沉淀B的主要成分为、(填化学式).
-
(4) 草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4﹣+H++H2C2O4→Mn2++CO2+H2O.实验中称取0.400g水泥样品,滴定时消耗了0.0500mol•L﹣1的KMnO4溶液36.00mL,则该水泥样品中钙的质量分数为.
下列说法中,正确的是( )
A . 硅元素在自然界里均以化合态存在
B . SiO2不能与水反应生成硅酸,不是酸性氧化物
C . 除去二氧化硅中少量的碳酸钙杂质应选用水
D . 粗硅制备时,发生的反应为C+SiO2=Si+CO2↑
光纤通信是一种现代化的通信手段,以光作为信息的载体,让光在光导纤维中传播,它可以提供大容量、高速度、高质量的通信服务.目前,我国正在大力建设高质量的宽带光纤通信网络,即信息高速光路.光纤通信所使用的光缆,其主要部件为光导纤维.下列说法正确的是( )
①制造光导纤维的主要原料是CaCO3
②制造光导纤维的主要原料是SiO2
③光导纤维传递光信号的基本物理原理是光的全反射
④光导纤维传递光信号的基本物理原理是光的折射.
A . ①④
B . ②③
C . ①③
D . ②④
给定条件下,下列选项中所示的物质间转化均不能一步实现的是( )
A . 粗硅 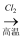 SiCl4
SiCl4  Si
B . Mg(OH)2
Si
B . Mg(OH)2  MgCl2
MgCl2  Mg
C . Na
Mg
C . Na  Na2O2
Na2O2  NaOH
D . AgNO3(aq)
NaOH
D . AgNO3(aq) 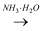 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq) 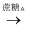 Ag
Ag
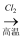 SiCl4
SiCl4  Si
B . Mg(OH)2
Si
B . Mg(OH)2  MgCl2
MgCl2  Mg
C . Na
Mg
C . Na  Na2O2
Na2O2  NaOH
D . AgNO3(aq)
NaOH
D . AgNO3(aq) 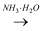 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq) 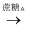 Ag
Ag
下列说法正确的是( )
①根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸和多元酸.
②混合物:铝热剂、福尔马林、水玻璃、漂白粉.
③根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素.
④SiO2既能与氢氟酸反应,也能与氢氧化钠溶液反应,但不属于两性氧化物.
⑤直径介于1~10nm之间的粒子称为胶体
⑥非金属元素的原子间只能形成共价键.
⑦H2O、Al2O3、HCl、NH3•H2O、Pb(CH3COO)2等均属电解质.
⑧族序数等于其周期序数的元素一定是金属元素.
A . ①③⑤
B . ②④⑦
C . ②⑤⑧
D . 全部正确
下列说法中正确的是( )
A . 大力实施矿物燃料“脱硫、脱硝”技术,可减少酸雨的发生
B . SiO2 具有较高的熔点,可用于制成耐高温的坩埚对氢氧化钠固体加热
C . 节日燃放的烟花,是钠、钾、锶、铂、铁等金属化合物焰色反应所呈现的色彩
D . CO、NO、NO2都是大气污染气体,在空气中都能稳定存在
在给定的条件下,下列选项所示的物质间转化均能实现的是( )
A . H2SiO3  SiO2
SiO2  SiCl4
B . 浓HCl
SiCl4
B . 浓HCl 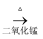 Cl2
Cl2 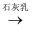 漂白粉
C . Fe
漂白粉
C . Fe 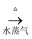 Fe2O3
Fe2O3  FeCl3
D . Mg(OH)2
FeCl3
D . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  无水MgCl2
无水MgCl2
 SiO2
SiO2  SiCl4
B . 浓HCl
SiCl4
B . 浓HCl 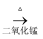 Cl2
Cl2 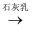 漂白粉
C . Fe
漂白粉
C . Fe 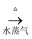 Fe2O3
Fe2O3  FeCl3
D . Mg(OH)2
FeCl3
D . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  无水MgCl2
无水MgCl2
下列关于硅单质及其化合物的说法错误的是( )
A . 水玻璃是一种矿物胶,既不易燃烧也不易腐蚀
B . 水泥、玻璃、石英都是硅酸盐制品
C . 氮化硅(Si3N4)是一种重要的结构陶瓷材料
D . 向Na2SiO3溶液中逐滴加入稀盐酸制备硅酸
置换反应的通式可表示为:单质甲+化合物A→单质乙+化合物B,请回答下列问题:
-
(1) 若甲为黄绿色气体,单质乙能使淀粉溶液变蓝色,则该反应的离子方程为。
-
(2) 若过量的单质甲 与化合物A发生反应的化学方程式为:
2Al+Fe2O3
 Al2O3+2Fe。除去反应后混合物中剩余的铝粉与生成的Al2O3所用的试剂是。
Al2O3+2Fe。除去反应后混合物中剩余的铝粉与生成的Al2O3所用的试剂是。 -
(3) 若甲为金属,其焰火为黄色,化合物B为一种常见的强碱,则该反应的化学方程式为 。
-
(4) 若单质乙是黑色非金属固体单质,化合物B是优质的耐高温材料,则该反应的化学方程式为 。
-
(5) 若化合物A可作光导纤维材料,乙为非金属半导体材料,则该反应的化学方程式为 。
能实现下列物质间直接转化的元素是( )
单质 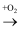 氧化物
氧化物  酸或碱
酸或碱  盐
盐
A . Si
B . Na
C . Al
D . Fe
硅的氧化物及硅酸盐构成了地壳中大部分的岩石、沙子和土壤。在无机非金属材料中,硅一直扮演着主角。下面几种物质中含有硅单质的是( )
| A | B | C | D |
| | | | |
| 玛瑙 | 光导纤维 | 太阳能电池板 | 水晶 |
A . A
B . B
C . C
D . D
化学与生产、生活、科技及社会发展等息息相关。下列说法中正确的是( )
A . 超市袋装食品中的硅胶,其作用是防止食物受潮、氧化变质
B . 绿色食品就是不使用化肥农药,不含任何化学物质的食品
C . “北斗”是我国自主设计研发的导航系统,其计算机芯片材料是高纯度的硅单质
D . 体积分数75%的酒精可用于消毒杀死新型冠状病毒,如果用95%的酒精则效果更好
化学与生活、科技密切相关。下列说法正确的是( )
A . “歼-20”飞机上使用的碳纤维被誉为“新材料之王”,是一种新型有机高分子材料
B . 2020年12月3日,在月球表面成功展开的五星红旗的主要材料芳纶属于合成纤维
C . 我国海洋开发走向深蓝,“蛟龙号”外壳材料使用的钛合金属于化合物
D . 2020年我国发射的嫦娥5号探月器的太阳能电池帆板的材料是 

化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是( )
A . NH3常用作制冷剂
B . 为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入硅胶
C . 小苏打用制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
D . 二氧化硅常用于制造光导纤维
硅及其化合物在现代信息技术、航天、医疗等领域有着广泛的应用。下列硅的单质或化合物中,广泛用作半导体材料的是( )
A . SiO2
B . Si
C . Na2SiO3
D . SiC
工业上可用焦炭与石英砂(主要成分是 )的混合物在高温条件下与氯气反应生成
)的混合物在高温条件下与氯气反应生成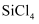 , 如图装置可用于实验室制备
, 如图装置可用于实验室制备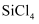 。已知
。已知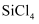 的沸点为55℃,且
的沸点为55℃,且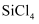 极易与水发生反应。
极易与水发生反应。
 )的混合物在高温条件下与氯气反应生成
)的混合物在高温条件下与氯气反应生成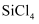 , 如图装置可用于实验室制备
, 如图装置可用于实验室制备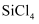 。已知
。已知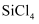 的沸点为55℃,且
的沸点为55℃,且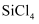 极易与水发生反应。
极易与水发生反应。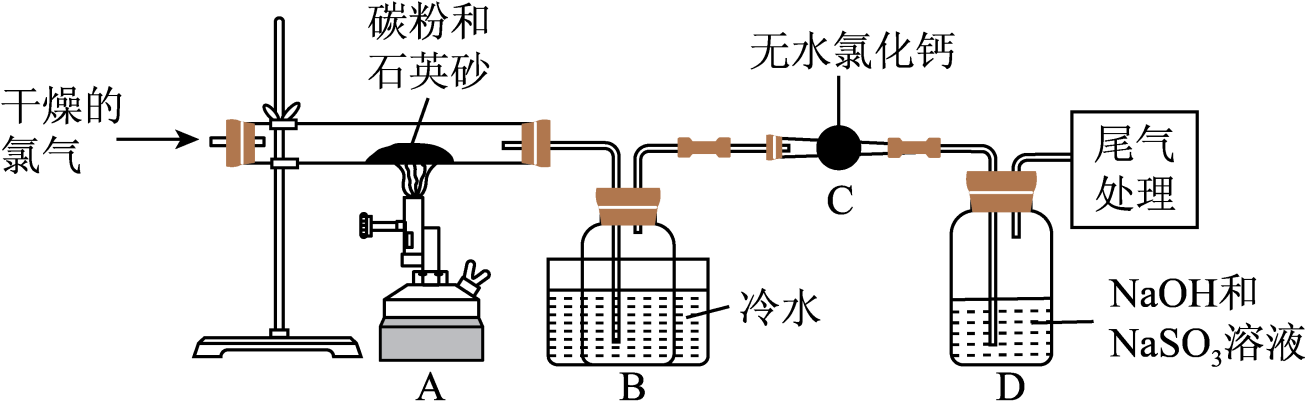
请回答:
-
(1) 请补充完整装置A中发生反应的化学方程式:①、②
 。
。
-
(2) 装置C的仪器名称是,装置C的作用是。
-
(3) 装置D中吸收气体一段时间后,吸收液中肯定含有
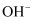 ,
,  ,
,  , 还可能含有其他阴离子。某化学兴趣小组设计实验以检验该吸收液中可能还存在的某些其他阴离子(忽略空气中
, 还可能含有其他阴离子。某化学兴趣小组设计实验以检验该吸收液中可能还存在的某些其他阴离子(忽略空气中 的影响)。
的影响)。【提出假设】假设1:有
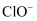 ;假设2:有
;假设2:有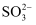 ;假设3:……
;假设3:……【设计方案】取少量吸收液于试管中,滴加稀硫酸至溶液略呈酸性,然后进行如下实验:
Ⅰ、向吸收液中滴加淀粉KI溶液,若溶液变为,可验证假设1成立。
Ⅱ、向吸收液中(简述实验操作和实验现象),可验证假设2成立。
下列物质应用正确的是( )
A . 纯碱用作治疗胃酸过多的药物
B . 氯气和消石灰用作生产漂白液的原料
C . 二氧化硫用作葡萄酒生产过程中的添加剂
D . 二氧化硅用作北斗芯片中的半导体材料
最近更新
- You’ve just missed your ______, and you will have to wait fo
- 阅读下面的文字,完成1—3题。 中国处于“文化孤立”之中吗 余秋雨 一位友好的美国音乐人说:“每个初次来华的西方人都会有
- 下图中,关于化工厂的建立哪个方案较为合理 ( )
- 思考判断(正确的打“√”,错误的打“×”) 增、减函数定义中的“任意x1,x2∈D”可以改为“存在x1,x2∈D”.()
- Live or not,a famous American actor, was always expecting___
- 史学家邓广铭认为:“宋代物质文明和精神文明所达到的高度,在中国整个封建社会历史时期之内,可以说是空前绝后的。”与该论述不
- 水陆草木之花,可爱者甚蕃。晋陶渊明独爱菊;自李唐来,世人盛爱牡丹;予独爱莲之出淤泥而不染,濯清涟而不妖,中通外直,不蔓不
- 已知一组数据的频率分布直方图如下. 求(1)众数;(2)中位数;(3)平均数.
- 在中,有理数的个数是 ▲ 个。
- 男女同学之间交往恰当的方式有 ①经常单独呆在一起 ②尊重对方,不随意干扰别人的生活和学习 ③学会自爱、自重,并懂得保护自
- 如图所示,墙上挂有一边长为的正方形木板,它的四个角的空白部分都是以正方形的顶点为圆心,半径为的圆弧,某人向此板投镖,假设
- 甲组有5名男同学、3名女同学;乙组有6名男同学、2名女同学,若从甲、乙两组中各选出2名同学,则选出的4人中恰有1名女同学
- 金属M与AgNO3溶液发生反应:M+2AgNO3===M(NO3)2+2Ag,下列说法正确的是( ) A.M可能是铝
- (本题2分+3分+4分)某商场将每件进价为80元的某种商品原来按每件100元出售,一天可售出100件,后来经过市场调查,
- 已知正实数a,b满足+=1,则a+b的最小值为() A.1 B.2 C.4 D.2
- 下图中表示北半球气旋示意图是( )
- Newrules will let millions of Americans know where more of t
- 现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是(
- ( )55. Could you tell me _________? A. how old is y
- 在等比数列{an}中,前n项和Sn=2n+c,则a12+a22+a32+…+an2等于_______________.







