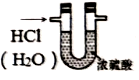制取氢氧化铁、氢氧化亚铁 知识点题库
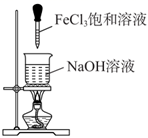
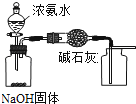 B . 用装置制备Fe(OH)2并能较长时间观察其颜色
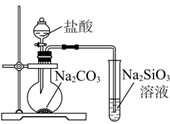
B . 用装置制备Fe(OH)2并能较长时间观察其颜色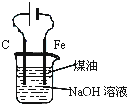 C . 装置可证明非金属性Cl>C>Si
C . 装置可证明非金属性Cl>C>Si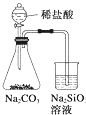 D . 装置向左推动针筒活塞可检验该装置的气密性
D . 装置向左推动针筒活塞可检验该装置的气密性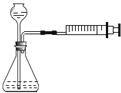
方法一:用不含的FeSO4溶液与用不含O2的蒸馏水配制的NaOH溶液反应来制备.
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需加入 . 发生反应的离子方程式:
(2)除去蒸馏水中溶解的O2常采用 的方法.
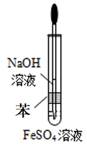
(3)生成白色Fe(OH)沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液的液面下,再挤出NaOH溶液.这样操作的理由是
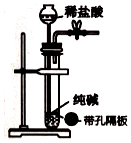
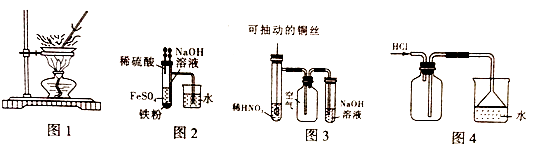
方法二:在如图的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂来制备.
(1)在试管Ⅰ里加入的试剂是 .(2)在试管Ⅱ里加入的试剂是 .
(3)为了制得白色Fe(OH)2沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,其理由是 .
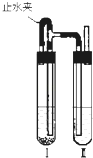
(1)将实验所需的稀硫酸和氢氧化钠溶液加热煮沸,其目的是 .
(2)按图所示连接好装置,打开止水夹a,反应片刻后,夹紧止水夹a,此时可观察到的现象是 ;乙中发生反应的离子方程式是 .
(3)将试管乙中的混合物倒入表面皿中,可观察到的现象 ;反应的化学方程式是 .
 比较Cl2、Fe3+、I2的氧化性
B .
比较Cl2、Fe3+、I2的氧化性
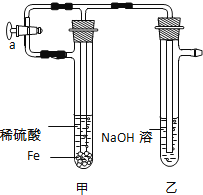
B . 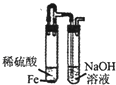 制取Fe(OH)2
C .
制取Fe(OH)2
C . 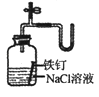 证明铁生锈时空气参加反应
D .
证明铁生锈时空气参加反应
D . 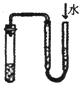 检查装置气密性
检查装置气密性
①取少量甲的品体溶于蒸馏水配成溶液:
②取少量甲溶液于试管中滴入KSCN溶液,无现象,再滴入氯水,溶液呈红色;
③取少量甲溶液于试管中加入适量NaOH溶液,加热:
④取少量甲溶液于试管中,向其中加入稀盐酸,再加入BaCl2溶液,出现白色沉淀。
回答下列问题:
-
(1) C的元素符号是,D在周期表中的位置。
-
(2) 用离子方程式表示实验②中现象的原因:。
-
(3) 实验③中出现的现象是。
-
(4) 经测定甲晶体(结晶水合物)的摩尔质量为392g/mol,其中阳离子与阴离子物质的量之比为3:2,则甲晶体的化学式为。
①SiO2 ②H2SiO3 ③Al(OH)3 ④Fe(OH)3 ⑤FeCl2
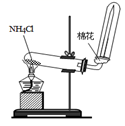
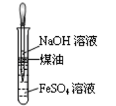 B . 制取氨气
B . 制取氨气 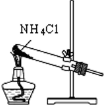 C . 分离碘和酒精
C . 分离碘和酒精 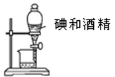 D . 收集少量二氧化氮气体
D . 收集少量二氧化氮气体 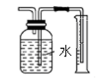
-
(1) NaHCO3能用于治疗胃酸过多,反应的离子方程式为。
-
(2) 铁和水蒸气反应的化学方程式为3Fe+4H2O(g)
 Fe3O4+4H2 , 该反应中84g Fe参加反应,转移电子的物质的量为。
Fe3O4+4H2 , 该反应中84g Fe参加反应,转移电子的物质的量为。
-
(3) 制备Fe(OH)3的实验操作:向煮沸的蒸馏水中加入几滴FeCl3溶液,。
-
(4) 密度为1.84g/cm3 , 质量分数为98%的浓硫酸的物质的量浓度为。
-
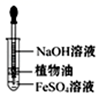
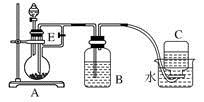
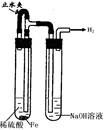
(1) B中盛一定量的NaOH溶液,A中应预先加入的试剂是,A中反应的离子方程式是:。
-
(2) 实验开始时就先将活塞E(填“打开”或“关闭”),C中收集到气体的主要成分是。
-
(3) 简述生成Fe(OH)2的操作过程。
-
(4) 拔去装置B中的橡皮塞,使空气进入,写出有关反应的化学方程式:。
| A | B | C | D |
| | | | |
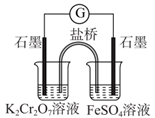
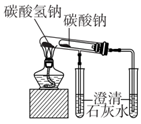
| 验证C的非金属性强于Si | 比较Fe2+和Cr3+还原性强弱 | 比较碳酸钠与碳酸氢钠的热稳定性 | 制备氢氧化铁胶体 |
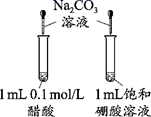 证明醋酸酸性比硼酸强
B .
证明醋酸酸性比硼酸强
B . 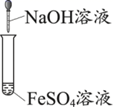 实验室制氢氧化亚铁
C .
实验室制氢氧化亚铁
C .  实验室制氨气
D .
实验室制氨气
D . 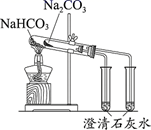 证明碳酸氢钠热稳定性比碳酸钠弱
证明碳酸氢钠热稳定性比碳酸钠弱
 、
、 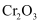 、
、 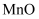 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下: 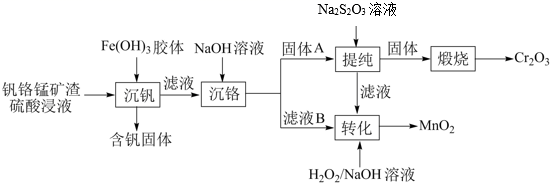
已知:pH较大时,二价锰[ 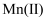 ](在空气中易被氧化.回答下列问题:
](在空气中易被氧化.回答下列问题:
-
(1) Cr元素位于元素周期表第周期族。
-
(2) 用
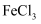 溶液制备
溶液制备 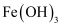 胶体的化学方程式为。
胶体的化学方程式为。
-
(3) 常温下,各种形态五价钒粒子总浓度的对数[
 ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中
]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中 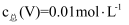 ,“沉钒”过程控制
,“沉钒”过程控制 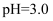 ,则与胶体共沉降的五价钒粒子的存在形态为(填化学式)。
,则与胶体共沉降的五价钒粒子的存在形态为(填化学式)。 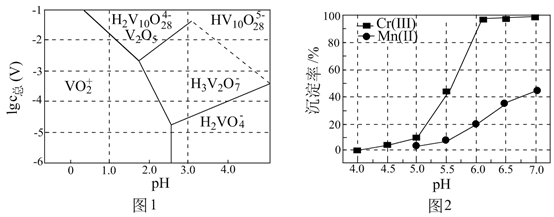
-
(4) 某温度下,
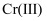 、
、 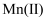 的沉淀率与pH关系如图2。“沉铬”过程最佳pH为;在该条件下滤液B中
的沉淀率与pH关系如图2。“沉铬”过程最佳pH为;在该条件下滤液B中 
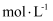 (
(  近似为
近似为 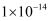 ,
, 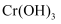 的
的  近似为
近似为 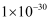 )。
)。
-
(5) “转化”过程中生成
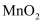 的离子方程式为。
的离子方程式为。
-
(6) “提纯”过程中
 的作用为。
的作用为。
 B . 证明过氧化钠与水反应放热
B . 证明过氧化钠与水反应放热 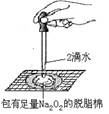 C . 制备并收集少量NO2气体
C . 制备并收集少量NO2气体 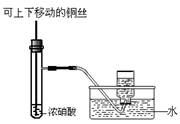 D . 实验室制备少量氨气
D . 实验室制备少量氨气 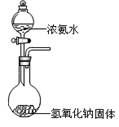
| | | | |
| A.“随开随用、随关随停”制CO2 | B.收集氨气的试管口处放置湿棉花,防止氨气与空气形成对流 | C.用浓H2SO4干燥HCl气体 | D.观察Fe(OH)2的生成 |
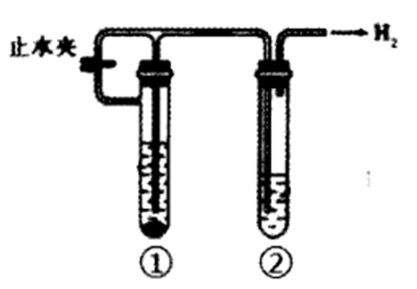
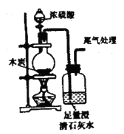 验证木炭和浓硫酸反应生成
验证木炭和浓硫酸反应生成 B .
B . 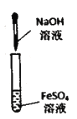 实验室制备
实验室制备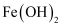 并能较长时间观察到白色固体
C .
并能较长时间观察到白色固体
C . 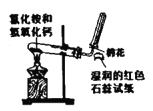 实验室制备和收集氨气并验满
D .
实验室制备和收集氨气并验满
D . 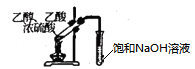 制备乙酸乙酯
制备乙酸乙酯
- 某校同学在水平直道上进行1000米跑步比赛。甲、乙两位同学同时出发,甲同学在整个比赛过程中作匀速运动。乙同学出发后,经过
- 观察图2,利用图形间的面积关系,写出一个代数恒等式: .
- A sharp sword was found buried together with the royal carpe
- 下列各组地形名称中,全部位于南方地区的是( ) A.东北平原 华北平原 东南丘陵
- (4分)在探究“固体熔化时温度的变化规律”实验中,某实验小组的同学根据测得的数据绘制了如图所示的图象.
- 新割的玻璃茶几有锋利的边缘,应把它磨平,这样使同一物体与之接触时 A.增大压力 B.减小压力
- Theteacher,with6 girls and 8 boys of her class, __________vi
- 用性引诱剂诱杀农业害虫是利用了( ) A.昆虫的取食行为 B.昆虫之间的通讯 C.昆虫的学习行为
- 当抵抗抗原侵入的功能过强时,进入人体内的某些食物和药物会引起____________反应。
- (浙江卷)2.下列各句中,没有错别字的一项是( ) A.散文是倍受读者青睐的文体,古今中外的散文家凭借生花妙
- 李伟在实验室药品柜中发现一瓶标签残缺的无色溶液(如图),老师告诉他这是实验室常用的试剂。这瓶溶液可能是 A.氯化钾
- 党的十七大提出要大力发展教育和科学事业。下列关于大 力发展教育和科学事业的说法不正确的是( ) A.有助于人民思想道德水
- 分子式为C10H14的单取代芳烃(苯环上只有一个侧链),其可能的结构有( ) A. 2种 B. 3种
- 以前,人们通常认为植物不像人和动物一样具有“记忆力”。近来,科学家在实验中发现,照射到一片叶子上的光,能够让整株植物作出
- 英国依仗工业革命所形成的技术基础, 在 19 世纪中期一跃成为最大的经济强国, 占据了工业霸主的地位, 把竞争对手远远地
- 加入Al能产生H2的溶液中一定能大量共存的是( ) A. K+、Na+、Br-、SO42- B.Na+、
- 某服装店购进一批甲、乙两种款型的时尚T恤衫,甲种款型共用了7800元,乙种款型共用了6400元,甲种款型的件数是乙种款型
- 下面关于酶的论述正确的是( ) ①对底物有严格的选择性 ②酶在体内不能更新 ③温度越高酶的活性越大
- 用如图所示的装置进行电解,在通电一段时间后,铁电极的质量增加。(1)写出乙中两极发生的电极反应式。 阴极:_______
- 下列各句没有语病且表意明确的一句是( ) A.氨基酸即便有益无害,“吊瓶”即便真是为学生健康着想,但当高三学生竟然要以