探究碳酸钠与碳酸氢钠的性质 知识点题库
-
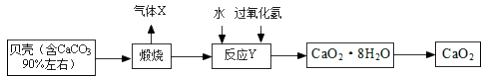
(1) 将过氧化钙晶体与溶液分离的方法是。
-
(2) 我国制碱工业的先驱侯德榜先生为纯碱和氮肥工业技术的发展做出了杰出的贡献。其制备 原料有气体 X、氨气、精制饱和食盐水,过程主要是先制得小苏打,再过滤并加热分解小苏打制得纯碱。
①实验过程中应该先向精制饱和食盐水中通入,其原因是。
②请写出制备纯碱第一步发生的化学方程式。
-
(3) 反应Y不能在较高温度下进行的原因是; 已知该反应是化合反应,则反应 Y 的化学方程式是;获得的过氧化钙晶体中常含有 Ca(OH)2 杂质,原因是。
-
(4) 现设计如下实验测定制得的过氧化钙晶体[CaO2·8H2O]中 CaO2 的质量分数:称取晶体样品25 g,加热到 220℃充分分解,其产物含有参与反应 Y 的固体物质和能使带火星木条复燃的气体等(此时所得气体混合物的总质量为1.6 g)(已知杂质不发生变化),则该晶体样品中 CaO2 的质量分数是。
①SiO2 ②Al ③Al2O3 ④Al(OH)3
⑤Na2CO3溶液 ⑥Ca(HCO3)2溶液 ⑦NH4HCO3溶液 ⑧KHSO4溶液
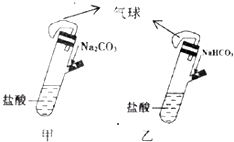
①质量相同的两种钠盐,NaHCO3与足量的酸反应产生的CO2比Na2CO3多 ②质量相同的两种钠盐,与足量酸反应产生相同体积(同温、同压下)的CO2 ③NaHCO3与酸反应生成CO2比Na2CO3快得多 ④NaHCO3比Na2CO3稳定,便于长期保存
-
(1) 小苏打的化学式:。
-
(2) 写出乙醛的结构简式:。
-
(3) 甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃。已知室温下1g甲硅烷自燃生成SiO2固体和液态水放出热量44.6kJ,则其热化学方程式为。
 Fe(s)
Fe(s) 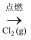 FeCl2(s)
B . Cu2S(s)
FeCl2(s)
B . Cu2S(s) 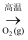 Cu(s)
Cu(s) 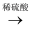 CuSO4(aq)
C . Al(s)
CuSO4(aq)
C . Al(s)  NaAlO2(aq)
NaAlO2(aq)  Al(OH)3(s)
D . NaCl(aq)
Al(OH)3(s)
D . NaCl(aq) 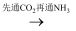 NaHCO3(s)
NaHCO3(s)  Na2CO3(s)
Na2CO3(s)
| A | B | C | D |
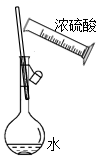
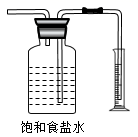
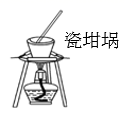
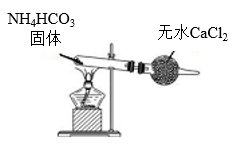
| 配制一定浓度的稀硫酸 | 测量Cl2的体积 | 加热熔融NaOH固体 | 制取干燥的氨气 |
| | | | |
 与
与  分别与足量的盐酸反应,
分别与足量的盐酸反应,  产生的
产生的  更多
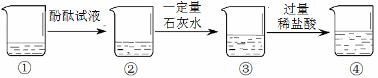
C . 可以用澄清石灰水鉴别碳酸钠溶液和碳酸氢钠溶液
D . 向
更多
C . 可以用澄清石灰水鉴别碳酸钠溶液和碳酸氢钠溶液
D . 向  中加入少量水后,
中加入少量水后,  能溶解,并伴随着吸热现象
能溶解,并伴随着吸热现象
| 选项 | 实验 | 现象 | 结论 |
| A | 向含有酚酞的Na2CO3浴液中加入BaCl2溶液 | 溶液颜色变浅 | Na2CO3溶液存在水解平衡 |
| B | 用pH计测定浓度均为0.1mol•L-1的NaCl和NaF溶液的pH | NaF溶液的pH较大 | 非金属性F>Cl |
| C | 向浓度均为0.1mol•L-1的BaCl2和CaCl2混合液中滴加Na2SO4溶液 | 出现白色沉淀 | Ksp(BaSO4)<Ksp(CaSO4) |
| D | 将铜与浓HNO3反应生成的气体收集后用冰水混合物冷却 | 气体颜色加深 | 2NO2(g) |
 )+c(HCO
)+c(HCO )+c(H2CO3)=0.10mol·L-1
B . 2c(CO
)+c(H2CO3)=0.10mol·L-1
B . 2c(CO )+c(HCO
)+c(HCO )<c(Na+)
C . 向其中滴加少量稀盐酸时(保持温度不变),CO
)<c(Na+)
C . 向其中滴加少量稀盐酸时(保持温度不变),CO +H2O
+H2O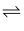 HCO
HCO +OH-的平衡常数增大
D . 向其中滴加少量NaOH溶液时,
+OH-的平衡常数增大
D . 向其中滴加少量NaOH溶液时, 的值增大
的值增大
选项 | 实验内容 | 实验目的 |
A | 向两支盛有5 mL不同浓度KMnO4溶液的试管中分别加入同浓度同体积的足量草酸溶液,观察实验现象 | 探究浓度对反应速率的影响 |
B | 向盛有1 mL 20%蔗糖溶液的试管中滴入3 ~ 5滴稀硫酸,将混合液煮沸几分钟、冷却,在冷却后的溶液中加入银氨溶液 | 检验蔗糖的水解产物中是否有葡萄糖 |
C | 向盛有2 g碳酸钠粉末的试管中加入少量水后,碳酸钠粉末结块变成晶体,用手触摸试管壁 | 验证碳酸钠粉末遇水生成碳酸钠晶体是放热反应 |
D | 向盛有5 mL 0.05 mol·L-1FeCl3溶液的试管中加入1 mL 0.15 mol·L-1 KSCN 溶液,溶液显红色,再加入1mol· L-1 KSCN溶液 | 验证 Fe3+和SCN-的反应为可逆反应 |
- 《汉书·地理志》载:“秦遂并兼四海,以为周制微弱,终为诸侯所丧,故不立尺土之封,分天下为郡县。”材料中的“周制”是指
- 在同一坐标系中,图象表示同一曲线的是( )A.y=f(x)与y=f-1(x)
- —Have you told her about it? —No,I really don't know
- 1787年宪法具有一定的民主性,下列内容最能体现其民主性的是( )A.总统和国会议员由选举产生 B.立
- 读珠江三角洲城市化发展示意图,完成下列问题。从1985年到2002年,珠江三角洲城市化发展迅速,其城市化过程具体表现在
- (本题满分10分)下面是计算应纳税所得额的算法过程,其算法如下: 第一步 输入工资x(注x<=5000); 第二
- 在19世纪的科学家中,其科学思想对于解放人们的思想与哥白尼的太阳中心说可以比拟的是( )A.爱因斯坦的相对论 B.
- 对金属制品进行抗腐蚀处理,可延长其使用寿命. (1)下列为铝材表面处理的一种方法:①碱洗的目的是除去铝材表面的自然氧化膜
- It would be very exciting to be areporter on a newspaper. As
- 某物质的化学式为RO2,其中R与氧的质量比为1∶1,则R是_____元素(符号或名称)。
- 如图所示,一理想变压器接在电压为U的交流电源上,原线圈接入电路的匝数可以通过调节滑动触头P来改变,副线圈连接了交流电流表
- Time flies as an arrow. I'm already in the second half 1._
- 运用“人工膜技术”制作的携有单克隆抗体的磷脂微球体药物如图所示。当药物被注射到实验鼠血液中一段时间后,首先在某种癌细胞内
- 下列关于水的说法不正确的是() A.水是一种氧化物
- “通过我的心灵给你送去温暖,让我的双手把你的风雨分担。”汶川大地震发生后,全国各地支援灾区,人们慷慨解囊争相捐款,无数志
- 实数满足,使取得最大值的最优解有两个,则的最小值为 A、0 B、 C、1 D、
- 我国城市居民委员会和农村村民委员会的相同之处是( ) A.前者是城市居民的自治组织,后者是基层的国家机关 B.前者有
- 某扇形的面积为1,它的周长为4,那么该扇形圆心角的度数为 ( ) A.2°
- (-1)2等于() A. B. 1 C. D. 2
- 右为“司隶校尉”印文, 掌握此印长官的职责是 A.掌管军事 B.协助皇帝管理行政C.削弱诸侯王封国
 N2O4(g)△H<0
N2O4(g)△H<0


