几组未知物的检验 知识点题库
(1)取少量固体粉末加到足量水中,得到白色沉淀,上层为无色清液.
(2)继续往其中加入足量稀硝酸,白色沉淀完全消失,并有气泡产生.
(3)取少量(2)中的溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶.
根据上述实验现象判断:该白色固体中一定含有 ,一定不含有 ,可能含有 .
如何验证可能存在的物质 .
-
(1) 由此推出各试剂瓶所盛的试剂为(填化学式):
A:,B:,C,D.
-
(2) A+B反应的离子方程式为.
-
(3) A+D反应的离子方程式为.
-
(1) 甲取少量白色固体在试管内用水溶解,结果得无色澄清的液体.因此,甲说肯定有一种物质不存在.这种物质的化学式是:
-
(2) 甲又先后向那试管内加入了稍过量的BaCl2溶液和稀硝酸,结果是先产生了白色沉淀,后又有一部分沉淀消失并从溶液里冒出无色气泡.因此甲又说肯定有两种物质存在.这两种物质是:、.
-
(3) 乙将甲所得混合物进行了过滤,取滤液约2mL盛于另一支洁净的试管里,然后又向该试管内加入了稍过量的AgNO3溶液和稀硝酸,结果也产生了白色沉淀.因此乙说那份白色固体中也肯定有NaCl.你说乙的结论(填“对”或“不对”),理由是:.
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
②向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中
一定含有的物质是,
一定不含的物质是,
可能含有的物质是(以上物质均写化学式),
写出第①步中反应的化学方程式:,
第②反应步中离子方程式:.
①将固体混合物溶于水,搅拌后得无色透明溶液
②往此溶液中滴加硝酸钡溶液,有白色沉淀生成
③过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解.
试判断,固体混合物中肯定有 ,肯定没有 ,可能有 ,对可能有的物质可采用滤液中滴加 溶液的方法来检验.(填化学式)
-
(1) A的化学式是,G的化学式是,判断的理由是.
-
(2) 写出其余几种物质的化学式.B:C:D:E:F:.
A
B
C
D
E
F
G
A
﹣
﹣
﹣
﹣
﹣
﹣
↓
B
﹣
﹣
﹣
﹣
↓
↓
↓
C
﹣
﹣
﹣
↓
﹣
↓
↓
D
﹣
﹣
↓
﹣
↓
↓
↓
E
﹣
↓
﹣
↓
﹣
↓
﹣
F
﹣
↓
↓
↓
↓
﹣
↓
G
↓
↓
↓
↓
﹣
↓
﹣
X | Y | Z | W | |
Y | ↑ | ﹣ | ↓ | 无明显现象 |
Z | ↓ | ↓ | ﹣ | 无明显现象 |
①取适量粉末投入蒸馏水中,粉末完全溶解,得到蓝色透明溶液A.
②取A溶液少量,向其中逐滴滴加烧碱溶液直到过量,观察到先有沉淀出现,而后沉淀逐渐增多,然后沉淀又逐渐减少,但最终仍有部分蓝色沉淀.
③再取A溶液两份,一份滴加BaCl2溶液后,出现白色沉淀;另一份滴加硝酸银溶液后也出现白色沉淀.
请回答下列问题:
-
(1) 原白色粉末一定含有,一定不含,可能含有.(填化学式)
-
(2) 写出过程②中涉及到的离子方程式:.
-
(3) 如果要进一步确定可能存在的物质,进行的实验操作及实验现象和结论是.
⑴将固体混合物溶于水,搅拌后得无色透明溶液
⑵往此溶液中滴加硝酸钡溶液,有白色沉淀生成
⑶过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解.
(填化学式)试判断,固体混合物中肯定有,肯定没有,可能有,对可能有的物质可采用滤液中滴加溶液的方法来检验.
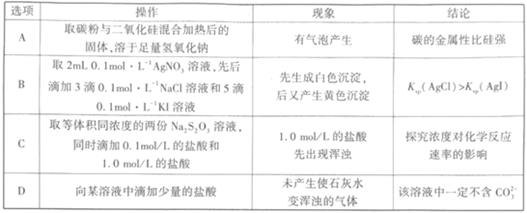
|
选项 |
实验方案、现象 |
结论 |
|
A |
用玻璃棒蘸取某样 品进行焰色反应,观察到黄色火焰 |
该样品中一定含钠元素 |
|
B |
将石蜡油(液态石蜡)分解的产物通入溴的四氯化碳溶液中,溶液逐渐褪色 |
分解产物中一定含有乙烯 |
|
C |
向酸性KMnO4溶液中先通入少量SO2 , 充分反应后,再滴入几滴BaCl2溶液,产生白色沉 |
SO2被氧化为SO42- |
|
D |
向FeCl3 溶液中加入过最的KI溶液,充分反应后,再滴入几滴KSCN溶液,溶液颜色变红 |
KI与FeCl3的反应为可逆反应 |
⑴将部分粉末加入水中,振荡,有白色沉淀生成;
⑵向(1)的悬浊液中加入过量稀硝酸白色沉淀消失,并有气泡产生;
⑶取少量(2) 的溶液滴入AgNO3溶液,有白色沉淀生成。下列说法正确的是( )
①取部分固体粉末加入水中,振荡,有白色沉淀生成;
②取①的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生;
试根据上述实验事实,回答下列问题:
-
(1) 原固体粉末中一定含有的物质是,可能含有的物质是。(写化学式)
-
(2) 写出上述步骤中发生反应的离子方程式:①。②。
-
(3) 若要判断可能含有的物质是否存在,则可取少量①中的上层清液分成两份,一份,另一份(补充实验步骤)
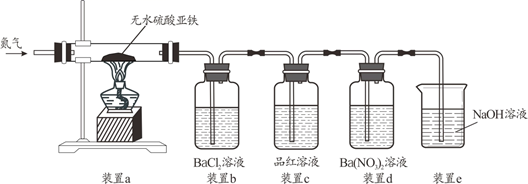
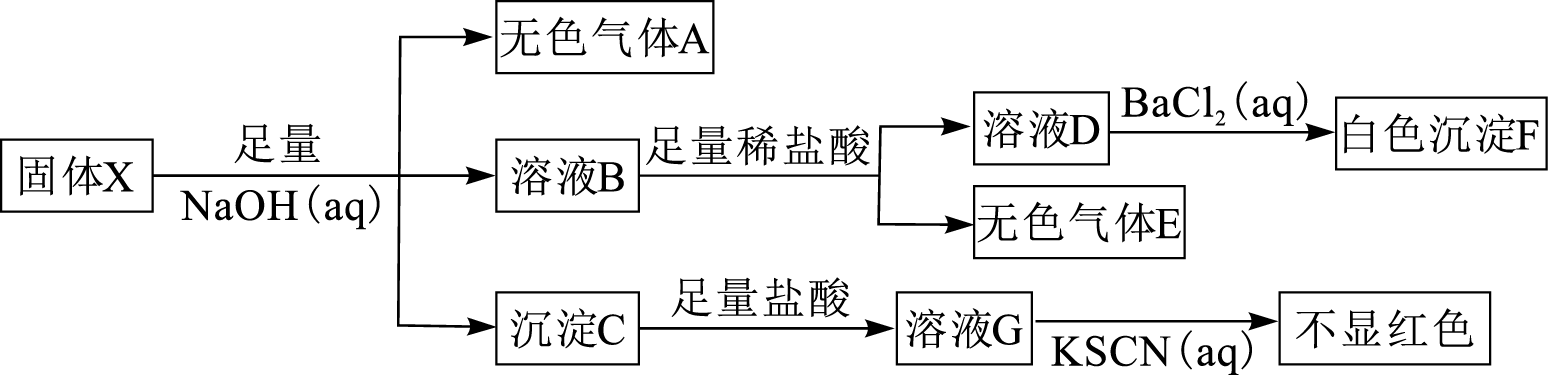
根据实验过程及现象,下列说法正确的是( )
| 选项 | 实验目的 | 实验操作 | 现象和结论 |
| A | 除去甲烷中混有的乙烯 | 将气体通入 | |
| B | 探究浓硫酸性质 | 向蔗糖中加入浓硫酸蔗糖变成疏松多孔的海绵状碳,并放出有刺激性气味的气体 | 浓硫酸具有脱水性和强氧化性 |
| C | | 向某溶液滴加 | 若产生白色沉淀,则该溶液含 |
| D | 检验 | 往该有机物中滴加酸性高锰酸钾溶液 | 酸性高锰酸钾溶液褪色,证明含有碳碳双键 |
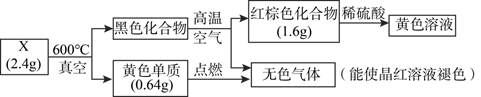
-
(1) 组成物质X的元素是。
-
(2) 黑色化合物转化为红棕色化合物的方程式为。
-
(3) 写出红棕色化合物与稀硫酸反应的离子方程式:
-
(4) 设计实验方案检验黄色溶液中的金属阳离子
- 2009年9月18日,中国第十七届中央委员会第四次全体会议公报指出:要更加注重推进结构调整,更加注重加快自主创新,更加注
- 2008年2月份全国居民消费价格(CPI)同比上涨8.73%,3月份CPI同比上升8.3%。下列措施能够起到抑制CPI过
- .1989年,中国与前苏联实现了关系正常化。这件事体现的外交原则是 A.一边倒 B.另起炉灶
- 古代雅典民主政治的本质特征是( ) A.公民直接参与国家管理 B.公职人员的普选制 C.奴隶主阶级的民主
- 下列叙述正确的是( ) A.两个纯种交配后,后代必是纯种 B.两个杂种交配后,后代必是杂种 C.纯种自交
- 英国君主立宪制的核心是 A.君主制 B. 责任内阁制 C.首相制 D. 议会制
- 某细菌能产生一种毒性肽,其分子式为C55H70O19N10,将它彻底水解后只能得到下列四种氨基酸,甘氨酸(C2H5NO2
- 已知NaHSO4显酸性,NaHCO3溶液显碱性,现有浓度为0.1mol·L-1的NaHSO3和NaHCO3两种溶液,两种
- (4分)已知某有机物的式量是58,根据下列条件回答有关问题:(1)若该有机物只由碳、氢两种元素组成,写出所有可能的结构简
- 用一定量的甲状腺激素连续喂养正常成年小白鼠4周,与对照组比较,实验组小白鼠表现为() A.耗氧量增加,神经系统的兴奋性降
- 实验室中,常用U形管压强计来探究液体内部压强规律的仪器,在研究液体内部压强与液体的密度关系时,要保持它的金属盒在不同液体
- 物质的性质决定物质的用途。下列对应关系不 成立的是
- (2014·北京东城区一模)下图是某国142°E经线附近气温、降水量分布图。读图,回答1~2题。1.图中() A.7月
- 如图所示,根据通过螺线管的电流情况,标出通电螺线管的N、S极。(2分)
- 反应L(s)+aG(g) bR(g)达平衡时,温度和压强对该反应的影响如图所示。图中压强P1>P2,x轴表示温度,
- 1901年1月,清廷发布上谕:“世有万古不易之常经,无一成不变之治法。……盖不易者三纲五常,昭然如日星之照世。而可变者令
- 题目:没想到我如此_________________(浮躁、虚荣、坚强、幸运、依赖父母……) 要求:①结合个人生活经历,
- 楼市调控新“国五条”,明确提出“扩大个人住房房产税改革试点范围”。政府开征房产税后,对商品房交易产生的影响用图示描绘出来
- ---- Do you know our town at all? -------No, this ________
- A、B、C、D、E、F、G、H、I都是初中化学中常见的物质。其中E、F、H均为黑色固体,B是紫红色固体,D是混合物。它们
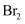 的
的  溶液中
溶液中 的检验
的检验 溶液和稀
溶液和稀 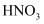
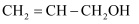 中的碳碳双键
中的碳碳双键


