离子反应发生的条件 知识点题库
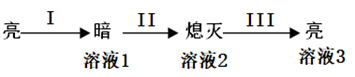
某模拟"人工树叶”电化学实验装置如右图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。下列说法正确的是( )
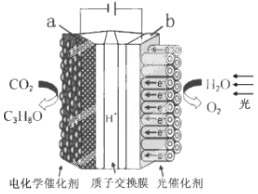
a气体 | b溶液 | 预测的现象 | |
① | CO2 | BaCl2溶液 | 白色沉淀析出 |
② | SO2 | Ba(NO3)2 溶液 | 白色沉淀析出 |
③ | Br2 | AgNO3溶液 | 淡黄色沉淀析出 |
④ | NH3 | AlCl3溶液 | 白色沉淀析出 |
-
(1) 在发生离子反应的反应物或生成物中,一定存在.(填序号)
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
-
(2) 用单线桥法标出下列方程式的电子转移数目和方向MnO4﹣+5Fe2++8H+═Mn2++5Fe3++4H2O
-
(3) 鲜榨苹果汁是人们喜爱的饮料.由于此饮料中含有Fe2+ , 现榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色的 Fe3+ . 这个变色的过程中的Fe2+被(填“氧化”或“还原”).若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生.这说明维生素C具有:.
A、氧化性 B、还原性 C、酸性 D、碱性.
①酸性氧化物与碱反应
②弱酸与盐溶液反应可生成强酸
③没有水生成,也没有沉淀和气体生成的复分解反应
④两种酸溶液充分反应后的溶液呈中性
⑤有单质参加的非氧化还原反应
⑥两种含氧化合物反应的产物有气体.
第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
甲 | BaCl2 | HCl | Cu(NO3)2 |
乙 | Fe2O3 | K2SO4 | H2SO4 |
丙 | Fe | NaOH | MgCl2 |
根据该表回答问题:
-
(1) 第Ⅲ组中有一种物质能与第组中的所有物质反应,这种物质是;
-
(2) 第Ⅱ组物质中,跟第Ⅰ组中所有物质都不能发生反应的是,该物质能与第Ⅲ组中所有物质发生反应,其化学方程式分别为
 H2↑+ Cu2+
C . 含0.1 mol FeBr2的溶液中通入0.1 mol Cl2:2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2Br2 + 6Cl-
D . 碳酸氢钙溶液中加入足量烧碱溶液:HCO3- + OH- = CO32- + H2O
H2↑+ Cu2+
C . 含0.1 mol FeBr2的溶液中通入0.1 mol Cl2:2Fe2+ + 4Br- + 3Cl2 = 2Fe3+ + 2Br2 + 6Cl-
D . 碳酸氢钙溶液中加入足量烧碱溶液:HCO3- + OH- = CO32- + H2O
实验操作 | 现象 | 结论 | |
A | 向收集满CO2的软塑料瓶中加入约1/3体积滴有石蕊试液的水,旋紧瓶盖,振荡 | 塑料瓶变瘪,溶液变红 | CO2能与石蕊反应 |
B | 往久置于空气中的氢氧化钠溶液滴加稀硫酸 | 有气泡 | 氢氧化钠溶液已变质 |
C | 在某无色溶液中滴加氯化钡溶液 | 有白色沉淀 | 无色溶液中一定含有 SO42-离子 |
D | 把质量相同的镁条与锌粒同时放入相同浓度和体积的盐酸中 | 镁条与盐酸产生气体更快 | 镁的金属活动性比锌强 |
①向饱和碳酸钠溶液中通入过量的 CO2
②向 Fe(OH)3 胶体中逐滴加入过量 H2SO4
③向 Ba(NO3)2 溶液中通入过量 SO3
④向石灰水中通入过量 CO2
⑤向硅酸钠溶液中逐滴加入过量的盐酸
|
实验1:向烧杯中依次加入下列试剂,记录灯泡变化 |
|
|
| ①Ba(OH)2粉末:灯泡不亮 ②加入蒸馏水:灯泡变亮 ③逐滴滴加0.1 mol/L H2SO4 , 灯泡变化如下: |
-
(1) Ba(OH)2与H2SO4在溶液中能发生反应。
a.置换反应 b.酸碱中和反应 c.复分解反应
-
(2) ①中灯泡不亮而②中加H2O后灯泡变亮的原因是加水后,Ba(OH)2发生了。
-
(3) 用离子方程式解释过程I中灯泡变暗的原因。
-
(4) 实验2:用Na2SO4溶液替代稀H2SO4 , 重复实验进行对照。加入Na2SO4溶液过程中灯泡不熄灭,原因是。
通过实验1和2可知:离子反应发生的条件之一是生成沉淀。
-
(5) 在两份完全相同的Ba(OH)2溶液中,分别滴入H2SO4和NaHSO4溶液(说明:等体积溶液含H2SO4和NaHSO4微粒数相同),其导电能力随滴入溶液体积变化的曲线如图所示。
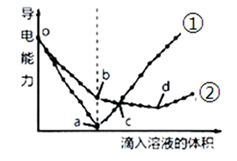
下列分析错误的是__________。
A . ①代表滴加H2SO4溶液的变化曲线 B . b点,溶液中大量存在的离子是Na+、OH-、SO C . c点,两份溶液中含有相同量的OH-
D . a、d两点对应的溶液均显中性
C . c点,两份溶液中含有相同量的OH-
D . a、d两点对应的溶液均显中性
-
(1) 不用做任何实验就可以肯定溶液中不存在的离子是。
-
(2) 取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,有关反应的离子方程式为。
-
(3) 取(2)的滤液加过量的NaOH溶液,出现白色沉淀,有关反应的离子方程式为。
-
(4) 原溶液中可能大量存在的阴离子是____________(填序号)。A . Cl- B . NO
 C . CO
C . CO  D . OH-
D . OH-
- 阅读下面的文字,并回答问题 一语未了,只听后院中有人笑声,说:“我来迟了,不曾迎接远客!”黛玉纳罕道:“这些人个个皆敛声
- 如图所示,边长分别为a、b的实心正方体甲、乙分别放在水平地面上,它们对地面的压强均为p,则甲物体的质量 ▲ (大
- 下图为人体内体温与水平衡调节的示意图,有关叙述正确的是( )①当受到寒冷刺激时,a、b、c、d激素的分泌均会增加
- 1954年颁布的《中华人民共和国宪法》是第一部社会主义性质的宪法 ( ) ①规定了国家的性质和根本的政治
- 在图形的全等变换中,有旋转变换,翻折(轴对称)变换和平移变换.一次数学活动课上,老师组织大家利用矩形进行图形变换的探究活
- 已知函数在处取得极小值 (1)求; (2)若对恒成立,求的取值范围。
- 海边盛产贝壳,其主要成分为CaCO3,以贝壳和纯碱为原料,生产烧碱的简要工艺流程如下:请回答下列问题: (1)A的化学式
- 如下图中的四个细胞图中,属于二倍体生物精子细胞的是()
- 选下列加点字注音全对的一项( ) A 震悚(sǒnɡ) 荒谬(miù) 溃退 (kuì) 锐不可当(d
- — Thank you for sharing your ruler with me.— . That’s what
- 近年来,浙江省仙居县大力推进“慈孝仙居”建设,着力打造“尊老、爱幼、孝亲”文明仙乡。忠孝是中华民族的传统美德,忠孝的观念
- 下列实验试剂或材料与其实验名称不相符合的是A.吡啰红和健那绿——观察DNA和RNA在细胞中的分布 B.澄清石灰水和重铬酸
- 在等差数列{an}中,已知a4+a8=16,则该数列前11项和S11= (A)58 (B)88
- 如图:A处通入氯气。关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色。由此作出的判断正确的是A.D中不可能
- 古代中国的春秋战国时期与古希腊的城邦国家时期处于同一时代,但却创造了不同的政治文明模式。造成这种不同的政治文明模式的主要
- 下列句子中没有语病的一项是 A.电信业内人士爆料,“高额吸费电话”能大行其道,是因为电信运营商参与了不法垃圾短信公司和声
- 函数的导数是( ) A. B. C.
- “在最小的空间内用最简单的耕作方式养活尽可能多的人是中国的终极目标,为此,他们将土地分成小块,劳动者把全部精力都投入到
- Where did you go lastnight?—I to go to LiLei’s birth
- 铝的阳极氧化是一种常用的金属表面处理技术,它能使铝的表面生成一层致密的氧化膜,该氧化膜不溶于稀硫酸。某化学研究小组在实验