摩尔质量 知识点题库
448mL某气体在标准状况下的质量为1.28g,该气体的摩尔质量约为( )
A . 32g
B . 48
C . 64g•mol﹣1
D . 32g•mol﹣1
元素周期表中大多数元素是金属元素,金属及其化合物在生活生产中有着重要应用,根据试题信息,完成下列计算:
-
(1) 某常见二价金属12.6g与足量稀硫酸反应,生成氢气5.04L(S.T.P),该元素原子的摩尔质量为
g/mol.
-
(2) 39.32g某金属混合物,由12.32g镁和0.25mol另一种比镁不活泼的金属元素A组成,该混合物与一定量盐酸反应,产生氢气4.928L(S.T.P),则参加反应的HCl为 mol,金属A的相对原子质量为
-
(3) 由NaCl、NaHCO3、Na2CO3•10H2O组成的混合物157.8g,充分加热后,产生的气体(气体温度150℃)依次通过无水CaCl2和碱石灰,两种吸收剂分别增重59.4g和13.2g,则混合物中NaHCO3的质量分数为 ,若等质量的该混合物与足量盐酸反应,产生二氧化碳(S.T.P) L.
下列叙述正确的是( )
A . 1mol H2O的质量为18g/mol
B . CO2的摩尔质量为44g
C . 3.01×1023个SO2分子的质量为32g
D . 标准状况下,1mol任何物质体积均为22.4L
下列说法不正确的是( )
A . 将标准状况下11.2L HCl溶于水,配成250mL盐酸,溶液的物质的量浓度为2mol/L
B . 硫酸和磷酸的摩尔质量相等
C . 同温同压下,相同质量的二氧化碳和二氧化硫的体积比是16:11
D . 2.24L CO和CO2混合气体中含有的碳原子数目为0.1NA
在同温同压下,向大小相同的气球分别充入CO和以下四种混合气体,当体积相等时A、B、C、D四个气球内,与充入CO气球内所含原子数一定相等的是( )
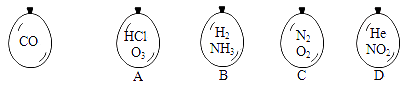
A . A
B . B
C . C
D . D
近20年来,同位素分析法在植物生理学、生态学和环境科学研究中获得广泛应用;如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用作环境指示物。下列有关说正确的是 ( )
A . 34S原子核内中子数为16
B . 1H218O的摩尔质量为20g/mol
C . 13C和15N原子核内的质子数相差2
D . 2H+的核外电子数为2
下列有关说法中不正确的是(不考虑盐的水解)( )
A . 同质量,不同密度的N2和CO所含原子数目相等
B . 标准状况下,1LO2含p个分子,则NA=22.4pmol-1
C . VLAl2(SO4)3溶液中含amol Al3+ , 则c(SO42-)= 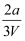 mol·L-1
D . 氦气的摩尔质量为Mg·mol-1 , 则一个氨原子的质量为
mol·L-1
D . 氦气的摩尔质量为Mg·mol-1 , 则一个氨原子的质量为  g
g
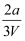 mol·L-1
D . 氦气的摩尔质量为Mg·mol-1 , 则一个氨原子的质量为
mol·L-1
D . 氦气的摩尔质量为Mg·mol-1 , 则一个氨原子的质量为  g
g
NA表示阿伏加德罗常数。下列说法错误的是( )
A . 32gO2所含的原子数目为NA
B . 18g水中含有的水分子数为NA
C . 17g氨气所含电子数目为10NA
D . 2.3gNa变成Na+时失电子数为0.1NA
下列说法正确的是( )
A . NH3→NH4Cl的转化过程中氮元素被还原
B . 2mol水的摩尔质量是1mol水的摩尔质量的两倍
C . 同温同压下,H2S气体的密度是NH3气体密度的两倍
D . 20% NaOH溶液中NaOH的物质的量是10% NaOH溶液中NaOH的物质的量的两倍
1mol/LNaOH溶液的含义是( )
A . 1L溶液中含有40gNaOH
B . 1L水中含有1molNaOH
C . 溶液中含有1molNaOH
D . 将40gNaOH溶于1L水中所得的溶液
-
(1) 按要求填写下列空格(设阿伏加德罗常数为NA)
①39 g Na2O2中的Na+NA;
②0.5mol H2O中的质子数为NA;
③1.204×1024个水分子的质量为 g;
④标准状况下,10g CO和CO2混合气体的体积是6.72L,则此混合气体中,CO和CO2的物质的量之比是;
⑤9.2g氮的氧化物NOx中含有N原子数为0.2mol,则x数值为。
-
(2) 用于分离或提纯物质的方法有:
A蒸馏(分馏) B萃取 C过滤 D重结晶 E分液
分离或提纯下列各组混合物,请选择上述最合适的方法的标号填在橫线上。
①除去Ca(OH)2溶液中悬浮的CaCO3微粒;
②分离四氯化碳与水的混合物;
③分离汽油和柴油;
④提纯氯化钠和硝酸钾混合溶液中的硝酸钾 。
-
(3) 找出下列各组物质中与另三种物质的类别不同的一种物质,用化学式填写在后面的横线上。
① CaO、Na2O、CO2、CuO ;
② H2、N2、P、Cu;
③ S、Fe、Cu、Zn;
④ HCl、H2O、H2SO4、HNO3。
对一定量气体体积的探究。已知1 mol不同气体在不同条件下的体积:
|
化学式 |
条件 |
1mol气体体积/L |
|
H2 |
0℃,101kPa |
22.4 |
|
O2 |
0℃,101kPa |
22.4 |
|
CO |
0℃,101kPa |
22.4 |
|
H2 |
0℃,202kPa |
11.2 |
|
CO2 |
0℃,202kPa |
11.2 |
|
N2 |
273℃,202kPa |
22.4 |
|
NH3 |
273℃,202kPa |
22.4 |
-
(1) 从表分析得出的结论:
①1mol任何气体,在标准状况下的体积都约为。
②1mol不同的气体,在不同的条件下,体积(填“一定”、“一定不”或“不一定”)相等。
-
(2) 理论依据:相同条件下,1mol任何气体的体积几乎相等,原因是:①,②。
-
(3) 应用:在标准状况下,4gO2的体积为。
-
(4) 等温、等压下,等体积的O2和O3所含分子个数比,质量比为。
-
(5) 已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为。
-
(6) 在三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)分别用p(Ne)、p(H2)、p(O2)表示,由大到小的顺序是__。
设NA为阿伏加德罗常数值,下列说法错误的是( )
A . 常温常压下,32gO2和32gO3所含氧原子数都是2NA
B . 同温、同压下,相同体积的氟气和氩气所含的原子数相等
C . 18g D2O含有的电子数为9NA
D . 2.4g金属镁变成镁离子时失去的电子数目为0.2NA
下列条件下,两瓶气体所含原子数不相等的是( )
A . 同质量、不同密度的  和CO
B . 同温度、同压强、同体积的
和CO
B . 同温度、同压强、同体积的  和
和  C . 同体积、同密度的
C . 同体积、同密度的 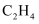 和
和  D . 同质量、同体积的
D . 同质量、同体积的  和
和 
 和CO
B . 同温度、同压强、同体积的
和CO
B . 同温度、同压强、同体积的  和
和  C . 同体积、同密度的
C . 同体积、同密度的 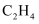 和
和  D . 同质量、同体积的
D . 同质量、同体积的  和
和 
设 NA为阿伏加德罗常数的值。下列有关叙述正确的是( )
A . 常温下,1 L 0.5 mol/L CH3COONH4 溶液的 pH=7,则溶液中 CH3COO-与 NH4+的数目均为 0.5NA
B . 10 g 质量分数为 46%的乙醇溶液中含有氢原子的数目为 0.6 NA
C . 16g 氨基(-NH2)中含有的电子数为 7 NA
D . 在密闭容器中将 2 mol SO2 和 1 mol O2 混合反应后,体系中的原子数为 8 NA
 表示阿伏加德罗常数,下列说法正确的是( )
表示阿伏加德罗常数,下列说法正确的是( )
A . NO的摩尔质量是 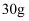 B . 标准状况下,
B . 标准状况下,  的体积是
的体积是 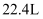 C .
C . 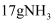 含有的原子总数为
含有的原子总数为  D . 摩尔
D . 摩尔 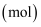 是国际单位制中七个基本物理量之一
是国际单位制中七个基本物理量之一
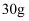 B . 标准状况下,
B . 标准状况下,  的体积是
的体积是 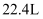 C .
C . 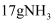 含有的原子总数为
含有的原子总数为  D . 摩尔
D . 摩尔 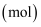 是国际单位制中七个基本物理量之一
是国际单位制中七个基本物理量之一
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)  CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
 CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
CH3OH(g) ΔH<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( ) 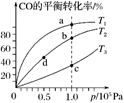
A . 温度:T1>T2>T3
B . 正反应速率:v(a)>v(c)、v(b)>v(d)
C . 平衡常数:K(a)>K(c)、K(b)=K(d)
D . 平均摩尔质量:M(a)<M(c)、M(b)>M(d)
NA为阿伏加德罗常数的值,下列说法正确的是( )
A . 12g  C所含的原子数为阿伏加德罗常数
B . O2的相对分子质量为32,所以O2的摩尔质量也为32。
C . 标准状况下,1molNO 与11.2L O2充分反应后分子总数为NA
D . P4为正四面体形分子,则1 mol P4分子中含有6NA个共价键
C所含的原子数为阿伏加德罗常数
B . O2的相对分子质量为32,所以O2的摩尔质量也为32。
C . 标准状况下,1molNO 与11.2L O2充分反应后分子总数为NA
D . P4为正四面体形分子,则1 mol P4分子中含有6NA个共价键
 C所含的原子数为阿伏加德罗常数
B . O2的相对分子质量为32,所以O2的摩尔质量也为32。
C . 标准状况下,1molNO 与11.2L O2充分反应后分子总数为NA
D . P4为正四面体形分子,则1 mol P4分子中含有6NA个共价键
C所含的原子数为阿伏加德罗常数
B . O2的相对分子质量为32,所以O2的摩尔质量也为32。
C . 标准状况下,1molNO 与11.2L O2充分反应后分子总数为NA
D . P4为正四面体形分子,则1 mol P4分子中含有6NA个共价键
设NA为阿伏加德罗常数值。下列有关叙述正确的是( )
A . 标准状况下,2.24L 三氧化硫中含原子数为0.4NA
B . 100g质量分数17%的H2O2溶液中极性键数目为NA
C . 常温常压下,10.0g碳酸氢钾中含离子数为0.3NA
D . 标准状况下,20g的D2O中所含质子数目和中子数目均为10NA
下列说法中,错误的是( )
A . Fe的摩尔质量是56 g·mol-1
B . 1 mol Cl2的体积一定是22.4 L
C . 1 mol N2中含有的分子数约为6.02×1023
D . 1 L1 mol·L-1NaOH溶液中含有1 mol Na+
最近更新
- 下图表示生物体内的某种物质,请分析回答下面的问题。(每空2分,共16分。)(1) A是由________________
- “节能减排”是当今社会发展的主题,下列做法不符合这一主题要求的是 A.燃料燃烧时供给充足的氧气 B.推广使用太阳能
- 下列各句中,加点的成语使用恰当的一项是( ) A.公园里摆放的各种盆栽菊花,正值花期,姹紫嫣红,微风一吹,更是
- 设向量a=(cosα,sinα),b=(cosβ,sinβ),且a,b满足|ka+b|=3|a-kb|(k为正实数).(
- After I mastered my firstconcerto(协奏曲) at age fourteen, my p
- 已知是两条不同的直线,是两个不同的平面,则下列命题正确的是( ) A.若,则 B
- 如图,已知D为△ABC边BC延长线上一点,DF⊥AB于F交AC于E,∠A=35°,∠D=42°,求∠ACD的度数.
- 已知椭圆E: +=1(a>b>0)的离心率为,右焦点到直线y=x的距离为. (1)求椭圆E的方程; (2)已知点M的坐标
- 关于世界人口的分布,叙述正确的是()。 A.世界人口稠密区都分布在经济发展水平高的国家 B.世界上的大平原都是人口稠密区
- 从某校随机抽取名学生,将他们的体重(单位:)数据绘制成频率分布直方图(如图),由图中数据可知= ,所抽取
- (1) (2)(3)
- 水平地面上的物体在水平恒力F的作用下由静止开始运动,一段时间后撤去F,其运动的v-t图像如图所示,若物体与地面间滑动摩擦
- 一颗子弹以水平速度v射入一树干中,射入深度为s.设子弹在树干中所受到的阻力为一恒力,那么子弹以的速度射入树干中,射入的深
- 胡萝卜根韧皮部的细胞在组织培养中,经过细胞增殖和细胞分化等过程可以发育为一个完整植株。下列说法中不正确的是 (
- It ishelpful to ________ a good habit of reading in languag
- 根据提示或要求答题: (1)读下列文段,任选一位诗人,写出他们的任一作品及广泛传诵的名句 有人说,语文是一首规模宏大的交
- 阅读材料,回答问题。材料二:“改革开放之初,我国基尼系数在0.3左右,90年代中期达0.42,但到了2010年,已经达到
- “依依”一词的意义有:①形容留恋,不忍分离;②形容树枝柔弱,随风摇摆。(只填序号)(1)在春暖花开的美好季节里,我邀请
- 下列现象或事实能说明分子之间有间隔的是。 A.用手捏气球,可以使气球变瘪。 B.墙内开花墙外香。 C.100ml的水与1
- 下列各组变化中,前者属于物理变化,后者属于化学变化的是()A . 铁生锈,自行车胎爆炸B . 矿石粉碎,分离液态空气制氧



