分液和萃取 知识点题库
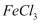 溶液中加入3mL5mol/L KF溶液,发现
溶液中加入3mL5mol/L KF溶液,发现 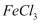 溶液渐渐褪至无色,再加入KI溶液和
溶液渐渐褪至无色,再加入KI溶液和  振荡后,静置,不见
振荡后,静置,不见  层有紫红色,则下列说法正确的是( )
层有紫红色,则下列说法正确的是( ) 不与 I- 发生反应
B .
不与 I- 发生反应
B .  与 F- 结合成不与 I- 反应的物质
C . F-使 I-的还原性减弱
D .
与 F- 结合成不与 I- 反应的物质
C . F-使 I-的还原性减弱
D .  被F-还原为
被F-还原为 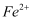 ,使溶液中不再存在
,使溶液中不再存在 
①CCl4和水②乙醇和甘油③乙醛和水④苯和水⑤己烷和水⑥环己烷和苯⑦溴苯和水.
选项 | 实验目的 | 所选主要仪器(铁架台等忽略) | 部分操作 |
A | 用浓硫酸配制480mL0.1mol/L硫酸溶液 | 500mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管 | 将量取好的浓硫酸放入容量瓶中,加水溶解至刻度线 |
B | 从食盐水中得到NaCl晶体 | 坩埚、酒精灯、玻璃棒、泥三角、三角架 | 当加热至大量固体出现时,停止加热,利用余热加热 |
C | 分离甲醇和甘油的混合物 | 蒸馏烧瓶、酒精灯、温度计、直形冷凝管、锥形瓶、牛角管 | 温度计水银球插入混合液液面以下 |
D | 用CCl4萃取溴水中的Br2 | 分液漏斗、烧杯 | 分离时下层液体从分液漏斗下口放出,上层液体从上口倒出 |
 B . 实验室制取蒸馏水
B . 实验室制取蒸馏水  C . 从饱和食盐水中提取氯化钠晶体
C . 从饱和食盐水中提取氯化钠晶体  D . 分离酒精和水
D . 分离酒精和水 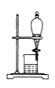
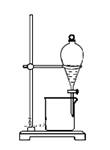 B . 除去氯化钠晶体中混有的氯化铵晶体
B . 除去氯化钠晶体中混有的氯化铵晶体 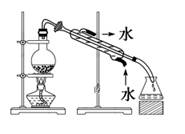 C . 分离CCl4中的Br2
C . 分离CCl4中的Br2 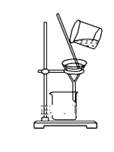 D . 除去CO2气体中的HCl气体
D . 除去CO2气体中的HCl气体 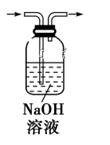
| 实验 | 操作或结论 |
| A.浓硫酸加入到蔗糖中 | 蔗糖变黑体现了浓硫酸的吸水性 |
| B.实验室收集NO | 可用排空气法收集 |
| C.SO2通入高锰酸钾溶液 | 高锰酸钾溶液褪色,说明SO2具有漂白性 |
| D.CCl4萃取碘水中的I2 | 先从分液漏斗下口放出有机层,后从上口倒出水层 |
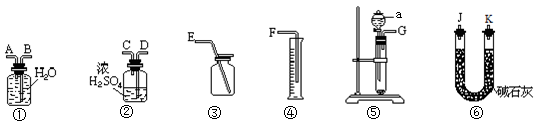
请回答下列问题:
-
(1) 装置⑤中仪器a的名称是。
-
(2) 用上述装置可以组装一套最简单的测定过氧化钠样品纯度的实验装置。
Ⅰ.该实验装置的组合是(填字母)。
a. ①④⑤
B. ①③⑤
C. ②④⑤
D. ③⑤⑥
Ⅱ.所选用装置的连接顺序应是(填各接口的字母,连接胶管省略)。
-
(3) 写出实验中Na2O2发生反应的化学方程式。
-
(4) 用上述实验后所得溶液配制成浓度为1.0mol/L的溶液,回答下列问题。
①向400mL该溶液中通入0.3mol CO2 , 则所得溶液中HCO3–和CO32–的物质的量浓度之比约为。
A.1:3 B.1:2 C.2:1 D.3:1
②将上述溶液蒸发结晶得到Na2CO3和NaHCO3固体混合物,下列选项中不能准确测定混合物中Na2CO3质量分数的是。
a. 取a g混合物充分加热,在干燥器中冷却至室温,减重b g
b. 取a g混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b g固体
c. 取a g混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b g
d. 取a g混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b g固体

下列说法正确的是( )
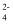 + 2HBr
C . ③中主要发生的是置换反应
D . 用酒精萃取精溴中的单质溴
+ 2HBr
C . ③中主要发生的是置换反应
D . 用酒精萃取精溴中的单质溴
海带 海带灰
海带灰 悬浊液
悬浊液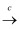 含I-的水溶液
含I-的水溶液 含I2的溶液
含I2的溶液 含I2的CCl4溶液
含I2的CCl4溶液 晶体碘
晶体碘
-
(1) 步骤c的操作方法是;除烧杯外,还需要使用的玻璃仪器是、。
-
(2) 最后的蒸馏通常用水浴加热而不是用酒精灯火焰直接加热,其原因为 。
-
(3) 步骤e的
 操作方法叫做,所用的主要实验仪器是 ,最初从该仪器流出的液体颜色为 色。
操作方法叫做,所用的主要实验仪器是 ,最初从该仪器流出的液体颜色为 色。
| A | B | C | D |
| | | | |
| 橡皮管能减小气体体积测量的误差 | 分离碘和四氯化碳的混合液 | 浓硫酸与萤石(主要成分为CaF2)加热制备HF | 防止铁管道被腐蚀 |
-
(1) I.某同学将铁铝合金样品溶解后取样25.00mL,分离并测定Fe3+的浓度,实验方案设计如下:
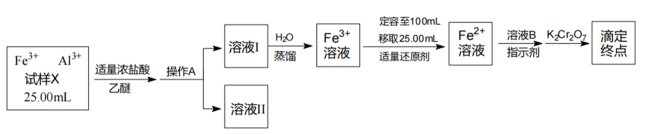
已知:乙醚[(C2H5)2O]是一种易挥发、易燃、有麻醉性的有机化合物,沸点为34.5℃,微溶于水。在较高的盐酸浓度下,Fe3+与HCl、乙醚形成化合物[(C2H5)2OH][FeCl4]而溶于乙醚;当盐酸浓度降低时,该化合物解离。
完成下列填空:
操作A的名称是。经操作A后,请设计实验方案判断Fe3+是否有残留。
-
(2) 滴定前,加入适量溶液B进行酸化,则B可能是。
a.H2SO3-H3PO4 b.H2SO4-H3PO4
c.HNO3-H3PO4 d.HI-H3PO4
-
(3) 滴定达到终点时,消耗0.1000 mol·L-1 K2Cr2O7溶液6.00 mL(生成物中Cr元素为+3价)。根据该实验数据,试样X中c(Fe3+)为。
-
(4) 上述测定结果存在一定的误差,为提高该滴定结果的精密度和准确度,可采取的措施是____。A . 稀释被测试样 B . 减少被测试样取量 C . 增加平行测定次数 D . 降低滴定剂浓度
-
(5) II.利用下图装置和试剂可以测定铁铝合金样品中的铝含量。
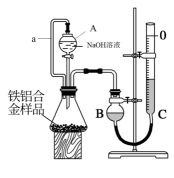
请回答:
下列有关该实验的说法中正确的是____。
A . 由于恒压分液漏斗的存在,该装置不能进行气密性检查 B . 读数前需将量气管C上下移动使B、C中的液面相平 C . 反应完成后生成的氢气都要转移至装置B中 D . 需要控制NaOH的量以防止产生气体过多超过量气装置的量程 -
(6) 若将恒压分液漏斗(A)去掉导管a,改成普通分液漏斗,则测得铁铝合金中的铝含量,(填“偏大”、“偏小”或“不变”),请说明理由。
分离提纯 | 试剂 | 方法 | |
A | 除去CO2中的HCl | NaOH溶液 | 洗气 |
B | 提取溴水中的溴单质 | CCl4 | 萃取 |
C | 除去NaCl中的Na2CO3 | 盐酸 | 蒸发结晶 |
D | 除去H2O中的Fe3+ | — | 蒸馏 |
- 以下表述能够反映夏、商、西周时期社会面貌的是 ①国家机构初具规模 ②金属农具普遍使用 ③建立邮驿传递制度
- 的展开式中,项的系数为 (用数字作答)
- 钛和钛合金被认为是21世纪的重要金属材料,已知钛原子的中子数为26,相对原子质量为46,则钛原子的质子数为( )
- 某公司向计算机个人用户提供免费的安全和杀毒服务,占据了国内网络安全软件市场的半壁江山。该公司的产品和服务之所以免费提供,
- 化学就在我们身边,它与我们生产、生活息息相关。请从①氢气②氮气③干冰④氧化钙⑤甲烷⑥石灰石中选择合适的物质填写下面空格(
- 历史文物是后人了解历史的第一资料,通过下图所示文物,我们可以了解哪一时期的历史A.商朝
- 如图所示,R1=10Ω,电流表A1示数为0.5 A,电源电压为10 V.下列叙述不正确的是() A.R1与R2并联
- 常用金属铝的元素符号是() A. Ag
- The professor has received the letter ____ to give a lecture
- 请运用你在初中学过的化学知识和技能,解决下列生活中的实际问题(在每个问题对应的横线上写出你选用的物质或方法): (1)暖
- 某种极具观赏价值的兰科珍稀花卉很难获得成熟种子,为尽快推广种植,可应用多种技术获得大量 优质苗,下列技术中不能选用
- . By no means _______ say like that. It is likely to spoil y
- The volleyball match will be put off if it______ . A. wil
- It is reported that the _________ between Israel and Palesti
- (二)古代诗歌阅读。(11 分) 阅读下面这首诗,完成 14-15 题。 绵谷回寄蔡氏昆仲 罗 隐 一年两度锦城游,前值
- 实验室提纯含少量氯化钠杂质的硝酸钾的过程如图所示.下列分析正确的是()A.操作Ⅰ是过滤,将固体分离除去 B.操作Ⅱ是加
- 影响樱花开放时间自南向北逐渐推迟的主要因素是( )
- 金刚石、石墨、C60都是碳元素组成的单质,关于它们的说法不正确的是() A.碳原子的排列不同 B.化学性质相似 C.完全
- 如图是某同学做实验时的电路图。闭合开关S后,发现灯泡L1、L2均不亮,电流表示数为零,电压表示数等于电源电压,则该电路中
- ___ human beings live in large numbers, the waters are very





