固体溶解度的概念 知识点题库

-
(1) 图中一处明显错误的操作是 (填序号),改正操作后,用上述图示的序号表示配制溶液的正确操作顺序 .
-
(2) 现配制100kg这种溶液,需氯化钠 kg;
-
(3) 现用质量分数为12%的氯化钠溶液(密度约为1.09g/cm3),配制50g质曼分数为6%的氯化钠溶液.需要质量分数12%的氯化钠溶液 mL(计算结果精确到0.1),需要水 mL(水的密度为1g/cm3).
-
(4) 20℃时,向50g水中加入20g氯化钠,充分溶解后,得到溶液的质量为68g,则20℃时,氯化钠的溶解度为 g.
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |
NaCl、KNO3两种物质的溶液度曲线图如图所示,请回答:

-
(1) 由图可知,20℃时氯化钠的溶解度为g.
-
(2) 依据图分析下列问题:50℃时,将氯化钠、硝酸钾固体各40g 分别加入两只各盛有100g水的烧杯中,充分搅拌,其中(填写物质化学式)得到饱和溶液;另一种物质的溶液中再加 入 g该溶质,溶液恰好饱和;若将温度都降到20℃,硝酸 钾溶液中溶质的质量分数(填“>”“<”或“=”)氯化钠溶液中溶质的质量分数.
-
(1) 过去,水曾被看成是一种元素,1781年英国科学家卡文迪许发现,在氢气与氧气的混合气中点火后会有水球生成。微观示意图如下所示:
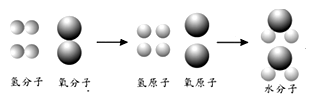
上述变化的微观实质为。
-
(2) 1783年拉瓦锡通过实验合成了水,还将水分解为氢气和氧气,确认了水是由组成的(填化学用语)。
-
(3) 水是最重要的溶剂。已知20℃时,氯化钠的溶解度为36g,20℃时把20g氯化钠放入50g水中,形成溶液的质量为g,该溶液中含有的粒子有(填化学用语)。

 时,进行了如下图所示的实验,下列叙述正确的是:
时,进行了如下图所示的实验,下列叙述正确的是: 

-
(1) 甲和乙的溶解度相等时的温度为
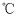 ;
;
-
(2) 上述实验过程中,属于不饱和的溶液的是(填字母,下同);溶液中溶质的质量分数相同的是。
-
(3) 将
 时,等质量的甲、乙饱和溶液降温至
时,等质量的甲、乙饱和溶液降温至  ,所得溶液中溶剂的质量甲乙(填“
,所得溶液中溶剂的质量甲乙(填“ 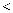 ”、“
”、“  ”或“
”或“  ”)。
”)。
-
(4) 将
 时,
时,  甲的饱和溶液降温至
甲的饱和溶液降温至  时,析出晶体的质量
时,析出晶体的质量 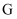 .
.


 ℃时NaCl和KNO3饱和溶液升温到40℃,KNO3溶液的溶质质量分数大于NaCl溶液的溶质质量分数
℃时NaCl和KNO3饱和溶液升温到40℃,KNO3溶液的溶质质量分数大于NaCl溶液的溶质质量分数
|
温度(℃) |
10 |
20 |
30 |
40 |
60 |
80 |
100 |
|
|
溶解度(g/100g水) |
硝酸钾 |
20.9 |
31.6 |
45.8 |
64 |
110 |
169 |
246 |
|
氯化钠 |
35.8 |
36 |
36.3 |
36.4 |
37 |
38.4 |
39.8 |
①从含有80g硝酸钾和9g氯化钠的混合物中提纯硝酸钾,进行如下实验(实验中不考虑各种损耗)

Ⅰ80℃时,硝酸钾的溶解度是。
Ⅱ80℃时,“溶液1”是(选填“饱和”或“不饱和”)溶液。将此溶液恒温蒸发50g水,降温至20℃,所得“溶液3”中硝酸钾的溶质质量分数是。
Ⅲ“溶液2”中硝酸钾质量(选填“<”“>”或“=”)“溶液3”中硝酸钾质量。
Ⅳ若固体M是纯净物,为得到更多固体M,“溶液3”最多还可以恒温蒸发g水。
②20℃时,在100克水中分别放入等质量的硝酸钾和氯化钠,都形成了饱和溶液,如右图所示。

请用两种不同的方法鉴别A和B烧杯中的物质,写出方法、现象与结论。
方法一。
方法二。
-
(1) 汽水中的气态溶质是(填化学式),打开瓶盖会有气体溢出,其原因是压强(填“增大”或“减小”),气体的溶解度减小。
-
(2) 厨房中的下列物质中放入足量水中,能得到溶液的是____(填字母序号)。A . 食盐 B . 蔗糖 C . 食用碱 D . 花生油 E . 面粉
-
(3) 氯化钠和蔗糖的溶解度如下表所示:
温度/℃
20
40
60
80
100
溶解度/g
氯化钠
36.0
36.6
37.3
38.4
39.8
蔗糖
203.9
231
287.3
362.1
487.2
①氯化钠和蔗糖都属于(填“易溶”、“可溶”、“微溶”、“难溶”)物质。
②若蔗糖中混入了少量的食盐,可以用(填“蒸发结晶”或“降温结晶”)的方法提纯蔗糖。
③若向60℃的100g水中加入250g蔗糖,可形成g蔗糖溶液,若将此溶液降温至20℃,可析出晶体g。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | |
溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | |
-
(1) 50℃时,NaCl的溶解度是g。
-
(2) 如图是NaCl和NH4Cl的溶解度曲线,则NH4Cl的溶解度曲线是(填“a”或“b”)。t℃时,若饱和NaCl溶液和饱NH4Cl溶液中溶质的质量相等,则下列说法错误的是(填字母)。

A.两种溶液中溶剂的质量相等
B.两种溶液中溶质质量分数相等
C.t℃大于20℃
-
(3) 20℃时,将mgNaCl不饱和溶液平均分为三份,并分别进行如下操作:



据此分析,x=,mgNaCl不饱和溶液中水的质量为g。

-
(1) 在t2℃时,向盛有10ga物质的烧杯中加入10g水,充分溶解后,所得溶液的质量为g。
-
(2) t2℃时,a、b、c三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是。
-
(3) 将t1℃时,将盛有c的饱和溶液的小试管放入盛水的烧杯中(如图2),向烧杯中加入一定量的氢氧化钠固体后,试管中产生的现象是。

-
(1) t1℃时,三种物质的溶解度由大到小的顺序是。
-
(2) t2℃时,使b的饱和溶液变为不饱和溶液,可采用的方法有。
-
(3) t2℃时,将40g a物质加入到50g水中充分搅拌,得到g溶液。
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
溶解度/g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 |
-
(1) 由表中数据可知,硝酸钾属于(填“易溶”“可溶”“微溶”或“难溶”)物质。
-
(2) 由表中数据可知,硝酸钾的溶解度随温度升高而。
-
(3) 使硝酸钾饱和溶液变为不饱和溶液,可采用的一种方法是。
- (08山东卷)分裂期细胞的细胞质中含有一种促进染色质凝集为染色体的物质。将某种动物的分裂期细胞与G1期(DNA复制前期)
- 如图1,△ABC中,∠ABC、∠ACB的平分线交于O点,过O点作BC平行线交AB、AC于E、F. (1)请写出图1中线段
- 弹簧上端固定,下端悬挂一根磁铁.将磁铁托起到某一高度后放开,磁铁能上下振动较长时间才停下来.如果在磁铁下端放一个固定的闭
- 一匹雄性黑马与若干匹纯种枣红马交配后,共生出20匹枣红马和23匹黑马。下列叙述中最可能的是() ①雄性黑马是杂合子 ②黑
- 下列几种估测最符合实际情况的是 ( ) A.人步行的速度约为5m/s B
- 所谓“求同存异”就是 A在不同的文化中找出他们的共同点 B在相同的文化中找出不同的特点 C只接受相同
- 下图中①、②、③、④为二分二至日气压带、风带分布示意图的一部分,读图回答如果图中风带皆影响大陆西岸,那么最不可能形成温带
- 肺循环的起点和体循环的终点分别是() A.右心室 右心房 B.左心室左心房 C.右心室 左心房 D.左心
- —What about _____concert? —Coco Lee’s concert? To be honest,
- 下列叙述中,正确的是 A.在船舶的外壳装上铜块可防止其发生电化学腐蚀 B.MnO2、FeCl3和CuSO4都可加快H2O
- 在△ABC中,若sinA=2sinBcosC,sin2A=sin2B+sin2C,试判断△ABC的形状.
- 认真阅读选文,完成后边各题。 “沙漠明珠”珠光渐暗 ①和莫高窟同称为敦煌两大奇观的月牙泉有“沙漠明珠”之称,但由于干旱缺
- 近年来有人提出了利用海水(含氯化钠)处理含二氧化硫的废气,该方法的流程 如下: (1) 上图中从海水最终得到“NaC
- 小明同学家买了一辆小汽车,车上配有安全带和安全气囊。安全带的宽度比较大,这是为了______压强(选填“增大”或“减小”
- f(x)=x5+ax3+bx-8,f(-2)=10,则f(2)等于( )A.-26
- A、B、C三个物体放在旋转的圆台上,动摩擦因数均为μ。A的质量为2m,B、C的质量均为m,A、B离轴R,C离轴2R,则
- (10·江西E篇) Every day we experience one of the wonders of the
- -- Have you moved into the new house? -- Not yet. The roo
- 阅读下面的文字,完成5-7题。 中国是小米和大米的起源地。小米是指粟、黍,主要在黄河流域起源和发展,后来成为中国北方的主
- 补全对话。 请根据对话内容,在对话空白处填入一个适当的单词,使对话意思完整与正确,并将答案填在答题卡相应的横线上。 W:



