晶体和结晶的概念与现象 知识点题库

-
(1) 50℃时,乙物质的饱和溶液中溶质与溶液的质量比为;
-
(2) 通过加溶质、蒸发溶剂和加热都能将接近饱和的溶液变为饱和溶液的物质是
-
(3) 50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃时,析出晶体最多的是,所得溶液中溶质质量分数最小的是.
-
(4) 若除去甲中混有的少量乙时,有以下实验步骤:
①常温下溶于水②过滤 ③降温结晶④蒸发浓缩.
合理的先后顺序是.



-
(1) 温度为℃时,A与C物质的溶解度相等.
-
(2) t2℃时,把A,B物质各30g分别加到50g水中,不能形成饱和溶液的是(填字母代号)
-
(3) t2℃时,将等质量A,B,C三种物质的饱和溶液降温至t1℃,所得的三种溶液中,溶剂质量的大小关系是(用字母代号和“>“、”<“或“=”填写)

-
(1) 20℃时,KNO3的溶解度约为g;
-
(2) 要使氯化钠从其饱和溶液中大量结晶析出,最好采用的结晶方法是
-
(3) 将NaCl和KNO3各30g,分别放入10℃100g水中充分溶解,能形成饱和溶液的是;(选填“NaCl”或“KNO3”)
-
(4) 分别将40℃的NaCl饱和溶液与KNO3饱和溶液,同时降温至10℃,下列有关说法中,正确的是 . (填序号)A . 析出晶体的质量一定相等 B . KNO3溶液变成不饱和溶液 C . 两种溶液中溶质质量分数关系:NaCl>KNO3 .


-
(1) P点的含义是
-
(2) t2 ℃时30g a物质加入到50g水中不断搅拌,能形成80g溶液吗?(填写“能”或“不能”)。
-
(3) t2 ℃时a、b、c三种物质的溶解度按由小到大的顺序排列是(填写物质序号)。
-
(4) 将t1 ℃时a、b、c三种物质饱和溶液的温度升高到t2 ℃时,三种溶液的溶质质量分数大小关系是 (填写选项序号)。A . c>a=b B . a=b>c C . a>b>c D . b>a>c
-
(1) 水(填“属于”或“不属于”)人类所需的六大基本营养素之一。
-
(2) 含有较多可溶性钙、镁化合物的水叫做(填“软水”或“硬水”)。
-
(3) 下列净化水的单一操作中,相对净化程度较高的是 (填字母)。A . 静置沉淀 B . 吸附沉淀 C . 蒸馏
-
(4) 水在通电的条件下可以分解,写出该反应的化学方程式。
-
(5) 甲和乙两种固体物质的溶解度曲线如下图所示,

回答下列问题:
①在℃时,甲和乙两种物质的溶解度相等。
②将t1℃时等质量的甲和乙两种物质的饱和溶液分别降温到0℃,析出固体质量较少的是(填“甲”或“乙”)。
③t2℃时,将60 g甲物质放入100 g水中,充分搅拌,所得溶液的溶质质量分数w(甲)与同温下乙物质的饱和溶液的溶质质量分数w(乙)大小关系为(填字母)。
A.w(甲)<w(乙) B.w(甲)>w(乙) C.w(甲)=w(乙) D.无法确定
-
(1) 净化水常用的方法有沉淀、过滤等,活性炭在净水器中能起到过滤和 的作用。
-
(2) 下列洗涤方法中,利用乳化原理的是__________________。A . 用洗涤精清洗衣服上的油污 B . 用酒精洗去试管中的碘 C . 用汽油清洗油渍
-
(3) 要将一瓶接近饱和石灰水变成饱和溶液,小明选择了如下的方法。其中可行的是(填序号)
①加入 CaO ②加入Ca(OH)2③升高温度 ④降低温度
-
(4) 如下图为甲、乙两种固体物质的溶解度曲线,请 据图回答下列问题

①t2℃时,甲、乙两种物质饱和溶液中的溶质质量分数的大小关系为:甲 乙(填“>”、“<”或“=”)。
②要从乙的饱和溶液中获得较多的晶体,宜采用的结晶方法是 结晶。
③t1℃,取等质量的甲、乙两种固体分别配成饱和溶液,需水质量较多的是(填“甲”或“乙”)。
-
(5) 下图是小明配制 50.0g 质量分数为18%的蔗糖溶液的实验操作示意图:

①配制上述溶液,小明需要称取蔗糖g
②用上图所示的序号表示符合题意配制该溶液的操作顺序为。
A.DECAB
B.ECADB
C.EDABC
③认真观察,改正图中的不符合题意操作。

| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度(g/100g 水) | 32 | 46 | 64 | 85.5 | 110 | 138 | 170 |
甲是 80℃含有 100g 水的 KNO3 溶液,操作过程如图所示。以下分析错误的是( )


 乙
B . 溶剂质量:甲
乙
B . 溶剂质量:甲  乙
C . 溶液质量:甲
乙
C . 溶液质量:甲 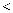 乙
D . 溶质质量
乙
D . 溶质质量

-
(1) 某同学设计的鉴别 NaNO2、NaCl固体的方案如下:
20℃时,取6.0gNaNO2和6.0gNaCl分别放入两只小烧杯中,各加入10mL水(水的密度为 1g/mL)。用玻璃棒充分搅拌后 观察现象。你认为此方案(填“可行”或“不可行”)。
-
(2) 除去 NaNO2固体中混有的少量 NaCl,实验步骤,加 水溶解,蒸发浓缩,,然后过滤、洗涤、干燥。
-
(3) 20℃时,将 182.2gNaNO2饱和溶液蒸发掉50g水,再降温到20℃,可析出晶体的质量为。
-
(4) 根据溶解度曲线,关于 NaNO2和NaCl 下列说法中错误的是______。A . 60℃时,NaNO2溶液的溶质质量分数大于NaCl溶液的溶质质量分数 B . 0℃时,等质量的两种固体加水配成饱和溶液,所得溶液的质量NaNO2溶液大于 NaCl溶液 C . 40℃时,NaNO2的饱和溶液降低温度,溶质质量分数减少 D . 60℃时,两种物质的饱和溶液降温到20℃时,NaNO2析出的晶体较多

A. t2℃三种物质的饱和溶液中,溶质质量最大的是A
B. t1℃的A,B,C三种物质的饱和溶液,分别蒸发等量的水后恢复至t1℃,析出溶质的质量B>A=C
C. 可用降低温度的方法使t2℃时C的不饱和溶液变为饱和溶液
D. 将t2℃时的三种物质的饱和溶液降温至t1℃时,溶质的质量分数由大到小的顺序是: .


|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
|
KNO3 |
13.3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
245 |
|
NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
39.8 |

-
(1) 依据上表数据,绘制KNO3 、NaCl的溶解度曲线,下图1中能表示KNO3溶解度曲线的是。(填“a”或“b”)
-
(2) 下图1中P点的含义是。
-
(3) 要使接近饱和的KNO3溶液,在不增加溶液质量的前提下变成饱和溶液,可以采用 。
-
(4) 30℃时,在两个各盛有100g水的烧杯中,分别加入相同质量的氯化钠和硝酸钾,充分溶解后,其结果如上图2所示,加入的甲物质是。
-
(5) 硝酸钾中含有少量氯化钠时,可通过(填“蒸发结晶”或“降温结晶”)的方法提纯。有下列可供选择的操作步骤:a.结晶 b.降温 c.热水溶解 d.过滤,具体采用的操作步骤依次是 。
-
(6) 20℃时,136g饱和食盐水,蒸发10g水后,再降温到20℃,可析出NaCl晶体的质量为g。
-
(7) 60℃时,将60g硝酸钾放入盛有50g水的烧杯中,充分搅拌,所得溶液的质量为g。
-
(1) 滇池,亦称昆明湖、昆明池、滇南泽、滇海。是云南省最大的淡水湖,有高原明珠之称,滇池不仅是昆明人民的母亲湖,更是一个丰富的生态系统。某学校化学兴趣小组的同学们欲对滇池的水样进行如下研究。
①小张先将水样进行,除去其中的难溶性杂质,再利用活性炭的性除去水中的异味; 再利用蒸馏的方法制取蒸馏水,在蒸馏过程中,水中加入少量碎瓷片的作用是。
②小李取该水样,利用如图装置完成实验。该实验中,负极和正极产生的气体体积比约为。

③为了保护好滇池,下列做法有利于保护水资源的是。
A.禁止在滇池中出现任何水生生物
B.禁止向滇池流域排放污水
C.关停滇池流域范围内的小型工厂
D.治理流域内的所有河流
-
(2) 如图是A、B、C三种不含结晶水的固体物质的溶解度曲线。

①t2℃时,将20gA加入60g水中,所得溶液的质量为g。
②t3℃时,取相同质量的A、B、C配制饱和溶液,所得溶液质量由大到小的关系是。
③将t2℃时A、B、C三种物质的饱和溶液升温至t3℃,所得溶液的溶质质量分数由大到小的关系是。
温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度/g | KCl | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
- 下列鸟类的行为中,属于求偶行为的是① 家燕南飞 ② 孔雀展屏 ③ 亲鸟喂小虫给雏鸟 ④ 雄鸽围着雌鸽跳跃转动⑤ 金丝燕用
- —Ididn’t hear you come in just now. — That’s good. We tri
- ----Youdidn’t wait for Mr. Smith last night, did you? ----
- 我国实行计划生育政策,但目前每年新增人口仍达1200多万,主要原因是( ) A.出生率高B.死亡率低 C.人口基
- 斯塔夫里阿诺斯的《全球通史》在“宋朝的黄金时代”的标题下写道,除了文化上的成就外,宋朝时期值得注意的是发生了一场名副其实
- 比较下列各组微粒半径,正确的是 ①Cl<Cl-<Br- ②F-<Mg2+<Al3+
- 下列说法中正确的是( ) A 只有镜面反射遵守光的反射定律 B 漫反射不遵守光的反射定律
- 用价层电子对互斥理论(VSEPR)预测H2S和NF3的立体结构,两个结论都正确的是( ) A.直线形;三角锥形
- The new medical care policy will be _____ to us all. A. gr
- 有人认为,联邦制下设“50个小政府”,做不到“全国一盘棋”,更谈不上“全国人民一条心”,因而是一种低效的国家结构形式,不
- 下列叙述错误的是() A.在实验室中,切不可吃东西、喝水 B.实验后不一定要洗手 C.进行实验操作前一定要对双手消毒 D
- 用铂丝做焰色反应实验,每次做完实验后铂丝都需要() A.用水洗涤2~3次后再使用 B.用滤纸擦干净即可使用 C.用盐酸洗
- 在泡沫橡胶的制造中,要利用下面反应放出的氧气:该反应中的双氧水( ) A.仅为氧化剂B.仅为还原剂C.既是
- 下列说法不正确的是( ) A.空间中,一组对边平行且相等的四边形是一定是平行四边形; B.同一平面的两条垂线一定
- 已知函数f(x)=则f(f(-2))=__________ _.
- 下图反映的史实发生于 A.英国 B.美国 C.法国
- 空气中含量最多的是( ) A. B. C.He
- 如图,在△ABC中,AD⊥BC,△ABD的面积是△ACD面积的2倍,沿AD将△ABD翻折,使翻折后BC⊥平面ACD,此时
- 太平天国曾先后颁布了《天朝田亩制度》和《资政新篇》,两部文献的共同特点是 A.试图在中国发展资本主义
- 阅读下面一首诗,然后回答问题。 武昌阻风 唐五代·方泽 江上春风留客舟,无穷归思满东流。 与君尽日闲临水,贪看飞花忘却愁



