盐的化学性质 知识点题库
化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH如下表
溶液 | Na2SO4 | NaHCO3 | Na2CO3 |
pH | pH=7 | pH>7 | pH>7 |

-
(1) 小新同学认为该溶液不可能的是 , 理由是 .
-
(2) 标签破损的原因 .
-
(3) 为确定其成分,小新同学设计如下方案进行探究
实验步骤
现象
结论
取该溶液少许于试管中,滴加过量的BaCl2溶液,振荡.
①
则该溶液是Na2CO3溶液
过滤,向滤渣滴加稀盐酸.
②
-
(4) 小芳认为可以设计更简单的实验方案,该方案是:(写出实验步骤、现象及结论).
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
-
(1) 哪几次反应中碳酸钙有剩余?
-
(2) 上表中m的值为 。
-
(3) 试计算这种石灰石中碳酸钙的质量分数。
A.对安全的认识 | B.用“化学”眼光分析 |
①点燃可燃性气体前一定要验纯 ②煤气泄漏立即打开排气扇 ③煤矿矿井要保持通风、严禁烟火 | ①洗涤剂去除油污是因为乳化作用 ②用适量的熟石灰可中和土壤的酸性 ③用水灭火是降低温度至可燃物的着火点以下 |
C.化学与健康 | D.对除杂和鉴别的认识 |
①霉变的大米洗净烧熟后可以食用 ②利用甲醛水溶液浸泡水产品防腐 ③人体缺铁会导致贫血 | ①用灼热的CuO除去CO中少量CO2 ②用Ca(OH)2溶液除去NaOH溶液中的Na2CO3 ③用燃烧的方法区分羊毛和涤纶 |
一种“环保石头纸”开始被人们使用,其主要成分是碳酸钙.某班同学对它产生了浓厚的兴趣,把“环保石头纸”带到实验室,完成了如右图所示的两个实验.请回答问题: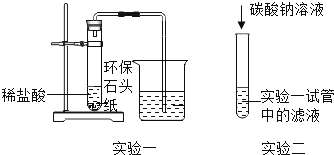
-
(1) 实验一:试管中产生大量的气泡,烧杯中澄清的石灰水变浑浊,请写出“环保石头纸”与稀盐酸发生反应的化学方程式 (假设“环保石头纸”中的其他成分既不溶于水,又不与盐酸发生反应);
-
(2) 实验二:试管中有白色沉淀产生.小刚同学想探究该实验反应后溶液中溶质的成分.
提出猜想:猜想①:NaCl、CaCl2和HCl;猜想②:NaCl;猜想③:NaCl和CaCl2 .
同学们经过讨论排除了猜想,理由是.
有同学认为小刚的猜想不全面,又提出猜想④:NaCl和Na2CO3 , 并通过实验验证了该猜想成立.请你将实验报告补充完整.
实验操作
实验现象
实验结论
取实验二反应后的上层清液少量于试管中,滴加少量 .
猜想④成立
-
(3) 实验结束后,未经处理的废液 (填“能”或“不能”)直接倒入下水道.
-
(1) 以上操作合理的而先后顺序为(数字序号不能重复使用).
-
(2) 请写出BaCl2溶液与Na2CO3溶液反应的化学方程式.
-
(3) 上述试剂中的Na2CO3不能用K2CO3代替,请说明原因.
|
A |
B |
C |
D |
|
|
|
|
|
|
在一定量的AgNO3溶液中逐滴加入NaCl溶液 |
等物质的量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 |
向稀盐酸溶液中逐滴加入氢氧化钠溶液 |
等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 |
①取少量样品溶于水得到无色溶液,然后滴加过量的氯化钡溶液,出现白色沉淀A,过滤.
②沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体.往步骤①所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B,过滤.回答下列问题:
-
(1) 白色沉淀B是,步骤②中放出的气体是.
-
(2) 杂质中一定含有,一定没有.
-
(3) 最终所得滤液中含有的阳离子是.
【猜想假设】
猜想1:该溶液没有变质,为NaOH溶液.
猜想2:该溶液全部变质,为Na2CO3溶液.
猜想3:该溶液部分变质,为NaOH和Na2CO3的混合溶液.
-
(1) 【设计方案】请你完善下表几组同学探讨的设计方案
实验操作
可能出现的现象与结论
同学评价
第1组
取少量样品溶液于试管中,向其中滴加酚酞试剂
若溶液变红,则猜想2不成立
第2组同学认为:此方案结论不正确,理由是:.
第2组
取少量样品溶液于试管中,向其中滴加足量的溶液CaCl2溶液
若产生白色沉淀,反应方程式是:,
则猜想(1)不成立
第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立
第3组
第一步:将第2组实验后的混合物过滤.第二步:取滤液于试管中,向其中滴加酚酞试剂
若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立.
第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:
.
-
(2)
【探究实验】综合各小组的方案后,动手实验.
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
【拓展延伸】同学们设计了下列两套装置进行实验:用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.

甲装置中可能发生反应的方程式是.
-
(3) 若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是(填化学式).
【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO3):84、Mr(H2O):18、Mr(MgO):40、Mr(CO2):44]

-
(1) 【实验步骤】
① ;
②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a,;
编 号
1
2
3
实验前
228.00
228.00
228.00
实验后
229.10
229.11
229.09
⑥准确称量C装置的质量(如右表);
⑦重复上述步骤;
⑧根据数据进行计算.
-
(2) 【实验分析及数据处理】
A装置中盛放的溶液是,其目的是;
-
(3) D装置的作用是;
-
(4) 计算碳酸镁晶须中的n值:(要有计算过程)
-
(5) 【实验反思】
实验结果与理论值有偏差,可以在B、C增加一个装置以减少误差;
-
(6) 下列选项中,会造成实验结果偏大的是;偏小的是;
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
-
(7) 为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热重分析,并绘制出如图2所示的热重曲线示意图.则:
①t2℃时,剩余固体为(填化学式);
① 最终剩余的4.0g物质是(填化学式);
② 碳酸镁晶须完全分解的化学方程式为:.
选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
A | CaCO3(CaO) | ﹣﹣ | 高温煅烧 |
B | KOH溶液(K2CO3) | 适量Ca(OH)2溶液 | 滴加试剂、过滤 |
C | Cu(Fe) | 适量CuSO4溶液 | 滴加试剂、过滤 |
D | CO2(CO) | 足量NaOH溶液 | 洗气、干燥 |
艾江南同学做出以下猜测:
猜测一:只有Cu2(OH)2CO3;猜测二:只有CuSO4•3Cu(OH)2 . 你认为还有一种可能性,你的猜测是.
资料(一):Cu2(OH)2CO3的化学性质可看成Cu(OH)2和CuCO3混合物的性质;CuSO4•3Cu(OH)2的化学性质可看成Cu(OH)2和CuSO4混合物的性质.
资料(二):CuCO3的分解温度约为220℃,CuSO4分解温度约为650℃,酒精灯外焰温度约为400℃.
经过分析,你认为验证你的猜测只要判断铜锈中有无和(填离子符号)两种离子即可.
为此,你利用如图装置设计了如下实验方案:

实验步骤 | 实验现象 | 实验结论 |
取样品放于试管中,加热. | 若观察到 | 则证明有Cu2(OH)2CO3 |
取加热后试管中的残留固体投入装有水的烧杯中,并向其中滴入几滴BaCl2溶液 | 若观察到溶液先变蓝色,后有 | 则证明有CuSO4•3Cu(OH)2 |


-
(1) 实验1中,两支试管的溶液都变成色。
-
(2) 实验2中,若试管B中盛装的是NaOH溶液,发生反应的化学方程式为,该反应的基本类型是反应。
-
(3) 实验3中,某同学向两支试管中吹气,A中有白色沉淀产生,发生反应的化学方程式为。B中无明显现象,为了探究吹气后B中溶质的成分,该同学进行了如下探究。
(提出猜想)猜想1:溶质是氢氧化钠;
猜想2:溶质是碳酸钠;
猜想3:溶质是。
溶质中出现碳酸钠的原因是氢氧化钠与发生了反应。
(实验和结论)
实验
实验现象
结论
取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,静置后取上层清液,向其中滴加几滴酚酞溶液
猜想3成立
(反思与评价)
老师评价该同学得出的结论错误,是因为猜想2也会产生相同的现象。如果要验证“猜想3成立”,必须要将氢氧化钙溶液换成溶液。

-
(1) 镁原子的质子数为,x值为。
-
(2) 镁属于元素(填“金属”或“非金属”),金属镁在化学反应在容易(填写“得到”或“失去”)电子。
-
(3) 海水中含有丰富的氯化镁,目前工业上绝大多数的金属镁是从海水中提取的,其生产流程如图:

在上述流程中,通过操作a分离出固体Mg(OH)2 , 操作a的名称是,试剂C为:。
反应①的化学方程式为。
反应②的化学方程式为。
-
(4) 上述流程中没有涉及到的基本反应类型是反应。
(实验探究)
-
(1) A,B,C,D四组同学分别进行了下列实验

写出下列的两个化学方程式:
①A中的反应;
②D中的反应。
-
(2) (挖掘实质)
如下图是A组反应的微观过程示意图,该化学反应的实质可以表示为:H++OH-=H2O

(实践运用)
完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色。
①溶液中的白色沉淀一定是,理由是
②废液中一定不含有的离子是和。
-
(3) 为了验证该溶液中能会含有的离子是否存在,我设计如下实验进行验证:
溶液中可能含有的
离子
实验步骤
实验现象
实验结论
①。
②取滤液滴加。
现象明显
含有该离子
-
(1) 碳酸钠俗称苏打或。如图为侯氏制碱法的流程图,通过步骤I后得到的悬浊液中有小苏打(在该溶液中难溶)和一种氮肥,请写出步骤I中发生反应的化学方程式:;上述过程中得到的氮肥遇碱会生成具有刺激性气味的(填化学式),该气体能使;从流程图中可得出小苏打的一条化学性质是。

-
(2) 氢氧化钠在空气中容易变质生成碳酸钠,现有放在空气中一段时间的氢氧化钠溶液,其中溶质的成分可能是:猜想①:NaOH;猜想②:Na2CO3;猜想③:。请设计实验证明猜想③正确。(写出相关的步骤和现象)
-
(3) 某海洋化工集团生产的碳酸钠产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%。为测定该产品中碳酸钠的质量分数,现取11.0g碳酸钠样品放入烧杯中,称得烧杯及所盛碳酸钠样品的总质量为158.0g,然后向烧杯中加入100g稀盐酸,充分反应,实验数据记录如下:
反应时间/min
3
6
9
12
烧杯及所盛物质的总质量/g
255.8
254.0
253.6
253.6
请你据此分析计算,该产品中碳酸钠的质量分数(是、否)符合标准。(写出计算过程,结果精确到0.1%)
-
(4) 小强同学想在社区宣传栏出一期“低碳减排·绿色生活”专刊,内容之一是汽车耗油量与二氧化碳排放量间关系。已知:①汽油密度约为0.7kg/L;②汽油(假定其为纯净物,根据汽油中C、H组成关系,其化学式可简单表示为CH2 , 其燃烧的化学方程式可表示为:2CH2+3O2
 2CO2+2H2O;请计算4升汽油完全燃烧生成二氧化碳的质量?
2CO2+2H2O;请计算4升汽油完全燃烧生成二氧化碳的质量?
- 分析法又称执果索因法,若用分析法证明:“设a>b>c,且a+b+c=0,求证<a”索的因应是() A.
- 下图是“我国第五次人口普查中四个省份的有关人口数据统计分析图”,读图判断①②③④所代表的省份依次是
- 从防止污染和减少用酸量的角度分析,下列制取Cu(NO3)2的方法中最好的是 A.CuCu(NO3)2
- 对于解决“白色污染”问题,下列叙述错误的是 A.减少使用不必要的塑料品,可用纸袋代替塑料袋
- 盘在地面上的一根不均匀的金属链重30 N,长1 m,从一端缓慢提起至另一端恰好离开地面时需做功10 J,金属链重力势能增
- 玉树地震中,党和政府及时采取一系列的措施为受灾群众提供了全方位的服务,赢得世界赞誉。这体现了: ①中国立党为公、执政为民
- 小张在2011年将30万资金全部用于投资股票,年底赚了10万。而2012年同样的投资却亏损了16万。小王在近两年内将30
- 已知函数数列的通项公式为. 当取得最小值时,的所有可能取值集合为 解答题(共90分)
- 下列措施对治理黄河无效的是 A.在中游植树种草 B.在下游加固大堤 C. 在黄土高原上修筑梯田 D. 在黄土
- 2011年06月27日金融时报报到,2011年节能减排工作会议总结了“十一五”期间人民银行系统节能减排工作的经验和成绩,
- Our house is on the top of the hill, and in winter the winds
- 下列计算,正确的是()A.B.C.D.
- 【答案解析】(1)4×104m/s.(2)π×10-5s,垂直地打在BC边的中点.(3)分析过程如上所述. 解析解:(1
- 在细胞工程中,需要利用细胞的全能性,下列细胞中全能性最高的是()A. 胡萝卜的韧皮部 B. 水稻的花粉 C. 绵羊的乳腺
- 下列剧种中,属于湖南地方剧种的是 A.京剧 B.昆剧 C.黄梅戏
- m g某金属M与含n mol HCl的盐酸恰好完全反应,生成MCl2和H2,则该金属的相对原子质量为() A.2m/n
- 根据下表中的已知条件,判断苏氨酸的密码子是-------( ) DNA双链 T G mRNA tRNA反密码子 A 氨基
- (10分)一个质量可不计的活塞将一定量的理想气体封闭在上端开口的直立圆筒形气缸内,活塞上堆放着铁砂,如图所示.最初活塞搁
- 有关遗传和变异的说法,正确的是 A.基因型为Dd的豌豆,产生的两种精子(或卵细胞)比例为1:1 B.自由组合定律的实质是
- — Would you mind my coming over andhaving a look at your new







