酸雨的产生、危害及防治 知识点题库
如图是某燃煤发电厂处理废气的装置示意图。下列说法不正确的是( )
火力发电厂用燃煤进行发电,由于煤中含有硫元素,燃烧时会产生二氧化硫,所以该发电厂采用石灰石浆吸收废气中的二氧化硫以防止污染大气,其发生反应的化学方程式为2CaCO3+2SO2+O2![]() 2CaSO4+2CO2 , 若处理2000t这种废气(假设废气中的二氧化硫全部被吸收),理论上需要62.6t含碳酸钙80%的石灰石.
2CaSO4+2CO2 , 若处理2000t这种废气(假设废气中的二氧化硫全部被吸收),理论上需要62.6t含碳酸钙80%的石灰石.
试解答:
-
(1) 若二氧化硫排放到空气中,会造成的环境污染问题是.
-
(2) 所吸收的废气中二氧化硫的质量分数是多少?
-
(1) 下列物质都可以用来作为燃料:①煤;②氢气;③石油;④天然气.其中,最清洁的燃料是(填序号).
-
(2)
充分燃烧1000g天然气和煤所产生的CO2和SO2气体的质量如图所示,根据图示分析,下列说法正确的是 .
 A . 煤燃烧产生的气体更易导致酸雨 B . 该天然气中不含硫元素 C . 煤燃烧对环境影响较小 D . 煤和天然气的燃烧都有温室气体产生
A . 煤燃烧产生的气体更易导致酸雨 B . 该天然气中不含硫元素 C . 煤燃烧对环境影响较小 D . 煤和天然气的燃烧都有温室气体产生 -
(3) 硫酸型酸雨的形成主要经过以下两步:①SO2在空气中被粉尘催化氧化得到SO3;②SO3与水化合形成硫酸.其中反应②的化学方程式为.
-
(4)
丙醇(化学式为C3H8O)是一种清洁燃料,它在一定量的氧气中燃烧的化学方程式可表示为C3H8O+4O2
 4H2O+2CO2+X,生成物X的化学式为.要使6.0g丙醇燃烧时不生成X,则消耗氧气的质量至少为g.
4H2O+2CO2+X,生成物X的化学式为.要使6.0g丙醇燃烧时不生成X,则消耗氧气的质量至少为g.
①水银②活性炭③生石灰④二氧化硫⑤碳酸钙⑥氢气
-
(1) 能够形成酸雨的是;
-
(2) 温度计中含有的物质是;
-
(3) 未来最清洁的燃料是;
-
(4) 石灰石的主要成分是;
-
(5) 溶于水放热的是;
-
(6) 防毒面具里填充的物质是.

能供给呼吸的是;可用于填充载人飞艇的是;
植物进行光合作用吸收的是;
用于仓库里储存粮食的气体是;引起酸雨的气体是。
①常用作灭火剂的物质是(填化学式)。
②能作有色光源的物质是(填化学式)。
③会引起酸雨的物质是(填化学式)。
④能作为清洁能源的物质是(填化学式)。
⑤能跟血液里的血红蛋白结合而使人中毒的物质是(填化学式)。

-
(1) 厨房清洁剂显性,在少量厨房清洁剂中滴入几滴酚酞,溶液呈色;
-
(2) 酸雨的酸性比正常雨水的酸性(填“强”或“弱”);
-
(3) 测量苹果汁pH时,pH试纸是否需要先用蒸馏水润湿(填“是”或“否”)。
-
(1) 稀盐酸能除铁锈(铁锈的主要成分是Fe2O3),写出稀盐酸除锈反应方程式,溶液的酸碱性,对生活、生产及人类的生命活动具有重要意义,把pH为酸雨;
-
(2) 现有:火碱溶液、Ba(NO3)2溶液、Na2CO3溶液、CuSO4溶液、稀硫酸,从以上5种物质中选出一种碱与一种盐反应并写出化学方程式。
-
(3) 天然气是一种重要的燃料,其主要成分为甲烷(CH4)。某课外兴趣小组同学对甲烷在氧气中完全燃烧后的产物进行探究。
①提出假设: A同学假设只生成CO2 , B同学假设只生成H2O,有同学认为A、B同学的假设都不完全正确,请你提出合理的猜想。
②实验验证: 为了验证你的猜想,可以将甲烷完全燃烧的产物依次通过进行检验(填物质名称)。

-
(1) 高速铁路非常平顺,时速能达到300公里以上。为保证行车的安全性和舒适性,高铁的钢轨是采用籾性好、硬度大的锰钢制成的,锰钢属于(填字母)
A.合成材料 B.金属材料 C.复合材料
-
(2) 高铁能够跑起来,依靠的是牵引供电系统给高速列车提供电力。高铁运行过程中完整的能量转化是:转化为。
-
(3) 火力发电厂发电时要消耗大量的煤炭资源,煤燃烧时会排放出、等污染物。这些气体或气体在空气中发生反应后的生成物溶于雨水,会形成。
酸雨是雨、雪等在形成和降落过程中,吸收并溶解了空气中的二氧化硫或氮氧化物等物质,形成的pH小于5.6的酸性降水。酸雨中的阴离子主要是硝酸根和硫酸根离子,根据两者在酸雨样品中的浓度可以判定降水的主要影响因素是二氧化硫还是氮氧化物。二氧化硫主要是来自于矿物燃料(如煤)的燃烧,氮氧化物主要是来自于汽车尾气等污染源。含有硫的煤燃烧生成二氧化硫,二氧化硫和水作用生成亚硫酸(H2SO3),亚硫酸在空气中被氧化成硫酸,雷雨闪电时,大气中也会产生少量硝酸,闪电时,氮气与氧气化合生成一氧化氮(NO),一氧化氮不稳定,在空气中被氧化成二氧化氮(NO2)。二氧化氮是一种红棕色、具有刺激性气味的气体,它可和水作用生成硝酸。酸雨对环境、工农业生产、建筑、森林植被等危害巨大,酸雨的危害已引起世界各国的普遍关注,依据文章内容,回答下列问题:
-
(1) 下列气体排放到空气中能形成酸雨的是____(填字母序号,下同)。A . CO2 B . NO2 C . CO D . SO2
-
(2) NO2的物理性质。
-
(3) 氮气与氧气反应的化学方程式为。
-
(4) 酸雨对下列物品有损害的是____。A . 大理石塑像 B . 铝制门窗 C . 钢铁结构大桥 D . 花草树木
-
(1) 谷雨——时雨乃降,五谷百果乃登。正常雨水pH≈5.6是由于空气中的溶解在雨水中造成的;
-
(2) 白露——白露满地红黄白,棉花地里人如海。鉴别棉花和羊毛的方法是。
-
(1) 下列说法中正确的是____(填字母)。A . 煤、石油和天然气都属于可再生能源 B . 从环境保护角度考虑,最理想的燃料是汽油 C . 可燃冰将成为未来新能源,其中主要含有甲烷水合物
-
(2) 煤燃烧时排放出的二氧化硫等污染物,有可能会导致降雨的酸性增强。我们把pH5.6(填“>”“=”或“<”)的降雨称为酸雨。某电厂为防止环境污染,用石灰石浆吸收二氧化硫,其反应的化学方程式为:
 , 则X的化学式为。
, 则X的化学式为。
-
(3) 我国科学家成功合成新型催化剂,能将CO2高效转化为甲醇(CH3OH)。该化学反应的微观过程如下图所示。

①反应前后,(填“分子”或“原子”)的种类不变,该反应的化学方程式为。
②该反应生成物丙和丁的质量比为(写最简比)。
-
(1) 任务一:分析酸雨的成因
【查阅资料】正常雨水的pH约为5.6,而酸雨是指pH<5.6的雨、雪或其他形式的降水。常见的酸雨有硫酸型、硝酸型和混合型。
【收集证据】同学们收集了一些刚降落的雨水水样,用pH计(测量pH的仪器)每隔五分钟测定一次雨水水样的pH,其数据如下:
测定时间
15:05
15:10
15:15
15:20
15:25
15:30
雨水的pH
4.95
4.95
4.94
4.88
4.86
4.85
【小组交流】
①正常雨水显酸性的原因是。
②酸雨的形成是因为在降雨过程中,雨水溶解了空气中的(填一种)等物质,并发生了一系列反应。在上述测定期间,雨水的酸性(填“增强”“减弱”或“基本不变”)。
-
(2) 任务二:探究酸雨的成分
【查阅资料】当地的酸雨主要含有颗粒物,Na+、K+、
 、H+和
、H+和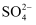 以及少量的
以及少量的 等。
等。【实验计划】验证酸雨中含有
 和
和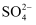
【进行实验】同学们将收集到的酸雨按一定比例浓缩,静置,分别取少量上层清液于两只试管中,按如图所示完成下列实验。

方案
实验操作
实验现象
实验结论
1
向A试管中滴加几滴X
产生白色沉淀
含有
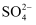
2
向B试管中滴加足量浓NaOH溶液,加热
有氨味
含有

【反思评价】
X是,其发生反应的化学方程式是。
-
(3) 小明提出:若用足量浓代替X和浓NaOH溶液,加热,只需进行一次实验即可得出最终结论,这一建议得到了其他同学的一致认可。
-
(4) 任务三:讨论酸雨的防治
【表达交流】
酸雨的危害不容忽视,防治酸雨刻不容缓。如何防治酸雨?请提出你的一条建议:。
- 如果|m|=﹣m,则m的取值范围是( ) A.m≤0 B.m<0 C.m≥0 D.m>0
- 如图所示,一网球运动员将球在边界处正上方水平向右击出,球刚好过网落 在图中位置(不计空气阻力),相关数据如图,下列
- 求下列函数的定义域.(1)y=;(2)y=;(3)y=++.
- 花草树木总能进入文人的视野,成为他们抒情的对象,如屈原《离骚》中的“扈江离与辟芷兮, 。”李清照《
- 已知函数f(x)=x2-mlnx,h(x)=x2-x+a. (1)当a=0时,f(x)≥h(x)在(1,+∞)上恒成立,
- 如图所示,表面粗糙的固定斜面顶端安有滑轮,两物块P、Q用轻绳连接并跨过滑轮(不计滑轮的质量和摩擦)P悬于空中,Q放在斜面
- 下列各句中,加点成语使用正确的一项是 A.北京城内的大茶馆已相继关了门。“裕泰”是硕果仅存的一家了,可是为避免被淘汰,它
- 要证明某溶液中不含Fe3+而可能含Fe2+,进行如下实验操作时的最佳顺序为() ①加足量氯水 ②加少量KMnO4溶液 ③
- 下列关于铁的叙述正确的是A.铁在潮湿的空气中易生锈 B.铁与稀硫酸反应,生成Fe2(SO4)3和H2C.能用铁桶盛农
- 下列表述正确的是 A. 用电子式表示氯化氢分子的形成过程: B.2CH3CH2OD+O22CH3CHO+2DHOC
- 下列有关铁的化学方程式中,书写正确的是( ) A. 4Fe+3O22Fe2O3 B .Fe+C
- 在中,,则角C的大小为( ) A.600 B.450 C.1200
- 在一定温度下,某体积不变的密闭容器中发生如下可逆反应:A2(g)+B2(g)2AB(g)。该反应达到平衡状态的标志是()
- 应用生物工程技术获得人们需要的生物新品种或新产品。请据图回答下列问题:(1)在培育转人生长激素基因牛过程中,①过程需要的
- 读图,回答下列:图中数码所对应的地质构造正确的是 A.①是背斜,④是地垒 B.①是地堑,③是地垒 C.②是断层,④是地
- 下图是反射弧的结构模式图,请据图回答(4分)(1)图中接受刺激并产生神经冲动的是[ ]______ (2)将神经冲动
- 右图表示某生态系统中甲、乙两种群在一段时间内数量变化情况。下列有关叙述错误的是( ) A.两个种群间能量流动方向是
- 下列关于遗传分子基础的叙述,正确的是 A.DNA分子一条链上相邻碱基之间通过氢键连接 B.核糖体通过核孔进入细胞核启动遗
- I shall never forget those years _______ I lived on the farm
- 分子式为C3H4Cl2链状有机物的同分异构体共有(不考虑顺反异构) A.4种 B.5种 C.6种 D.7种



