中和反应及其应用 知识点题库
|
|
|
|
A、分别向等质量的镁和锌中滴加足量的盐酸 | B、向pH=2的盐酸中滴加过量的氢氧化钠溶液 | C、向BaCl2和NaOH混合溶液中逐滴加入稀硫酸至过量 | D、向盐酸和氯化铜的混合溶液中加氢氧化钾溶液 |
 在稀盐酸中加入氯化铜,然后向其中逐滴加入 NaOH 溶液
B .
在稀盐酸中加入氯化铜,然后向其中逐滴加入 NaOH 溶液
B .  在 NaOH 溶液中加入 CaCO3 , 然后向其中逐滴加入稀盐酸
C .
在 NaOH 溶液中加入 CaCO3 , 然后向其中逐滴加入稀盐酸
C .  在 NaOH 溶液中加入 CuO,然后向其中逐滴加入稀硫酸
D .
在 NaOH 溶液中加入 CuO,然后向其中逐滴加入稀硫酸
D .  在 NaOH 溶液中加入 Ba(NO3)2 , 然后向其中逐滴加入稀硫酸
在 NaOH 溶液中加入 Ba(NO3)2 , 然后向其中逐滴加入稀硫酸
 K2MnO4+MnO2+O2↑
C . CaO+H2O═Ca(OH)2
D . Ca(OH)2+2HCl═CaCl2+2H2O
K2MnO4+MnO2+O2↑
C . CaO+H2O═Ca(OH)2
D . Ca(OH)2+2HCl═CaCl2+2H2O
A.对现象的认识 | B.化学与安全 |
①打开盛有浓盐酸的瓶盖,瓶口出现白烟 ②铁丝在空气里燃烧,火星四射 ③碳酸钠溶液里滴加酚酞,溶液变成红色 | ①稀酸溅入眼睛﹣﹣用大量水冲洗 ②进入地窖﹣﹣先做灯火实验 ③稀释浓硫酸﹣﹣先放水,再放浓硫酸 |
C.对除杂和鉴别的认识 | D.对概念的理解 |
①用稀盐酸除去氧化钙中含有的少量碳酸钙 ②用熟石灰鉴别硫酸铵和硫酸钾固体 ③用肥皂水鉴别硬水和软水 | ①能改变反应速率的物质,不一定是催化剂 ②生成盐和水的反应一定是中和反应 ③由一种元素组成的物质一定是单质 |
-
(1) 改良酸性土壤的碱(填化学式);
-
(2) 胃酸过多,服用胃舒平[Al(OH)3]发生反应的化学方程式:;
-
(3) 有一瓶溶液pH是4.5,如果要使溶液的pH升高,可以用的方法;
-
(4) 鉴别稀盐酸和稀硫酸最好选用试剂(填名称);发生反应的化学方程式为:;
-
(5) 不同的碱具有相似性质,但性质也存在差异。例如:氢氧化钠不能与碳酸钠溶液反应,而氢氧化钙溶液却能与其反应,原因是;
-
(6) 稀释浓硫酸的方法:.

实验操作步骤 | 实验现象 | 解释、结论与化学方程式 |
⑴取少量CuSO4粉末,向其中滴加几滴水 | CuSO4粉末 | 化学方程式: |
⑵向盛有无水醋酸的干燥试管中加入CuSO4粉末;另取一支干燥试管,向其中加入和。 | CuSO4粉末 | 实验说明: |
⑶将固体氢氧化钠加入盛有无水醋酸和CuSO4的试管里 | CuSO4粉末 | 结论: NaOH与醋酸反应有水生成 |

-
(1) 打开浓盐酸的试剂瓶,观察到瓶口有,这是因为浓盐酸有性。
-
(2) 根据如图写出反应的化学方程式。

-
(1) 请写出该中和反应方程式:。
-
(2) 猜想与假设:
猜想一:甲同学:“两种物质已恰好完全中和,溶液呈中性”;
猜想二:乙同学:“反应后氢氧化钠过量,溶液呈碱性”;
猜想三:丙同学:。
甲、丙两位同学经过讨论后觉得乙同学的猜想不正确,两位同学的理由是:。
-
(3) 设计并进行实验:
①为了验证自己的猜想,甲同学设计了以下实验方案:
实验步骤
实验现象
实验结论
用洁净干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比。
pH(填“>”、“=”或“<”)7
猜想一不成立
②请你设计另一个实验(与甲同学方案不同)方案,验证丙同学的猜想,并填写下表:
实验步骤
实验现象
实验结论
-
(4) 拓展探究:你还能设计不同的实验方案来验证丙同学的猜想吗?
实验步骤
实验现象
实验结论
-
(1) 计算氢氧化钠溶液的溶质质量分数;
-
(2) 该同学查阅资料发现,当溶液pH>8.2时,酚酞为红色,当溶液恰好为无色时,计算出的氢氧化钠溶液浓度(填“偏大”或“偏小”或“没有误差”)。


-
(1) 甲组同学向滴有酚酞溶液的稀盐酸中滴加NaOH溶液,振荡后溶液仍为无色,此现象(填“能”或“不能”)证明氢氧化钠与盐酸发生了反应;
-
(2) 乙组同学进行实验时,发现试管中出现了“怪现象”——有气泡产生。同学们通过讨论一致认为乙组同学所用的NaOH溶液已变质,写出产生气泡的化学方程式。
-
(3) 【提出问题】变质的NaOH溶液中含有哪些溶质?
【作出猜想】猜想一:;猜想二:NaOH、Na2CO3
-
(4) 【查阅资料】CaCl2溶液显中性。
【实验探究】

①滴加酚酞溶液后的现象为,证明猜想二成立。
②小丹同学用CuSO4溶液代替酚酞溶液也证明了猜想二成立,写出此反应的化学方程式。
【反思交流】实验室的化学药品应密封保存。
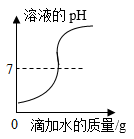 向一定量的稀盐酸中滴入水
B .
向一定量的稀盐酸中滴入水
B .  O2的溶解度与温度、压强的关系
C .
O2的溶解度与温度、压强的关系
C . 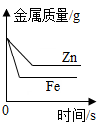 在等质量、等质量分数的两份稀硫酸中,分别加入过量且等质量的铁粉、锌粉
D .
在等质量、等质量分数的两份稀硫酸中,分别加入过量且等质量的铁粉、锌粉
D .  向稀硫酸和硫酸铜的混合溶液中加入足量的氢氧化钡溶液
向稀硫酸和硫酸铜的混合溶液中加入足量的氢氧化钡溶液
实验探究Ⅰ:在50 mL一定浓度的氢氧化钠溶液中滴加50 mL一定浓度的盐酸,并用玻璃棒搅拌,观察到溶液的温度升高,由此现象小李同学得出两者能发生反应的结论。通过查阅相关资料后,小张同学发现此结论不够严谨,设计了下列3个对比实验:
①50 mL一定浓度的盐酸与50 mL蒸馏水混合,测量溶液温度的变化。
②50 mL一定浓度的氢氧化钠溶液与50 mL蒸馏水混合,测量溶液温度的变化。
③50 mL一定浓度的盐酸与50 mL一定浓度的氢氧化钠溶液混合,测量溶液温度的变化。
用数字化实验技术测得3个实验,溶液温度随时间变化的关系如图所示。


-
(1) 由图可知,盐酸、氢氧化钠溶液稀释时均(填“放热”或“吸热”),但它们稀释时温度的变化量远两溶液混合时温度的变化量(填“大于”或“小于”)。
-
(2) 从微观角度分析,此中和反应的温度变化主要是由于(填离子符号)两种离子发生反应放出热量的缘故。
-
(3) 实验探究Ⅱ:
在50 mL一定浓度的氢氧化钠溶液中滴加2~3滴酚酞试液,再逐滴加入一定浓度的盐酸,并用玻璃棒搅拌,溶液颜色由红色刚好变为无色时,可说明两者发生了反应。该反应的化学方程式为。
-
(4) 取一定量反应后的无色溶液加热蒸发,在蒸发的过程中,“意外”发现溶液由无色又变成红色。同学们对红色溶液中溶质的成分(酚酞除外)进行再探究。
查阅资料:酚酞在pH<8.2的溶液中呈无色,在8.2<pH<14的溶液中呈红色。
【作出猜想】
猜想一:NaCl
猜想二:NaCl、NaOH
猜想三:NaCl、NaOH和

同学们讨论后一致认为猜想是错误的。
【实验验证】取样,滴加,无气泡产生,猜想三不正确。
-
(5) 【原因分析】反应后无色溶液中仍存在少量NaOH,加热蒸发,当溶液的pH在范围内,溶液的颜色变红。
-
(6) 【总结反思】向某碱性溶液中滴加2~3滴无色酚酞试液,振荡后溶液的颜色(填“一定”或“不一定”)变红。
- 有一种烃的分子结构如图所示,有关该分子的说法不正确的是A.该烯烃的分子式为C5H4 B.该分子中1、2、4、5四个碳原子
- 下列有关细胞的叙述错误的是 A.细胞在癌变过程中,细胞膜成分发生改变,表面的AFP(甲胎蛋白)等蛋白质可能会增加
- There was once a youngman who liked puppets (木偶) so much tha
- 一个四边形,截一刀后得到的新多边形的内角和将 ( ) A.增加180度
- 秦朝为加强中央集权而采取的措施是 A.废除分封制,实行郡县制 B.颁布
- 已知函数,若对任意都有成立,则的最小值是.
- It was the boy _____ had been in prison _____ stole the mone
- 如右图所示人体血液循环,图中①,②,③,④表示心脏各腔。据图回答下列问题。(5分) (1)体循环的途径是②
- One day I happened to meet an Englishman in the street and s
- _______ is known to us all, only the theory________ practic
- This kind of cakes ______ good while cakes of that kind ____
- 关于细胞结构与功能关系的描述中,错误的是 A.细胞壁是细胞这一最基本生
- 2011年,全国政协办公厅选编人民网“E政广场”上网友的30篇“E提案”,印发到每位全国政协委员手中。2012年全国“两
- 酶的活性部位往往与底物分子在空间结构上具有特殊的匹配关系,当酶与底物结合时,启动化学反应的发生。下列叙述能用图示解释的是
- 若,且αsinα-βsinβ>0,下面结论正确的是( ) A.α>β B.α+β>0
- 有关生物膜结构和功能的下列叙述中,错误的是( ) A. 细胞膜上载体蛋白的种类和数量决定了植物根细胞对无机盐离子的
- “在他心里,国为重,家为轻,科学最重 ,名利最轻,5年归国路,10年两弹成。”他说“我姓钱,但我不爱钱”。科学家钱学森不
- 下列离子在溶液中可大量共存,形成无色透明溶液的一组是 A. K+、Na+、OH—、MnO4- B. Ba
- Smith is a good student and studies very hard, _________.
- 俗话说,养兵千日,用兵一时。近年来我国军队进行了多种形式的军事演习。如图所示,在某次军事演习中,一辆战车以恒定的速率在起







