有关元素化合价的计算 知识点题库
交警常使用“酒精测试仪”对驾驶员是否酒后驾车进行测试。“酒精测试仪”中含有重铬酸钾(K2Cr2O7),其中铬元素(Cr)的化合价为( )
A . +2
B . +3
C . +6
D . +7
据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠[Na2SO3]等,可能会对人体的健康产生危害。Na2SO3中S元素的化合价为()
A . -2
B . +2
C . +4
D . +6
“酒驾”是当前热门的话题之一。交通巡逻警察检查驾驶员是否饮酒的仪器里装有K2Cr2O7 , K2Cr2O7中铬元素(Cr)的化合价为( )
A . +2
B . +5
C . +6
D . +7
据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠[Na2SO3]等,可能会对人体的健康产生危害。Na2SO3中S元素的化合价为( )
A . -2
B . +2
C . +4
D . +6
近年,卫生部发出通知:从2005年7月1日起禁止在面粉中加溴酸钾,因溴酸钾(KBrO3)会导致人的中枢神经紊乱,引发癌变。KBrO3中Br元素的化合价为 ( )
A . +1
B . +3
C . +5
D . -1
下列五种物质中均含有氮元素,它们按氮的化合物的顺序排列:①NH3②N2③NO④X⑤NaNO3 .
则根据这种排列规律,X可能是
A.NH4Cl B.N2O C.N2O3 D..
人们日常生活离不开金属,高科技新材料的开发和应用也需要金属.

-
(1) 地壳中含量最高的金属元素是
-
(2) 锂电池是一种新型的高能电池,其质量轻,电容量大,颇受手机、手提电脑等制造商的青睐.某种锂电池的总反应式为Li+MnO2=LiMnO2 , 其中化合价发生变化的元素是
-
(3) 根据如图金属应用实例推断,金属具有的物理性质有
-
(4) 日常使用的金属材料多数属于合金,如表列出了一些常见合金的主要成分和性能.由表推断,与组成合金的纯金属相比,合金的优点一般有(填序号)①强度更低;②硬度更高;③熔点更高;④抗腐蚀性更好.
合金
合金的主要性能
主要成分及纯金属的性能
焊锡
熔点183℃
锡:熔点232℃;铅:熔点327℃.
硬铝
强度和硬度好
铝、铜、镁等.硬度小,质软.
不锈钢
抗腐蚀性好
铁、铬、镍等.纯铁抗锈蚀性能不如不锈钢.
-
(5) 人们每年要从金属矿物资源中提取数以亿吨计的金属.根据所学化学知识,按要求写出一个生成金属的化学方程式:.
据报道,用于清洗龙虾的“洗虾粉”中含有柠檬酸钠、亚硫酸钠[Na2SO3]等,可能会对人体的健康产生危害.其中Na2SO3中,S元素的化合价为( )
A . ﹣2
B . +2
C . +4
D . +6
天宫二号是我国首个真正意义上的空间实验室。在太空舱里,常用  作催化剂将宇航员呼出的
作催化剂将宇航员呼出的 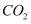 转化为
转化为  ,已知
,已知  中Ni 为+2价,则Fe的化合价为( )
中Ni 为+2价,则Fe的化合价为( )
 作催化剂将宇航员呼出的
作催化剂将宇航员呼出的 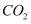 转化为
转化为  ,已知
,已知  中Ni 为+2价,则Fe的化合价为( )
中Ni 为+2价,则Fe的化合价为( )
A . +1
B . +2
C . +3
D . +4
由于高铁列车车厢是密闭的空间,因此提供清洁的空气、保持车厢的卫生非常重要。
-
(1) 高铁酸钠(Na2FeO4)是高铁上常用的一种“绿色环保高效”消毒剂。
①高铁酸钠中铁元素的化合价为;
②下面是一种制备高铁酸钠的反应原理:Fe2O3+3NaNO3+4NaOH=2Na2FeO4+3NaNO2+2X,X的化学式为。
-
(2) 某品牌的空气净化剂含有过氧化钠(Na2O2),它可以使车厢里的二氧化碳转化为碳酸钠和氧气,写出其化学反应方程式。
在点燃条件下,A和B反应生成C和D,反应前后分子变化的微观示意图如下:

回答问题:
-
(1) 构成B物质的基本粒子是
-
(2) 4种物质中,属于单质的是
-
(3) A物质中氢元素的化合价为+1,则氮元素的化合价为
运用图示法可以帮助我们巧学化学。下列化学知识用相应图示表示正确的是( )
A .  密度(常温常压)
B .
密度(常温常压)
B .  硫元素的化合价
C .
硫元素的化合价
C .  含碳量
D .
含碳量
D .  pH
pH
 密度(常温常压)
B .
密度(常温常压)
B .  硫元素的化合价
C .
硫元素的化合价
C .  含碳量
D .
含碳量
D .  pH
pH
玻璃中加入二氧化钒可以有选择地吸收和反射色光,二氧化钒(VO2)中钒元素的化合价为( )
A . +5
B . +4
C . +1
D . -4
工业上常用Na2SO3制亚硫酸纤维素酯、硫代硫酸钠、有机化学药品、漂白织物等,Na2SO3中硫元素的化合价是( )
A . +2
B . -2
C . +3
D . +4
消毒剂在公共场所的卫生防疫中发挥着重要作用。二氧化氯(ClO2)是一种高效、广谱、安全的杀菌消毒剂。以粗盐水(含可溶性杂质MgSO4、CaCl2)为原料制取ClO2的工艺流程如图:

-
(1) 试剂B为。
-
(2) 加入过量Na2CO3溶液的目的是。写出流程中发生化合反应的化学方程式:。
-
(3) 步骤④中发生反应的化学方程式为。
-
(4) ClO2中氯元素的化合价为,步骤⑤涉及的物质中含氯元素化合价最高的是。
-
(5) 上述流程中可循环利用的物质有。(填写物质的名称)
橄榄石(主要成分Mg2SiO4)可用来生产耐火材料。Mg2SiO4中硅元素的化合价是( )
A . -1
B . +2
C . +3
D . +4
生铁用途十分广泛。下图是工业上利用赤铁矿(主要成分是 Fe2O3 , 还含少量SiO2等杂质)冶炼生铁的过程示意图。

回答下列问题:
-
(1) ①生铁是常用的合金,生铁属于(填“纯净物”或“混合物”)。
②“高炉气体”中的(填化学式)会导致酸雨。
③ 炉渣的主要成分是CaSiO3 , 其中硅元素的化合价为。
-
(2) ① 利用下图所示实验装置可模拟工业炼铁。下列说法正确的是(填标号)

A实验时应先点燃酒精灯后通CO
B充分加热,a处固体由黑色变为红棕色
Cb处可用澄清石灰水检验生成的CO2
D可用NaOH溶液吸收尾气中的CO
②用化学方程式表示利用 CO 炼铁的原理。
-
(3) 生活中铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程。下列措施能防止铁制品锈蚀的是(填标号)。
A.涂油、喷漆 B.镀耐腐蚀的铬层 C.用盐水清洗 D.久置于酸性环境
黑火药是中因四大发明之一,其主要反应为 。下列说法正确的是( )
。下列说法正确的是( )
 。下列说法正确的是( )
。下列说法正确的是( )
A . X的化学式为2N
B . 参加反应的碳、硫质量比为3:1
C . KNO3中氮元素的化合价为+3
D . CO2中的“2”表示一个二氧化碳分子中含有2个氧原子
工业上制备单质镁的原理之一为:① 氧化镁与盐酸反应 MgO + 2HCl=MgCl2 + H2O;② 电解熔融氯化镁 MgCl2 Mg + Cl2↑。下列判断错误的是( )
Mg + Cl2↑。下列判断错误的是( )
 Mg + Cl2↑。下列判断错误的是( )
Mg + Cl2↑。下列判断错误的是( )
A . 镁元素在反应前后质量守恒
B . 反应①属于置换反应
C . 反应②应隔绝氧气进行
D . 反应中各元素的化合价均发生改变
工业上用绿矾(FeSO4·7H2O)制备还原铁粉(Fe)的部分转化过程如下:

-
(1) Ⅰ的反应为 FeSO4 +(NH4)2CO3=FeCO3↓+(NH4)2SO4 , 该反应的基本反应类型是。
-
(2) Ⅱ的反应中,铁元素的化合价(填“升高”“降低”或“不变”)。
最近更新
- 某历史兴趣小组在开展研究性学习时收集了亚历山大东征、丝绸之路、马可·波罗来华等素材,请你判断他们的研究主题是 A.帝国的
- 在“研究平面镜成像的特点”实验中,在玻璃板的一侧放一支点燃的蜡烛A,在玻璃板的另一侧放一支没有点燃的蜡烛B,当寻找像的位
- 维生素C(简称Vc,化学式为C6H8O6)是一种水溶性物质,其水溶性呈酸性,人体缺乏Vc易得坏血症,故Vc。又称抗坏血酸
- II语言知识及应用(共两节,满分35分) 第一节 完形填空(共10小题;每小题2分,满分20分) 阅读下面短文,掌握其
- 16、下列化学物质在相关实验中的作用正确的是( )
- 设,对于函数,下列结论正确的是 ( ) A.有最大值而无最小值 B.有最小值而无
- 实验室现有块状石灰石、高锰酸钾、稀硫酸、二氧化锰、棉花、木块及下列仪器:请回答下列同题: (1)仪器①的名称._____
- 某科研小组对黄瓜幼苗代谢问题进行了探究。右图一表示在适宜光照条件下黄瓜幼苗的一个细胞内发生的部分生理过程(用序号表示)。
- 为数列{}的前项和.已知>0,=. (Ⅰ)求{}的通项公式; (Ⅱ)设,求数列{}的前项和.
- 计算
- “若x、y∈R,且x2+y2=0,则x、y全为0”的否命题是()A.若x、y∈R,且x2+y2≠0,则x、y全不为0
- 下图所示为中纬度的某地区,仅从图中信息考虑,四点中最不可能形成城市聚落的是( )A.a B.b
- 人的糖蛋白必须经内质网和高尔基体进一步加工合成。通过转基因技术,可以使人的糖蛋白基因得以表达的受体细胞是:
- 阅读下面的文字,完成后面小题。(25分) 医者仁心、肝胆相照的吴孟超 林蔚 雅商 “医生眼里看的是病,心里装的是人。”吴
- 下列仪器中常用于物质分离的是 A.天平 B.分液漏斗 C.量筒
- 若大气降水是100%,以前渗入某城市地下和转化为城市地表径流的数量分别占降水的50%和10%。随着城市化进程,现在渗入地
- 小明一组的同学做灯泡串联的实验时,接通开关后发现L1较亮L2较暗,有四位同学对电流大小分别给出四种不同看法,你认为正确的
- 在等差数列{an}中,a1=-25,S3=S8,则前n项和Sn的最小值为 。 A.-80 B.-7
- 在发展中国家,大量农村人口迁往城市的原因有:①城市有较多的就业机会;②城市有较好的生活条件;③城市环境优美;④城市有较好
- 番菜争推一品香,西洋风味睹先尝。刀叉耀眼盆盘洁,我爱香槟酒一觞。”这一情景在上海最早可能出现于( ) A.明朝



